- Anunț important
02.06.2026
În atenția tuturor părților interesate (solicitanți/ beneficiari ) – referitor la obținerea avizelor de utilizare pentru dispozitivele medicale aflate în dotarea mijloacelor de intervenţie pentru asistenţă medicală de urgenţă prespitalicească (MIAMUP)
Va informăm că avizul de utilizare pentru dispozitivele medicale aflate în dotarea mijloacelor de intervenţie pentru asistenţă medicală de urgenţă prespitalicească (MIAMUP) nu reprezintă o autorizare a mijlocului de intervenție, ci o evaluare a dotării minime obligatorii și a performanțelor dispozitivelor medicale.
Cererea pentru emiterea avizului de utilizare a dispozitivelor medicale din dotarea MIAMUP trebuie sa fie însoțită de certificatul de înmatriculare sau carte de identitate emise de autoritățile din Romania – Direcția Generală Permise de Conducere și Înmatriculari sau Registrul Auto Român din care să reiasă că autovehicolul a fost încadrat anterior ca ambulanță.
Încadrarea autovehiculelor secondhand în categoria ambulanțelor de tip A,B, C etc., se realizează în baza documentelor de conformitate emise de producătorul /carosierul acestora și este obligatorie în procedura de evaluare a performanțelor dispozitivelor medicale aflate in dotarea minimă obligatorie a MIAMUP. - Anunț important
15.05.2026
În atenția persoanelor interesate
Comisia Europeană a organizat o serie de sesiuni de instruire online (web-streamed) în limba engleză, dedicate modulelor bazei de date EUDAMED, pentru a veni în sprijinul tuturor factorilor interesați din domeniul dispozitivelor medicale.
• 28 aprilie 2026, 11:00 – 19:00: Modulul pentru Actori (Actor module)
• 5 mai 2026, 11:00 – 19:00: Modulul UDI/Dispozitive (UDI/Devices module)
• 7 mai 2026, 11:00 – 19:00: Modulul Organisme Notificate și Certificate (Notified Bodies & Certificates module)
Înregistrările video ale celor trei workshopuri EUDAMED organizate de Comisia Europeană în perioada aprilie – mai 2026 sunt arhivate și pot fi vizionate integral prin intermediul link-urilui:
https://health.ec.europa.eu/latest-updates/upcoming-all-day-web-streamed-eudamed-trainings-2026-04-14_en
Pe lângă înregistrările video complete ale webinarilor, Comisia Europeană pune la dispoziție și Ghiduri video scurte (training videos) structurate pe sub-teme specifice (cum ar fi înregistrarea dispozitivelor de tip „legacy” etc) ce pot fi vizionate direct în secțiunea dedicată din:
https://webgate.ec.europa.eu/eudamed-help/en/onboarding-material/videos/training-videos.html
Vă recomandăm să accesați aceste sesiuni de instruire puse la dispoziție de Comisia Europeană având în vedere că utilizarea primelor patru module EUDAMED devine obligatorie începând cu data de 28 mai 2026. - Anunț important
04.05.2026
În atenția tuturor părților interesate (importatori/distribuitori, utilizatori)
Ca urmare a unei sesizări primite și a verificărilor efectuate de ANMDMR, atragem atenția tuturor părților interesate că au fost depistate pe piața din România prezervative Durex Intense falsificate, NR. LOT CUTIE 1002389669, DATA DE EXPIRARE 2030-03, și respectiv NR. LOT FOLII 1002286212, DATA DE EXPIRARE 2030-03 care ar fi fabricate de producătorul Reckitt Benckiser Healthcare (UK) Limited, UK.
Potrivit raportului producătorului, numărul lotului 1002389669, DATA DE EXPIRARE 2030-03, inscripționate pe cutia produsului nu corespund cu numărul original din fabrică, data de expirare corectă pentru acest lot este 2029-02, nu 2030-03, respectiv numărul lotului 1002286212, DATA DE EXPIRARE 2030-03, inscripționate pe foliile produsului nu corespund cu numărul original din fabrică, data de expirare corectă pentru acest lot este 2028-10, nu 2030-03.
În plus codificarea lotului de pe folii este neclară și nu corespunde cu produsul din fabrică, foliile identificate sunt conectate între ele, în timp ce în cutia produsului original, foliile sunt individuale.
Atenționăm părțile interesate să nu importe / distribuie sau achiziționeze, în vederea punerii la dispoziție pe piața din România sau utilizării, prezervative LOT CUTIE 1002389669 și LOT FOLII 1002286212 , marca DUREX, indiferent de numele (modelul/tipul) acestora, dacă sunt în termen de valabilitate, acestea fiind dispozitive medicale falsificate.
În cazul în care aveți cunoștință de importatori / distribuitori care au comercializat pe teritoriul României astfel de prezervative falsificate sau în cazul în care ați intrat în posesia unor astfel de prezervative falsificate, sesizați Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România – Serviciul Supraveghere Piață, la adresa de email sesizaridm@anm.ro sau la celelalte date de contact existente pe site-ul ANMDMR. - Anunț important
20.04.2026
În atenția tuturor părților interesate
Sesiuni de instruire online organizate de Comisia Europeană pentru modulele EUDAMED (aprilie – mai 2026)
Comisia Europeană organizează o serie de sesiuni de instruire online (web-streamed) în limba engleză, dedicate modulelor bazei de date EUDAMED, pentru a veni în sprijinul tuturor factorilor interesați din domeniul dispozitivelor medicale.
ANMDMR încurajează participarea la aceste sesiuni, care se vor desfășura conform următorului program:
• 28 aprilie 2026, 11:00 – 19:00: Modulul pentru Actori (Actor module)
• 5 mai 2026, 11:00 – 19:00: Modulul UDI/Dispozitive (UDI/Devices module)
• 7 mai 2026, 11:00 – 19:00: Modulul Organisme Notificate și Certificate (Notified Bodies & Certificates module)
Aceste sesiuni sunt esențiale pentru înțelegerea fluxurilor de lucru în EUDAMED și pentru asigurarea conformității cu legislația europeană privind dispozitivele medicale.
Link-urile de conectare vor fi disponibile pe site-ul Comisiei Europene la:
https://health.ec.europa.eu/medical-devices-eudamed/getting-ready_en#trainings
Menționăm că aceste sesiuni au un caracter demonstrativ, nu interactiv. Prin urmare, pe parcursul acestor webinare nu vor exista sesiuni de întrebări și răspunsuri (Q&A) sau posibilitatea de participare activă a audienței. - Anunț important
23.02.2026
În atenția tuturor importatorilor, distribuitorilor și utilizatorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România (ANMDMR) a fost informată cu privire la comercializarea pe teritoriul Uniunii Europene a unor unități falsificate ale produsului “COVID-19 and Influenza A+B Antigen Combo Rapid Test For Self-testing”, cu referința FCO-6032 și numărul de lot FCO24090516, fabricate de producătorul Safecare Biotech (Hangzhou) Co., Ltd., China.
Potrivit informațiilor intrate în posesia ANMDMR, produsele contrafăcute pot fi identificate prin următoarele elemente:
Pe ambalaj a fost aplicată o etichetă ce conține informații modificate referitoare la numărul lotului, data fabricației și data expirării, după cum urmează:
– Număr lot: FCO24090516
– Data fabricației: 09/2024
– Data expirării: 09/2026
– Numărul lotului și data de expirare au fost eliminate de pe caseta de testare inclusă în kit, astfel încât apar doar simbolurile
– Data de expirare a fost eliminată de pe tubul care conține soluția de extracție (tampon ).
– Bețișorul inclus în kit nu este același cu cel utilizat de producătorul original al produsului. Producătorul original al bețișoarelor este Dalian Rongbang Medical Healthy Devices Co. Ltd., cu reprezentantul autorizat Lotus NL, BV (Țările de Jos)
In plus, a fost identificat pe teritoriul Uniunii Europene și un alt lot contrafăcut cu numărul FCO2023020312, în timp ce numărul lotului original este FCO20230203.
În cazul în care ați intrat în posesia unor dispozitive medicale falsificate de tipul celor mai sus menționate sau în cazul în care aveți cunoștință de distribuitori care comercializează pe teritoriul României astfel de dispozitive, nu le utilizați și sesizați Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România la datele de contact existente pe site-ul ANMDMR. - Anunț important
28.01.2026
În atenția tuturor părților interesate
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România a fost informată cu privire la prezența pe piața UE și non-UE a unui software dezvoltat de producătorul Therapeak B.V., Țările de Jos, care oferă bolnavilor planuri de tratament, ca urmare a înregistrării pe site, completării unui chestionar și participării la sesiuni de 30 de minute cu un terapeut generat de inteligența artificială, în funcție de afecțiunea declarată.
Întrucât acest software are scop medical, de diagnosticare și/sau tratament al unei boli, dar nu îndeplinește cerințele de reglementare aplicabile dispozitivelor medicale din Regulamentul UE 2017/745 privind dispozitivele medicale (lipsă certificat de conformitate UE emis de un Organism Notificat), Autoritatea Competentă pentru dispozitive medicale din Țările de Jos a solicitat producătorului retragerea de pe piața UE a acestui software neconform.
În aceste condiții, Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toate părțile interesate să dea dovadă de atenție sporită, să nu acceseze site-urile în care se face referire la acest software neconform sau, în cazul în care au accesat deja acest software, să nu ia în considerare planurile de tratament generate prin inteligență artificială de acest software, ci să urmeze planurile de tratament stabilite de cadrele medicale din România care le au în evidență pentru respectivele afecțiuni. - Anunț important
26.01.2026
În atenția utilizatorilor și operatorilor economici care desfășoară activități cu dispozitive medicale
Vă aducem la cunoștință faptul că începând cu luna ianuarie 2026 tarifele pentru activităţile desfăşurate de Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale din România în domeniul dispozitivelor medicale au fost indexate cu rata medie a inflaţiei din anul 2025 și se regăsesc în Anexa 1 atașată acestui anunț.
descarcă Anexa 1 …
- Anunț important
28.11.2025
În atenția tuturor părților interesate
Comisia Europeană a publicat în Jurnalul Oficial al Uniunii Europene Decizia (UE) 2025/2371 din 26 noiembrie 2025 privind anunțul referitor la funcționalitatea și îndeplinirea specificațiilor funcționale ale anumitor sisteme electronice incluse în Baza europeană de date referitoare la dispozitivele medicale(EUDAMED):
https://eur-lex.europa.eu/legal-content/RO/TXT/PDF/?uri=OJ:L_202502371
Prin aceasta se confirmă faptul că următoarele sisteme electronice incluse în EUDAMED sunt funcționale și îndeplinesc specificațiile funcționale menționate la articolul 34 alineatul (2) din Regulamentul (UE) 2017/745:
• sistemul electronic pentru înregistrarea operatorilor economici (Actor registration) – menționat la articolul 30 din Regulamentul (UE) 2017/745(MDR) și la articolul 27 din Regulamentul (UE) 2017/746(IVDR);
• baza de date privind UDI și sistemul electronic pentru înregistrarea dispozitivelor (UDI/Device registration) – menționate la articolele 28 și 29 din Regulamentul (UE) 2017/745(MDR) și la articolele 25 și 26 din Regulamentul (UE) 2017/746(IVDR);
• sistemul electronic privind organismele notificate și privind certificatele (Notified Bodies and Certificates module) – menționat la articolul 57 din Regulamentul (UE) 2017/745(MDR) și la articolul 52 din Regulamentul (UE) 2017/746(IVDR);
• sistemul electronic de supraveghere a pieței (Market Surveillance) – menționat la articolul 100 din Regulamentul (UE) 2017/745(MDR) și la articolul 95 din Regulamentul (UE) 2017/746(IVDR).
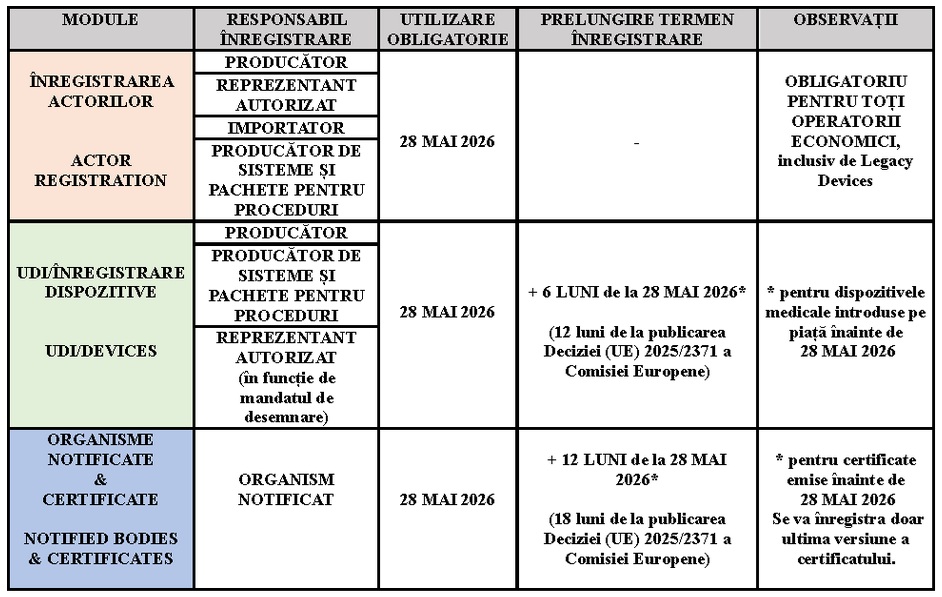
Obligațiile și cerințele legate de Eudamed se aplică de la data care corespunde unei perioade de șase luni de la data publicării menționate anterior(conform art. 123 din MDR, art. 113 din IVDR), respectiv din 28 mai 2026.
Potrivit prevederilor art. 123 din MDR/ art. 113 din IVDR termenele de înregistrare în EUDAMED sunt următoarele:
- Anunț important
07.10.2025
În atenția tuturor părților interesate
În cazul în care distribuitorii sau importatorii desfăşoară oricare dintre activităţile menţionate la art. 16 alin. (2) lit. (a) şi (b) din Regulamentul UE) 2017/745 privind dispozitivele medicale(MDR)/ Regulamentul UE) 2017/746 privind dispozitivele medicale pentru diagnostic in vitro(IVDR), aceştia trebuie să informeze ANMDMR cu privire la punerea la dispoziţie pe piaţă a dispozitivului reetichetat sau reambalat conform prevederilor art. 12 din OMS 3539/2022, respectiv OMS 3753/2023.
Distribuitorul sau importatorul tebuie să transmită la ANMDMR un certificat, eliberat de un organism notificat și desemnat pentru tipul de dispozitive care fac obiectul activităților menționate la art. 16 alin. (2) lit. (a) și (b) din MDR/IVDR, care atestă faptul că sistemul de management al calității al distribuitorului sau al importatorului este în conformitate cu cerințele prevăzute la art. 16 alin. (3) din MDR/IVDR.
Astfel, vă comunicăm că sunt acceptate doar certificatele emise de organismele notificate care conțin toate informațiile corespunzătoare cerințelor indicate în ghidul MDCG 2021-23 Guidance for notified bodies, distributors and importers on certification activities in accordance with Article 16(4) of Regulation (EU) 2017/745 and Regulation (EU) 2017/746.
descarcă documentul …
- Anunț important
29.08.2025
În atenția tuturor părților interesate
Potrivit informațiilor intrate în posesia ANMDMR, pe piața din Vietnam au fost identificate dispozitive medicale falsificate provenite de la un distribuitor din China.
Discrepanțele identificate de producătorul Thermoplastic Comfort Systems, Inc., SUA la dispozitivele medicale TCS Unbreakable Dental Resin falsificate constau în:
1. Prezența pe etichetă a marcajului CE urmat de numărul Organismului Notificat National Standards Authority of Ireland, Irlanda (0050), în condițiile în care dispozitivele medicale originale sunt încadrate în clasa I și conțin pe etichetă doar marcajul CE.
2. Întreaga etichetă, configurația ambalajului și distribuția informațiilor diferă față de dispozitivele medicale originale.
3. Eticheta dispozitivelor medicale falsificate a fost copiată de pe versiunile anterioare ale etichetei dispozitivelor medicale originale, atunci când produsul necesita implicarea unui organism notificat în vederea introducerii pe piață, iar marcajul CE urmat de numărul organismului notificat figura pe etichetă.
În cazul în care ați intrat în posesia unor dispozitive medicale falsificate de tipul celor mai sus menționate sau în cazul în care aveți cunoștință de distribuitori care comercializează pe teritoriul României astfel de dispozitive, nu le utilizați și sesizați Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România la datele de contact existente pe site-ul ANMDMR. - Anunț important
04.08.2025
În atenția tuturor părților interesate
ANMDMR a fost informată despre prezența pe teritoriul Portugaliei a unui produs falsificat compus din medicamentul Ozempic 1 mg, lot NF63704 și dispozitivul medical ac NovoFine Plus 32G 4mm, lot NE61324-2.
Potrivit producătorului Novo Nordisk A/S, Danemarca, acele NovoFine Plus 32G 4mm din lotul original au alte date de fabricație și de expirare, după cum urmează:
Lotul NE61324-2 original a fost fabricat la 29.04.2023 și expiră la 31.03.2028.
Lotul NE61324-2 falsificat a fost fabricat la 04.2024 și expiră la data de 03.2029.
În cazul în care ați intrat în posesia unor astfel de produse falsificate nu le utilizați și sesizați Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România la datele de contact existente pe site-ul ANMDMR. - Anunț important
01.08.2025
În atenția tuturor celor interesați
ANMDMR atenționează cu privire la retragerea certificării CE pentru dispozitivul medical Los Deline – gel hidrofilic pentru endoprotezarea țesuturilor moi ale corpului uman, producător BIOTRH S.R.O., Republica Cehă. Acest dispozitiv medical este un produs injectabil, neresorbabil, pe bază de copoliamidă, utilizat în principal în scopuri estetice, pentru creșterea volumului corporal, la nivel de sâni și fese.
Retragerea certificării CE a fost decisă de Organismul Notificat la data de 02.05.2023, ca urmare a rezultatelor nesatisfăcătoare ale unui test de reactivitate intracutanată.
Potrivit informațiilor intrate în posesia ANMDMR, după retragerea certificatelor, prin Notificarea în materie de siguranță în teren FSN-23-002-PR, producătorul BIOTRH S.R.O., Republica Cehă a solicitat retragerea de pe piață a tuturor dispozitivelor medicale Los Deline 100g rămase neutilizate, preconizate că se mai aflau pe teritoriul următoarelor state: Suedia, Germania, Italia, Grecia, Turcia, Elveția, Cipru, Franța și Norvegia.
Termenul limită de retragere a acestor dispozitive de pe teritoriul UE a fost 30 noiembrie 2023, însă având în vedere perioada de valabilitate a acestor dispozitive (3 ani) și faptul că acestea au fost comercializate inclusiv în țări din afara UE de unde pot pătrunde pe teritoriul UE, ANMDMR recomandă atât profesioniștilor din domeniul sănătății cât și pacienților să manifeste prudență maximă și în cazul în care au intrat în posesia unor astfel de dispozitive sau au cunoștință de distribuitori care comercializează pe teritoriul României altfel de dispozitive să nu le utilizeze și să sesizeze Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România – Serviciul Supraveghere Piață la datele de contact existente pe site-ul ANMDMR. - Anunț important
31.07.2025
În atenția producătorilor români de dispozitive medicale și dispozitive medicale pentru diagnostic in vitro și a tuturor părților interesate
Potrivit Deciziei de punere în aplicare (UE) 2019/939 a Comisiei din 6 iunie 2019 pentru desemnarea entităților emitente însărcinate cu operarea unui sistem de atribuire a identificatorilor unici ai dispozitivelor în domeniul dispozitivelor medicale, reînnoită pentru o perioadă de cinci ani, de la 27 iunie 2024 până la 27 iunie 2029 prin Decizia de punere în aplicare (UE) 2024/2120 a Comisiei din 30 iulie 2024 de reînnoire a desemnării entităților emitente însărcinate cu operarea unui sistem de atribuire a identificatorilor unici ai dispozitivelor în domeniul dispozitivelor medicale, au fost recunoscute oficial de către Comisia Europeană ca entități emitente UDI următoarele organizații:
– GS1 AISBL,
– Health Industry Business Communications Council (HIBCC)
– ICCBBA
– Informationsstelle für Arzneispezialitäten — IFA GmbH
Aceste decizii au fost publicate în Jurnalul Ofícial al Uniunii Europene.
Astfel, vă informăm că doar aceste 4 entități sunt desemnate de către Comisie și pot emite UDI.
În cazul în care ați contractat o altă organizație în afara celor 4 enumerate mai sus pentru emiterea sistemului de identificare unică a unui dispozitiv („sistemul UDI”) sau în cazul în care aveți cunoștință de astfel de organizații care pretind că sunt entități emitente UDI, este necesar să sesizați Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România – Direcția Reglementare, Supraveghere piață la datele de contact existente pe site-ul ANMDMR (dgdm@anm.ro și drsp@anm.ro). - Anunț important
04.07.2025
În atenția producătorilor români de dispozitive medicale și dispozitive medicale pentru diagnostic in vitro și a tuturor părților interesate
Vă informăm că începând cu 26 mai 2025, toți producătorii de dispozitive medicale, indiferent de clasa de risc a dispozitivului medical, au obligația de aplicare a suportului UDI pe eticheta dispozitivelor medicale și pe toate nivelurile superioare de ambalare conform articolului 123 alineatul (3) litera (f) și articolului 27 alineatul (4) din MDR.
De asemenea, această obligație se aplică și tuturor producătorilor de dispozitive medicale pentru diagnostic in vitro încadrate în clasele de risc B, C, D conform articolului 113 alineatul (3) litera (e) și articolului 24 alineatul (4) din IVDR.
Pentru dispozitivele medicale pentru diagnostic in vitro încadrate în clasa de risc A, aplicarea suportului UDI pe etichetă este obligatorie începând cu 26 mai 2027. - Anunț important
04.07.2025
În atenția tuturor importatorilor, distribuitorilor și utilizatorilor de dispozitive medicale
ANMDMR a fost informată despre confiscarea de către Autoritățile vamale din Suedia a unor dispozitive medicale Sculptra contrafăcute, aparținând loturilor A6108 (dată expirare 12/2026) și A00203 (dată expirare 04/04/2027).
Producătorul dispozitivelor originale Sculptra, Poly-L-Lactic Acid, compania Q-Med AB Galderma, Suedia, a confirmat că ambele loturi sunt contrafăcute, iar lotul A00203 este unul recurent.
Potrivit verificărilor efectuate de Autoritatea Competentă pentru dispozitive medicale din Suedia, flacoanele Sculptra contrafăcute sunt marcate CE 0344, nu conțin PLLA (Poly-L-Lactic Acid), ingredientul principal din dispozitivele Sculptra originale și conțin glucoză, un ingredient care nu se regăsește în dispozitivele Sculptra originale.
Sculptra, Poly-L-lactic acid este un biostimulator utilizat pentru corectarea depresiunilor cutanate (cute, riduri, pliuri, cicatrici) și pentru îmbătrânirea pielii, precum și pentru corecții de volum mare, în caz de pierdere a grăsimii faciale (lipodistrofie).
În cazul în care ați intrat în posesia dispozitivelor medicale din loturile contrafăcute A6108 (dată expirare 12/2026) și A00203 (dată expirare 04/04/2027) sau în cazul în care aveți cunoștință de distribuitori care comercializează pe teritoriul României altfel de dispozitive, nu le utilizați și sesizați Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România – Serviciul Supraveghere Piață la datele de contact existente pe site-ul ANMDMR. - Anunț important
25.06.2025
În atenția producătorilor de dispozitive medicale cu sediul în România
Vă informăm că producătorii români care notifică la ANMDMR dispozitive medicale în vederea înregistrării în baza națională de date în conformitate cu Ordinul ministrului sănătății nr. 3.539/2022 pentru aprobarea Normelor metodologice privind introducerea pe piaţă a dispozitivelor medicale și înregistrarea operatorilor economici în Baza europeană de date referitoare la dispozitivele medicale (Eudamed), precum și în baza națională de date și de derogare de la procedurile de evaluare a conformităţii sauOrdinul ministrului sănătății nr. 2.845 din 29 Septembrie 2022 privind aprobarea Normelor metodologice pentru aplicarea prevederilor art. 13 din Ordonanţa de urgenţă a Guvernului nr. 46/2021 privind stabilirea cadrului instituţional şi a măsurilor pentru punerea în aplicare a Regulamentului (UE) 2017/745 al Parlamentului European şi al Consiliului din 5 aprilie 2017 privind dispozitivele medicale, de modificare a Directivei 2001/83/CE, a Regulamentului (CE) nr. 178/2002 şi a Regulamentului (CE) nr. 1.223/2009 şi de abrogare a Directivelor 90/385/CEE şi 93/42/CEE ale Consiliului, privind înregistrarea dispozitivelor fabricate la comandă introduse pe piaţă sub propriul nume de producătorii cu sediul în România trebuie să prezinte în documentația aferentă solicitării Certificatul de înregistrare la ONRC și un certificat constatator din care să rezulte autorizarea activității de fabricare a dispozitivelor medicale, prin indicarea codului CAEN (rev.3), specifică tipului de dispozitiv medical notificat.Exemple:
CAEN 3250, Fabricarea de dispozitive, aparate și instrumente medicale stomatologice pentru:
- fabricarea de pânze chirurgicale și catgut,
- fabricarea de aparate de distilat și centrifuge de laborator,
- fabricarea de mobilier medical, chirurgical, stomatologic,
- fabricarea de articole oftalmice, ochelari de vedere, lentile șlefuite conform rețetei, lentile de contact,
- fabricarea de măști de protecție de unică folosință (măști chirurgicale, măști FFP2, FFP3, etc)
CAEN 2120, Fabricarea preparatelor farmaceutice
- fabricarea preparatelor de diagnosticare medicală, inclusiv teste de sarcină,
- fabricarea substanțelor de diagnosticare radioactivă in- vivo,
- fabricarea vatei, tifonului, feșelor, bandajelor medicinale impregnate, a catgutului chirurgical, etc.
- fabricarea de echipamente medicale cu ultrasunete,
- fabricarea de electrocardiografe,
- fabricarea de echipamente medicale endoscopice
CAEN 2660, Fabricarea de echipamente pentru radiologie, electrodiagnostic și electroterapie
CAEN 6210, Activități de realizare a softului la comandă
Realizare software – dispozitiv medical
- Anunț important
16.06.2025
În atenția tuturor importatorilor, distribuitorilor și utilizatorilor de dispozitive medicale
ANMDMR a fost informată despre un caz de furt produs în Belgia în data de 10 Aprilie 2025 în care a fost implicat un camion care transporta filere Juvederm din Pringy, Franța în Roermond, Țările de Jos. Ancheta a descoperit că 25 din 26 de paleți au fost furați.
Toate stocurile rămase la producătorul AbbVie, Franța din loturile afectate precum și toate dispozitivele rămase în camion care nu au fost furate vor fi distruse.Dispozitivele medicale și loturile afectate sunt:
Cod produs PRODUS LOT Cantitate Piețe afectate 20076422 Juvéderm VOLUX 1003645951 4.513 Număr de referință dedicat pentru China 94151JA Juvéderm Vista VOLUMA XC 1003583816 4.954 Număr de referință dedicat pentru Japonia 94506KO Juvederm VOLUMA cu Lidocaină 1003598746 1003598748
8.572 7.095
Număr de referință dedicat pentru Coreea de Sud. 96637JR Juvederm VOLUMA cu Lidocaină 1003598743 6.311 Număr de referință comun pentru țările UE si planificat a fi livrat în Germania, Italia, Austria și Elveția (pachet multilingv) 20073835 SKINVIVE by Juvederm 2*1mL 1003543583 4.221 Număr de referință dedicat pentru India 96180II PF Juvederm Volbella w/lidocaine 32G 1003645893 919 Număr de referință dedicat pentru India 96666JR JUVEDERM ULTRA 3 2*1.0mL 1003636606 5.268 Număr de referință comun pentru pentru țările UE si planificat a fi livrat în Germania, Italia, Austria și Elveția (pachet multilingv) În cazul în care ați intrat în posesia unor dispozitive medicale de tipul celor mai sus menționate sau în cazul în care aveți cunoștință de distribuitori care comercializează pe teritoriul României altfel de dispozitive, nu le utilizați și sesizați Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România – Supraveghere Piață la datele de contact existente pe site-ul ANMDMR.
- Anunț important
03.06.2025
În atenția persoanelor interesate
Lista furnizorilor de instruire având ca tematică legislația în domeniul dispozitivelor medicale, agreați de ANMDMR
Conform Normelor, pentru obținerea avizului de funcționare, operatorul economic trebuie să dispună de personal suficient și calificat/instruit pentru activitatea pe care o desfășoară/domeniul în care activează.
Persoana responsabilă de conformitatea cu reglementările (PRCR) specifice domeniului dispozitivelor medicale și șeful de depozit trebuie să facă dovada participării la cursuri de instruire având ca tematică legislația în domeniul dispozitivelor medicale.
descarcă documentul
- Anunț important
20.03.2025
În atenția instituțiilor sanitare
În data de 27 februarie 2025 a fost publicat în Monitorul Oficial partea I, Ordinul ministrului sănătății nr. 650 privind aprobarea normelor de procedură pentru aplicarea prevederilor art. 5 alin. (5) din Regulamentul (UE) 2017/745 al Parlamentului European şi al Consiliului din 5 aprilie 2017 privind dispozitivele medicale, de modificare a Directivei 2001/83/CE, a Regulamentului (CE) nr. 178/2002 şi a Regulamentului (CE) nr. 1.223/2009 şi de abrogare a Directivelor 90/385/CEE şi 93/42/CEE ale Consiliului privind dispozitivele medicale şi dispozitivele medicale pentru diagnostic in vitro fabricate şi utilizate doar în cadrul instituţiilor sanitare
Acest ordin reglementează aspectele referitoare la fabricarea și utilizarea în cadrul instituțiilor sanitare a dispozitivelor medicale/ dispozitivelor medicale pentru diagnostic in vitro precum și aspectele referitoare la notificarea utilizării unor astfel de dispozitive către ANMDMR. Actul normativ poate fi consultat în secțiunea Dispozitive medicale/ Legislație/ Ordine de ministru.
Formularul utilizat pentru notificarea fabricării și utilizării unor astfel de dispozitive medicale se regăsește în secțiunea “Dispozitive Medicale/Formulare și tarife” sub codificarea F.MD/IVD_IS. Menționăm că analiza notificării și a dosarului aferent este o activitate tarifată OMS nr. 3.467/17.11.2022 privind aprobarea cuantumului tarifelor pentru activităţile desfăşurate de Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale din România în domeniul dispozitivelor medicale, cu cuantumul tarifelor indexate 2025.
Formularul de plată aferent acestei activități se regăsește în secțiunea “Dispozitive Medicale/Formulare și tarife” sub denumirea ”Formular pentru plata tarifului – EVALUARE DOSAR DE NOTIFICARE DISPOZITIVE MEDICALE FABRICATE ŞI UTILIZATE ÎN CADRUL UNITĂŢILOR SANITARE PUBLICE SAU PRIVATE / EVALUARE DOSAR DE NOTIFICARE A UNEI MODIFICĂRI DE DISPOZITIVE MEDICALE FABRICATE ŞI UTILIZATE ÎN CADRUL UNITĂŢILOR SANITARE PUBLICE SAU PRIVATE” - Anunț important
10.03.2025
În atenția utilizatorilor și distribuitorilor de dispozitive pentru monitorizarea glicemiei
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează utilizatorii și distribuitorii de dispozitive medicale cu privire la creșterea numărului de reclame înșelătoare care apar pe platformele de social media (ex. Facebook, Instagram, TikTok) dar și pe unele pagini de internet, reclame care pretind existența pe piață a unor dispozitive de monitorizare a glicemiei (glucometre) non-invazive. Aceste reclamele înșelătoare de pe internet promovează dispozitive îndoielnice de monitorizare a glicemiei (glucometre) non-invazive printre care enumerăm: glucometru nedureros și neinvaziv; monitorizare completă fără înțepături, glucometru multifuncțional de nouă generație; monitorizare completă a stării, glucometru multifuncțional; măsurător laser non-invaziv; glucometru neinvaziv de înaltă precizie; glucometru neinvaziv; dispozitiv medical neinvaziv premium etc.
Atragem atenția tuturor celor interesați că, pentru a spori credibilitatea, în vederea escrocării persoanelor vulnerabile și comercializării dispozitivelor îndoielnice de monitorizare a glicemiei (glucometre) non-invazive, se folosesc afirmații înșelătoare privind originile produselor, acestea fiind promovate ca aparținând în mod fals unor producători de renume din domeniul dispozitivelor medicale.
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România recomandă tuturor părților interesate ca, înainte de orice achiziție, să verifice informațiile despre dispozitivele medicale din surse de încredere și, în cazul identificării de reclame înșelătoare să nu acceseze link-urile, să nu distribuie sau să cumpere produsele promovate în astfel de reclame. - Anunț important
25.02.2025
În atenția utilizatorilor și distribuitorilor de dispozitive de monitorizare a funcțiilor vitale pentru pacienți, Contec CMS8000 și Epsimed MN-120
În urma semnalării de către autoritățile din domeniul securității cibernetice a unor posibile vulnerabilități critice de tip backdoor, adică accesarea dispozitivului de către un atacator și încărcarea sau modificarea fișierelor stocate pe acesta, punând în pericol securitatea datelor și integritatea sistemului, Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România recomandă:
– Evitarea conectării la rețeaua de internet a acestor dispozitive medicale;
– Monitorizarea permanentă a traficului de rețea pentru a identifica semne ale unor activități suspecte – în cazul în care mențineți dispozitivul conectat la internet;
– Transmiterea de urgență către ANMDMR a oricăror semnale de funcționare anormală, cum ar fi neconcordanțe între funcțiile vitale afișate ale pacientului și starea fizică reală a acestuia, prin completarea Formularului de raportare a incidentelor grave suspectate în legătură cu dispozitivele medicale sau dispozitivele medicale pentru diagnostic in vitro – pentru profesioniști din domeniul sănătăţii, utilizatori şi pacienți (https://www.anm.ro/dispozitive-medicale/raporteaza-un-incident/). - Anunț important
23.01.2025
În atenția tuturor operatorilor economici
Vă aducem la cunoștință faptul că începând cu luna ianuarie 2025 tarifele pentru activităţile desfăşurate de Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale din România în domeniul dispozitivelor medicale au fost indexate cu rata medie a inflaţiei din anul 2024 și se regăsesc în Anexa 1 atașată acestui anunț.
descarca documentul…
- Anunț important
09.01.2025
În atenția persoanelor interesate
Comisia Europeană a lansat pe site-ul său (https://ec.europa.eu/ eusurvey/ runner/ 2024MD Availability MFARIMDB survey) a doua consultare publică destinată operatorilor economici (producători, reprezentanți autorizați, importatori sau distribuitori) în ceea ce privește dispozitivele medicale și dispozitivele de diagnostic in vitro în cadrul studiului derulat pentru monitorizarea disponibilității dispozitivelor medicale pe piața Uniunii Europene (HADEA/2021/P3/03).
Mai multe informații despre participare, confidențialitate și alte detalii despre acest studiu sunt disponibile la: https://health.ec.europa.eu/study-supporting-monitoring-availability-medical-devices-eu-market_en și la: https://ppri.goeg.at/Study_MD_Availability.
Termenul de participare este 28 februarie 2025.
Scopul acestui studiu este de a colecta informații despre tranziția dispozitivelor la Regulamentele UE pentru dispozitive medicale (MDR) și in vitro (IVDR). Chestionarul conține și întrebări referitoare la evaluarea țintită în curs de desfășurare de către Comisia Europeană. Prima consultare publică a furnizat date esențiale și rezultatele sunt accesibile utilizând un tablou interactiv și în forma unei prezentări PPT.
Studiul este condus de Gesundheit Österreich GmbH (GÖG), Institutul Național Austriac pentru Sănătate Publică, în colaborare cu Areté și CivicConsulting și comisionat de către Comisia Europeană – Directoratul General pentru Sănătate și Siguranța Alimentelor (DG SANTE) prin intermediul Agenției Executive Europeane pentru Domeniile Sănătății și Digital (HaDEA). - Anunț important
23.12.2024
În atenția persoanelor interesate
Având în vedere aprobarea Ordinului ministrului sănătății nr. 5930 din data de 11.12.2024 privind modificarea și completarea anexei la Ordinul ministrului sănătății nr. 194/2015 privind aprobarea Normelor pentru evaluarea şi avizarea publicităţii la medicamentele de uz uman, vă informăm ca s-a modificat modalitatea de transmitere a formularelor de declarare a activităților de sponsorizare:
articolul 35, alineatele (5) și (7) se modifică și vor avea următorul cuprins:
”(5) Declararea activităţilor de sponsorizare, precum şi a celorlalte cheltuieli, altele decât sponsorizarea, efectuate în condiţiile alin. (3) şi (4) se va realiza conform formularelor al căror model este prevăzut în anexele nr. 1 şi 2, prin semnătură electronică potrivit prevederilor art. 3 pct. 11 şi 12 din Regulamentul (UE) nr. 910/2014, prin intermediul aplicațiilor online care pot fi accesate pe portalul ANMDMR: portal.anm.ro.”
Vă solicitam să folosiți această modalitate de transmitere a formularelor de declarare, unica modalitate de transmitere a formularelor către ANMDMR conform prevederilor legale.
Vă rugăm ca înainte de completarea și transmiterea formularelor de declarare a activităților de sponsorizare să consultați Ghidul de completare atât pentru beneficiari cât și pentru sponsori. - Anunț important
17.12.2024
În atenția persoanelor interesate
Comisia Europeană a lansat pe site-ul său (https://ec.europa.eu/info/law/better-regulation/have-your-say/initiatives/14155-EU-rules-on-medical-devices-and-in-vitro-diagnostics-targeted-evaluation_en) o cerere de participare la consultarea publică în scopul evaluării țintite a reglementărilor UE pentru dispozitive medicale și dispozitive de diagnostic in vitro.
Rezultatele consultării vor contribui la evaluarea
• eficienței, eficacității și proporționalității
• satisfacerii nevoilor actuale și emergente
• alinierii cu alte acțiuni europene
• valorii adăugate la nivelul UE
ale regulamentelor MDR și IVDR.
În același timp, Comisia Europeană și-a intensificat eforturile de a furniza instrumentele de implementare necesare.
Cele mai recente actualizări și completări ale cadrului necesar implementării MDR și IVDR sunt publicate pe https://health.ec.europa.eu/medical-devices-sector/new-regulations_en: regulamente de aplicare a MDR și IVDR, ghiduri și broșuri pentru toate părțile interesate, de clarificare și susținere în înțelegerea corectă și aplicarea prevederilor legale, precum și linkuri la modele de documente impuse de legislație și întocmite de asociații profesionale europene din domeniu pentru producători și alți actori ai pieței dedicate:- Întrebări și răspunsuri referitoare la perioadele de tranziție ale IVDR (Q&A Extension of the IVDR transitional periods)
- Template pentru declarația producătorului de IVD în perioada de tranziție de pe site-ul MedTech Europe
- Template pentru acordul scris și emis de un organism notificat (Template for notified body confirmation letter endorsed by NBCG-Med)
- Întrebări și răspunsuri referitoare la obligația de a informa întreruperile sau încetările Q&A Obligation to inform in case of interruption or discontinuation of supply
- Formularul de raportare a unei întreruperi sau încetări în producția unui dispozitiv medical (MDCG 2024-16: Manufacturer Information Form on Interruption or Discontinuation of Supply of certain medical devices and certain in vitro diagnostic medical devices)
- Tabel de identificare al dispozitivului (MDCG 2024-16 Annex: Device Identification table)
Vă invităm de asemenea să consultați periodic și pagina dedicată ghidurilor (documentelor de orientare) pentru implementarea MDR și IVDR (https://health.ec.europa.eu/medical-devices-sector/new-regulations/guidance-mdcg-endorsed-documents-and-other-guidance_en), care au fost recent actualizate de către MDCG) și în special a celor pentru:
• Aplicarea prevederilor MDR dispozitivelor legacy: MDCG 2021-25 rev.1, Application of MDR requirements to “legacy devices” and to devices placed on the market prior to 26 May 2021 in accordance with Directives 90/385/EEC or 93/42/EEC (https://health.ec.europa.eu/document/download/cbb11a6e-f0f3-4e30-af5e-990f9ef68bc1_en?filename=md_mdcg_2021_25_en.pdf )
• Calificarea ca dispozitive de diagnostic in vitro MDCG 2024-11 Guidance on qualification of in vitro diagnostic medical devices (https://health.ec.europa.eu/document/download/12b92152-371f-404d-a865-93800cd5cdca_en?filename=mdcg_2024-11_en.pdf )
• Implementarea regulilor pentru Master UDI-DI pentru lentilele de contact în ce privește structura, acordarea, etichetarea și înregistrarea în Eudamed, MDCG 2024-14, Guidance on the implementation of the Master UDI-DI solution for contact lenses (https://health.ec.europa.eu/document/download/c8c6cca5-460e-410e-a325-be08bfc7dea6_en?filename=mdcg_2024-14_en.pdf )
• Cerințe de reglementare pentru oxidul de etilenă, MDCG 2024-13, Regulatory status of ethylene oxide (EtO) intended for the sterilisation of medical devices (https://health.ec.europa.eu/document/download/3fa74c6b-953a-41f5-b024-8889ac8b5ddf_en?filename=mdcg_2024-13_en.pdf )
• Produse de graniță între dispozitive medicale și medicamente, MDCG 2022-5 rev.1, Guidance on borderline between medical devices and medicinal products under Regulation (EU) 2017/745 on medical devices (https://health.ec.europa.eu/document/download/b5a27717-229f-4d7a-97b1-e1c7d819e579_en?filename=mdcg_2022-5_en.pdf) - Întrebări și răspunsuri referitoare la perioadele de tranziție ale IVDR (Q&A Extension of the IVDR transitional periods)
- Anunț important
13.12.2024
În atenția producătorilor și tuturor părților interesate
Vă informăm că, începând cu data de 10 ianuarie 2025 producătorii români vor avea obligația să informeze ANMDMR precum și operatorii economici, instituțiile sanitare și profesioniștii din domeniul sănătății cărora le furnizează un dispozitiv în mod direct cu privire la întreruperea sau încetarea anticipată a furnizării acestuia conform prevederilor din Regulamentul (UE) 2024/1860 al Parlamentului European și al Consiliului.
În acest scop a fost creată o pagină nouă în secțiunea Dispozitive medicale – Raportează o întrerupere sau o încetare în furnizarea dispozitivelor medicale sau a dispozitivelor medicale pentru diagnostic in vitro în care regăsiți toate informațiile necesare și actualizate. - Anunț important
26.11.2024
În atenția persoanelor interesate
Vă informăm că în data de 21.11.2024, Comisia Europeană a publicat ghidul Implementarea treptată a EUDAMED – Întrebări și Răspunsuri privind aspectele practice ale implementării treptate a EUDAMED – Gradual roll out of EUDAMED – Q&As on practical aspects related to the implementation of Regulation (EU) 2024/1860 (November 2024). Documentul poate fi descărcat accesând linkul:
https://health.ec.europa.eu/latest-updates/gradual-roll-out-eudamed-qas-practical-aspects-related-implementation-regulation-eu-20241860-2024-11-21_en
Ghidul conține 22 de întrebări și răspunsuri care clarifică termeni și aspecte ale implementării treptate a EUDAMED și este destinat facilitării aplicării prevederilor Regulamentului amintit în ceea ce privește implementarea treptată a bazei de date EUDAMED, a modului în care modulele devenite funcționale ale EUDAMED vor deveni obligatoriu de utilizat, de îndată ce sunt declarate funcționale în loc să se aștepte ca toate modulele să devină disponibile și să fie declarate funcționale, precum și utilizarea celor care sunt deja disponibile pentru utilizare voluntară.
În acest moment sunt deja disponibile pentru utlizare voluntară primele 3 din cele 6 module ale EUDAMED (înregistrarea Actorilor; UDI și înregistrarea dispozitivelor; Organisme Notificate (Notified Bodies) și certificate). Comisia Europeană pregătește alte 2 module (vigilență și supraveghere după introducerea pe piață; supravegherea pieței) acestea urmând să fie finalizate în 2024; se anticipează ca ulterior, toate aceste 5 module să fie declarate funcționale la jumătatea anului 2025. Se prevede ca modulul rămas, ultimul din totalul de 6 module ale EUDAMED, care acoperă investigațiile clinice / studiile de performanță să devină funcțional după trimestrul 3 al anului 2026.
Termenele anticipate la care modulele EUDAMED vor fi declarate funcționale se găsesc în diagrama disponibilă la:
https://health.ec.europa.eu/document/download/04ce2012-97df-4dd0-8a39-d4f6993b9e16_en?filename=md_eudamed_roadmap_en.pdf
Conform prevederilor perioadei de tranziție stabilite prin Regulamentul (EU) 2024/1860 de modificarea regulamentelor referitoare la dispozitivele medicale și cele de diagnostic in vitro, utilizarea fiecăruia dintre modulele EUDAMED va deveni obligatorie la 6 luni după ce fiecare dintre acestea vor fi declarate funcționale prin publicarea unei note de către Comisie în Jurnalul Oficial al Uniunii Europene, ca urmare a rezultatului pozitiv al unui audit independent în ceea ce privește funcționalitatea și îndeplinirea specificațiilor de către respectivul modul.
Mai multe informații despre EUDAMED sunt disponibile la
https://webgate.ec.europa.eu/eudamed/landing-page#/
https://webgate.ec.europa.eu/eudamed-help/en/welcome-to-the-eudamed-information-centre.html - Anunț important
12.11.2024
În atenția operatorilor economici avizați de Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România care desfășoară activități în domeniul dispozitivelor medicale
În conformitate cu OMS nr. 566/2020 pentru aprobarea Normelor metodologice de aplicare a Titlului XX din Legea nr. 95/2006 privind reforma în domeniul sănătății, activitățile de comercializare și de prestări servicii în domeniul dispozitivelor medicale supuse controlului prin avizare sunt următoarele:
a) import dispozitive medicale;
b) distribuție dispozitive medicale;
c) instalare și/sau mentenanță dispozitive medicale.
Avizul de funcționare emis în conformitate cu OMS nr. 566/2020 este valabil pe o perioadă de 3 ani de la data emiterii, dacă se mențin neschimbate condițiile care au stat la baza avizării. Valabilitatea acestui aviz încetează la data emiterii noului aviz de funcționare. - Anunț important
01.11.2024
În atenția producătorilor și tuturor părților interesate
Vă informăm că în data de 30.10.2024, Comisia Europeană a publicat Ghidul de Întrebări și Răspunsuri privind aspectele practice legate de implementarea obligațiilor de informare referitoare la întreruperea sau încetarea furnizării anumitor dispozitive prevăzute la articolul 10a din MDR și IVDR, astfel cum a fost introdus prin Regulamentul (UE) 2024/1860 din 13 iunie 2024 de modificare a Regulamentelor (UE) 2017/745 și (UE) 2017/746 în ceea ce privește introducerea treptată a Eudamed, obligația de informare în cazul întreruperii sau al încetării furnizării și dispozițiile tranzitorii pentru anumite dispozitive medicale pentru diagnostic in vitro.
Documentul poate fi descărcat accesând linkul:
https://health.ec.europa.eu/document/download/b431b10f-8512-4f47-9191-e1b84b2f9a27_en?filename=mdr_qna-article10a_mdr-ivdr_en.pdf
descarca documentul…
- Anunț important
24.10.2024
În atenția utilizatorilor profesioniști de dispozitive medicale
Vă informăm că începând cu data de 24.10.2024, intră în vigoare prevederile art.933 alin.(1)lit. l) din Legea 95/2006 și anume:
Art. 933 – (1) În vederea asigurării nivelului de securitate şi performanţă adecvat scopului pentru care sunt realizate dispozitivele medicale şi a evitării generării de incidente, utilizatorii au obligaţia:
k) de a se asigura că utilizează doar dispozitive medicale în situaţia în care în cadrul activităţilor profesionale folosesc echipamente în scop de diagnosticare, prevenire, monitorizare,prevedere, prognozare, tratament sau ameliorarea unei boli, astfel cum sunt definite la art. 2 pct. 1 prima liniuţă din Regulamentul (UE) 2017/745;
l)*) să se conformeze prevederilor lit. k) pentru dispozitivele medicale puse în funcţiune şi aflate în utilizare anterior intrării în vigoare a termenului prevăzut la art. V alin. (3) din Ordonanţa Guvernului nr. 37/2022 pentru modificarea şi completarea Legii nr. 95/2006
privind reforma în domeniul sănătăţii şi a Legii nr. 227/2015 privind Codul fiscal, precum şi stabilirea unor alte măsuri în domeniul sănătăţii, aprobată cu modificări şi completări prin Legea nr. 328/2022.
_____________
*) Prevederile lit. l), introduse prin O.U.G. nr. 88/2023, intră în vigoare la data de 24 octombrie 2024 (a se vedea art. IX alin. (1) lit. c) din O.U.G. nr. 88/2023)ANMDMR, ca autoritate competentă în domeniul dispozitivelor medicale, supraveghează și controlează dacă sunt respectate cerințele reglementărilor legale prin controale tematice. Aceste controale se vor desfășura atât la operatorii economici care importă, comercializează / distribuie și prestează activități în domeniul dispozitivelor medicale cât și la utilizatorii profesioniști care le utilizează.
Astfel, în cadrul controalelor ce vor fi efectuate de către ANMDMR la utilizatorii profesioniști de dispozitive medicale, se va verifica dacă în cadrul activității profesionale de diagnosticare, prevenire, monitorizare, prevedere, prognozare, tratament sau ameliorarea unei boli sunt folosite doar dispozitive medicale. - Anunț important
18.10.2024
În atenția persoanelor interesate
Începând cu 21.10.2024, activitatea de înregistrare și eliberare a documentelor, inclusiv pentru Direcția Generală a Dispozitivelor Medicale, se va desfășura doar la sediul Agenției Naționale a Medicamentelor și a Dispozitivelor Medicale din România din Str. Aviator Sănătescu 48, Sector 1, București.Program cu publicul:
LUNI – JOI : 9:00 – 15:00
VINERI – 9:00 – 13:00 - Anunț important
13.08.2024
În atenția utilizatorilor profesionali care lucrează sau sunt angajați în unități sanitare
Comisia Europeană are în vedere în prezent posibilitatea de a permite utilizarea instrucțiunilor electronice de utilizare(eIFU) pentru toate dispozitivele de uz profesional (cele care sunt utilizate de profesioniștii din domeniul sănătății). În acest sens a inițiat un sondaj referitor la utilizarea eIFU pentru dispozitivele medicale, care sunt, în mod special, utilizate de cadre medicale și alți utilizatori profesionali care lucrează sau sunt angajate într-o instituție sanitară din Uniunea Europeană. Termenul până la care puteți accesa chestionarul este 11 octombrie 2024.
Vă rugăm accesați:
pagina sondajului https://ec.europa.eu/eusurvey/runner/Survey_eIFUs_medicaldevices_2024
și chestionarul în limba română
https://ec.europa.eu/eusurvey/runner/Survey_eIFUs_medicaldevices_2024?surveylanguage=RO - Anunț important
17.07.2024
În atenția persoanelor interesate
Anunț privind cursurile de formare profesională și instruire pentru personalul cu atribuții specifice de instalare și/sau mentenanță dispozitive medicale
Potrivit prevederilor Ordinul nr. 566/2020 pentru aprobarea Normelor metodologice de aplicare a titlului XX din Legea nr. 95/2006 privind reforma în domeniul sănătății, referitoare la avizarea activităților în domeniul dispozitivelor medicale, cursurile de formare profesională și instruire pot fi susținute de personal tehnic instruit:
a) al unui producător/reprezentant al unui producător;
b) din cadrul asociațiilor profesionale în domeniul dispozitivelor medicale;
c) al operatorilor economici avizați de către ANMDMR, în cazul în care aceștia au în obiectul de activitate desfășurarea cursurilor de instruire.
descarca documentul…
- Anunț important
10.07.2024
În atenția tuturor părților interesate
Vă informăm că în data de 09 iulie 2024, Comisia Europeană a publicat REGULAMENTUL (UE) 2024/1860 AL PARLAMENTULUI EUROPEAN ȘI AL CONSILIULUI din 13 iunie 2024 de modificare a Regulamentelor (UE) 2017/745 și (UE) 2017/746 în ceea ce privește introducerea treptată a Eudamed, obligația de informare în cazul întreruperii sau al încetării furnizării și dispozițiile tranzitorii pentru anumite dispozitive medicale pentru diagnostic in vitro (IVD-uri).
Regulamentul prevede accelerarea lansării și utilizării obligatorii a Eudamed pentru modulele care sunt deja disponibile și funcționează corect începând cu sfârșitul anului 2025 – îmbunătățind astfel transparența, oferind informații la zi despre dispozitivele aflate pe piața UE și contribuind la monitorizarea disponibilității dispozitivelor.
De asemenea, se introduce obligația pentru producători de a notifica în prealabil autoritățile, operatorii economici și/sau instituțiile de sănătate în caz de întreruperi în furnizarea de IVD-uri sau dispozitive medicale care ar crea un risc pentru pacienți înainte de a înceta, temporar sau definitiv, furnizarea unui dispozitiv vital.
Noile perioade de tranziție propuse vor depinde de tipul de dispozitiv, în special de clasa sa de risc, stabilită conform Regulamentului (UE) 2017/746 (IVDR):
– perioadă de tranziție mai scurtă pentru IVD-uri cu risc ridicat, de clasă D (31 decembrie 2027)
– perioade mai lungi pentru IVD-uri cu risc mediu și scăzut, din clasele C și B (31 decembrie 2028 și 31 decembrie 2029 respectiv).
– în secțiunea Directive și regulamente – Dispozitive medicale, Regulamentul propriu-zis (fisierul “REGULAMENTUL (UE) 2024_1860 AL PARLAMENTULUI EUROPEAN ȘI AL CONSILIULUI_RO_TXT.pdf”).
descarcă regulamentul…
descarcă Ghid de Întrebări & Răspunsuri privind aspecte practice legate de punerea în aplicare a Regulamentului (UE) 2024_1860 …
descarcă Ghid de Întrebări si Răspunsuri privind aspecte practice legate de punerea în aplicare a Regulamentului (UE) 2024_745_rev.2…
- Anunț important
22.04.2024
În atenția persoanelor interesate
Lista furnizorilor de instruire având ca tematică legislația în domeniul dispozitivelor medicale, agreați de ANMDMR
Conform Normelor, pentru obținerea avizului de funcționare, operatorul economic trebuie să dispună de personal suficient și calificat/instruit pentru activitatea pe care o desfășoară/domeniul în care activează.
Persoana responsabilă de conformitatea cu reglementările (PRCR) specifice domeniului dispozitivelor medicale și șeful de depozit trebuie să facă dovada participării la cursuri de instruire având ca tematică legislația în domeniul dispozitivelor medicale.
descarca documentul…
- Anunț important
15.04.2024
În atenția tuturor părților interesate (unități sanitare, importatori / distribuitori, pacienți)
Începând din luna aprilie 2024 a fost creată pe site-ul ANMDMR o nouă secțiune COMUNICĂRI PRIVIND SIGURANȚA, în care vor fi postate, la începutul fiecărei luni, notificările în materie de siguranță în teren (Field Safety Notice – FSN) primite de ANMDMR în luna precedentă.
Vă aducem la cunoștință că prima postare pe site cuprinde doar Sumarul notificărilor în materie de siguranță în teren aferent perioadei 18-29.03.2024, urmând ca, începând din luna mai, să fie postate toate notificările primite de ANMDMR în decursul unei luni.
Dacă ați intrat în posesia unui dispozitiv afectat de o problemă privind siguranța, citiți cu atenție notificarea aferentă privind siguranța în teren și urmați instrucțiunile producătorului cuprinse în aceasta. Pentru întrebări legate de instrucțiunile producătorului, vă rugăm să contactați direct emitentul notificării în materie de siguranță în teren. - Anunț important
09.04.2024
În atenția persoanelor interesate
Anunț privind cursurile de formare profesională și instruire pentru personalul cu atribuții specifice de instalare și/sau mentenanță dispozitive medicale
descarca documentul…
- Anunț important
08.03.2024
În atenția operatorilor economici – persoane impozabile stabilite în România
În contextul implementării cu caracter obligatoriu a sistemului RO e-Factura de la 1 ianuarie 2024, conform prevederilor art. LIX, alin. (1) din Legea 296/2023, toate facturile emise de către ANMDMR reprezentând tarife prevăzute în Ordinul 888/2014, respectiv în Ordinul 3467/2022, vor fi transmise numai prin sistemul RO e-Factura, indiferent dacă destinatarii sunt sau nu înregistrați în Registrul RO e-Factura. - Anunț important
04.03.2024
În atenția operatorilor economici care solicită emiterea sau reînnoirea avizului de funcționare
În această secțiune, Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România (ANMDMR) vă pune la dispoziție platforma digitală din cadrul proiectului „Serviciul de eliberare avize de funcționare / reînnoire avize de funcționare”. Pentru accesul în platformă operatorii economici își vor crea contul de utilizator la adresa: https://avizaredm.anmdm.ro/login și vor urma instrucțiunile din manualul de utilizare pe care îl puteți descărca aici. Întregul proces de avizare se va desfășura online prin platforma digitală, operatorii economici având la finalizarea solicitării acces la avizul de funcționare emis sau reînnoit.
Încurajăm toți operatorii economici care prestează activități în domeniul dispozitivelor medicale să își creeze contul de utilizator pentru transmiterea cererilor de eliberare şi reînnoire aviz de funcţionare
descarcă manualul de utilizare …
- Anunț important
06.02.2024
În atenția tuturor operatorilor economici
Vă aducem la cunoștință faptul că începând cu luna ianuarie 2024 tarifele pentru activităţile desfăşurate de Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale din România în domeniul dispozitivelor medicale au fost indexate cu rata medie a inflaţiei din anul 2023 și se regăsesc în Anexa 1 atașată acestui anunț.
descarcă documentul…
- Anunț important
29.01.2024
În atenția tuturor părților interesate
Vă informăm că în data de 23 ianuarie 2024, Comisia Europeană a publicat o propunere de rectificare a Regulamentului (UE) 2017/745, destinat dispozitivelor medicale (MDR) și a Regulamentului (UE) 2017/746, destinat dispozitivelor medicale pentru diagnostic in vitro (IVDR).
Propunerea are menirea:
– să asigure disponibilitatea dispozitivelor medicale pentru diagnostic in vitro, acordând mai mult timp producătorilor pentru a trece la noile reguli, sub rezerva anumitor condiții importante
– să sporească transparența și să protejeze îngrijirea pacienților prin accelerarea lansării unor părți ale bazei de date europene privind dispozitivele medicale – EUDAMED
– să ofere sistemelor de sănătate mai mult timp pentru a proteja îngrijirea pacienților, obligând producătorii să notifice în cazul întreruperii aprovizionării cu anumite dispozitive medicale și dispozitive medicale pentru diagnostic in vitro.
descarcă documentul…
- Anunț important
07.12.2023
În atenția producătorilor români de dispozitive medicale și dispozitive medicale pentru diagnostic in vitro și a reprezentanților autorizați
Vă informăm că în data de 01 decembrie 2023, Comisia Europeană a publicat un studiu de monitorizare a disponibilității dispozitivelor medicale pe piața UE. Chestionare pentru producătorii de MD și IVD și reprezentanții autorizați.
Anunțul poate fi regăsit/completat la pagina web a Comisiei Europene accesând următorul link:
https://ec.europa.eu/eusurvey/runner/MFandAR - Anunț important
24.10.2023
În atenția unităților sanitare și tuturor factorilor interesați
În urma sesizării primite de la MEDTRONIC România SRL, referitoare la prezentarea de către prezentarea de către firma DEYAN KRAFT MEDICAL SRL adresei ANMDMR nr.112327E/06.06.2023 în cadrul procedurilor de soluționare a unor contestații urmare a unor licitații pentru sisteme de monitorizare a glicemiei, în legătură cu aceste sisteme produse de MEDTRONIC MINIMED U.S., ANMDMR a desfășurat o verificare pentru clarificarea aspectelor referitoare la adecvarea utilizării acestor dispozitive medicale la pacienții copii diabetici cu vârste sub 14 ani.
Verificarea a vizat sistemele de monitorizare a glicemiei produse de MEDTRONIC MINIMED U.S. care includ senzorul Guardian (3), pe care MEDTRONIC România SRL le comercializează pe piața din România, în calitate de distribuitor autorizat al producătorului MEDTRONIC MINIMED.
Concluziile verificării au demonstrat că sistemele MEDTRONIC de monitorizare a glicemiei comercializate pe piața din România nu prezintă limite de vârstă, fiind adecvate utilizării și pentru copii sub 14 ani.
Astfel, față de punctul de vedere ANMDMR cu nr. 112327E/06.06.2023, facem următoarele precizări:
Punctul de vedere exprimat în adresa ANMDMR menționată se referă la documentul ”System user Guide” prezentat în format letric de DEYAN KRAFT MEDICAL S.R.L. împreună cu solicitarea, și care include aplicația Guardian Connect (iOS: CSS7200, Android™ , CSS7201), transmițătorul Guardian Connect transmitter (MMT- 7821L), senzorul Guardian Sensor (3) și accesoriile acestora.
Documentul prezentat este ver. 2018, valid în Statele Unite ale Americii și publicat pe site-ul oficial al producătorului MEDTRONIC MINIMED US pe pagina dedicată utilizatorilor din Statele Unite ( afișat automat la deschiderea paginii web, alte locații pot fi selectate pe butonul corespunzător).
Redăm link-ul:
https://www.medtronicdiabetes.com/sites/default/files/library/download-library/user-guides/guardian-connect-v3_2/us-manual.pdf
Manualul ”System user Guide”:
– este destinat utilizării sistemului ca ansamblu, sistemul incluzând cele 3 componente principale: aplicatia, transmițătorul și senzorul , precum și accesoriile acestora;
– nu poartă marcajul CE, aplicabil în spațiul european;
– manualul de utilizare respectă cerințele legale din Statele Unite ale Americii și, ca urmare, include limite de vârstă precizate la pagina 2.
În Spațiul Economic European , MEDTRONIC MINIMED comercializează aceste sisteme, conform legislației europene în vigoare la momentul introducerii pe piață, respectiv Directiva 93/42/EEC.
Acest dispozitiv a fost supus procedurilor de evaluare a conformității corespunzătoare clasei dispozitivului, cu implicarea organismului notificat GMED Franța.
Ca urmare a certificatului emis de GMED, producătorul a emis declarația de conformitate și a aplicat marcajul CE. Acest marcaj se regăsește și pe ultima pagină a manualului de utilizare alături de numărul de identificare al organismului notificat (CE 0459). De asemenea este indicat reprezentantul autorizat în Uniunea Europeană, și anume MEDTRONIC B.V. Olanda.
Pe piața europeană, inclusiv în România, sistemul este comercializat cu 3 manuale, pentru componentele principale, și anume.
GuardianTM Connect – User Guide, cu varianta în limba română GuardianTM Connect – Ghid de utilizare (pentru transmițător);
GuardianTM Sensor (3) – Ghidul utilizatorului (în mai multe limbi, inclusiv lb. Engleză și lb. Română) (pentru senzor).
GuardianTM Connect – Ghid de utilizare a aplicației (pentru aplicație).
Aceste manuale nu indică limite de vârsta în utilizare pentru componentele sistemului de monitorizare a glicemiei.
Redăm mai jos link-urile pentru manualele de utilizare, publicate pe site-ul MEDTRONIC România:
https://resources.cloud.medtronic-diabetes.com/sites/prd/files/documents/2022-03/manual-guardian-connect-lock-out1.pdf
https://resources.cloud.medtronic-diabetes.com/sites/prd/files/documents/2022-03/guardian-sensor-3-ifu.pdf
https://resources.cloud.medtronic-diabetes.com/sites/prd/files/documents/2022-03/guardian-connect-aplicatie-32-lot-1.pdf - Anunț important
16.10.2023
În atenția persoanelor interesate
Anunț privind cursurile de formare profesională și instruire pentru personalul cu atribuții specifice de instalare și/sau mentenanță dispozitive medicale
descarca documentul…
- Anunț important
06.10.2023
În atenția producătorilor, reprezentanților autorizați, operatorilor economici și a tuturor părților interesate
Vă informăm că în data de 27 septembrie 2023, Comisia Europeană a publicat noua versiune a documentului Manual on borderline and classification for medical devices under Regulation (EU) 2017/745 on medical devices and Regulation (EU) 2017/746 on in vitro diagnostic medical devices.
Au fost introduse noutăți precum adezivi endovasculari, senzori, soluții de irigare, implanturi personalizate și multe altele.
Anunțul Comisiei Europene poate fi accesat la: https://health.ec.europa.eu/latest-updates/manual-borderline-and-classification-community-regulatory-framework-medical-devices-september-2023-2023-09-27_en
descarca documentul…
- Anunț important
04.10.2023
În atenția producătorilor, reprezentanților autorizați, operatorilor economici și a tuturor părților interesate
Vă informăm că în data de 26 septembrie 2023, Comisia Europeană a publicat documentul Întrebări și răspunsuri privind dispozițiile tranzitorii pentru produsele fără un scop medical vizat acoperite de anexa XVI a MDR.
Anunțul Comisiei Europene poate fi accesat la: https://health.ec.europa.eu/system/files/2023-09/md_new-reg_annex-xvi_q-n-a_transition-prov.pdf
descarca documentul…
- Anunț important
25.09.2023
În atenția tuturor părților interesate (importatori/distribuitori, utilizatori)
Ca urmare a unei sesizări primite și a verificărilor efectuate de ANMDMR, atragem atenția tuturor părților interesate că au fost depistate pe piața din România prezervative Durex falsificate, LOT 0010471127, care ar fi fabricate de producătorul Reckitt Benckiser Healthcare (UK) Limited, UK.
Potrivit producătorului, acest lot a fost fabricat o singură dată în 2011, cu data de expirare 2016-09, sub numele Durex Fetherlite, fiind livrat către Nigeria în ambalaje de câte 3 bucăți.
Atenționăm părțile interesate să nu importe / distribuie sau achiziționeze, în vederea punerii la dispoziție pe piața din România sau utilizării, prezervative LOT 0010471127, marca DUREX, indiferent de numele (modelul/tipul) acestora, dacă sunt în termen de valabilitate, acestea fiind dispozitive medicale falsificate.
În cazul în care aveți cunoștință de importatori / distribuitori care au comercializat pe teritoriul României astfel de prezervative falsificate sau în cazul în care ați intrat în posesia unor astfel de prezervative falsificate, sesizați Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România – Serviciul Supraveghere Piață, la adresa de email sesizaridm@anm.ro sau la celelalte date de contact existente pe site-ul ANMDMR. - Anunț important
28.08.2023
În atenția producătorilor, reprezentanților autorizați, operatorilor economici și a tuturor părților interesate
Vă informăm că în data de 23 august 2023, Comisia Europeană a publicat diagrama cu condițiile și termenele limită pentru introducerea pe piață a dispozitivelor „legacy” și a dispozitivelor implantabile la comandă de clasa III sau punerea lor în funcțiune în conformitate cu articolul 120 MDR, modificat prin Regulamentul 2023/607.
Diagrama este menită să ajute producătorii și alți actori relevanți să decidă dacă dispozitivul este acoperit de perioada de tranziție extinsă prevăzută la articolul 120 din Regulamentul (UE) 2017/745 privind dispozitivele medicale (MDR), modificat prin Regulamentul 2023/607.
Diagrama de flux ar trebui să determine eligibilitatea, condițiile și termenele limită pentru introducerea pe piață sau punerea în funcțiune a anumitor dispozitive în conformitate cu articolul 120 MDR.
Este recomandată de asemenea consultarea textulului din MDR, care are prioritate față de diagramă, și întrebările și răspunsurile privind aspectele practice legate de implementarea Regulamentului (UE) 2023/607.
Diagrama de flux este împărțită în două părți:
Partea 1: Dispozitive „legacy” menționate la articolul 120 alineatul (3a) din MDR, adică dispozitive acoperite de un certificat emis de un organism notificat în conformitate cu Directiva 90/385/CEE (AIMDD) sau Directiva 93/42/CEE (MDD) înainte de 26 mai 2021 și dispozitive „legacy” menționate la articolul 120 alineatul (3b) din MDR, adică dispozitive pentru care procedura de evaluare a conformității conform cu Directiva 93/42/CEE (MDD) nu a necesitat implicarea unui organism notificat, pentru care declarația de conformitate a fost întocmită înainte de 26 mai 2021 și pentru care procedura de evaluare a conformității conform MDR necesită implicarea un organism notificat.
Partea 2: dispozitive implantabile la comandă clasa III menționate la articolul 120 alineatul (3f) MDR.
Anunțul poate fi descărcat de pe pagina web a Comisiei Europene accesând următorul link:
https://health.ec.europa.eu/latest-updates/flowchart-assist-deciding-whether-or-not-device-covered-extended-mdr-transitional-period-2023-08-23_en
descarca documentul…
- Anunț important
21.08.2023
În atenția persoanelor interesate
Lista furnizorilor de instruire având ca tematică legislația în domeniul dispozitivelor medicale, agreați de ANMDMR
Conform Normelor, pentru obținerea avizului de funcționare, operatorul economic trebuie să dispună de personal suficient și calificat/instruit pentru activitatea pe care o desfășoară/domeniul în care activează.
Persoana responsabilă de conformitatea cu reglementările (PRCR) specifice domeniului dispozitivelor medicale și șeful de depozit trebuie să facă dovada participării la cursuri de instruire având ca tematică legislația în domeniul dispozitivelor medicale.
Art. 9, alin. (3) din Norme, prevede:
(3) Cursurile de instruire vor fi efectuate de către persoane fizice autorizate și persoane juridice care au în obiectul de activitate prestarea instruirilor prevăzute la alin. (2) lit. b) și care fac dovada experienței profesionale în activități de reglementare sau de evaluare a conformității dispozitivelor medicale astfel:
a) în activități de reglementare cu experiență profesională de cel puțin patru ani în domeniul dispozitivelor medicale sau participarea în cadrul grupurilor de lucru specifice domeniului dispozitivelor medicale la nivelul Comisiei Europene/Consiliului Uniunii Europene;
b) în activități de evaluare a conformității dispozitivelor medicale în cadrul unui organism de evaluare a conformității notificat pe directivele specifice dispozitivelor medicale, cel puțin doi ani.
De la apariția OMS 566/2020 până în prezent ANMDMR a luat legătura cu firmele care au emis diplome/certificate ca urmare a susținerii unor cursuri de instruire având ca tematică legislația în domeniul dispozitivelor medicale și pe care le-am regăsit în dosarele depuse de operatorii economici în vederea avizării activității desfășurate. În baza procedurii interne de lucru, așa cum este specificat la art. 7 din Norme, s-au solicitat dovezile îndeplinirii cerințelor art. 9, alin. (3) de către lectorii utilizați pentru susținerea acestor cursuri.
Până la această dată, firmele care au făcut dovada îndeplinirii acestor cerințe sunt următoarele:Nr. crt. Denumire persoană juridică Nume, prenume lector 1. MEDTECH CONSULTING SRL MARGARETA MIHALACHE 2. MEDICAL DEVICE LEX SRL LAZĂR IORDACHE
IOANA ȚENE3. MEDIA KOMPASS SRL NICOLAE FOTIN 4. CERTINSPECT REGISTER SRL GHEORGHE NEAGU 5. ASOCIAȚIA DE STANDARDIZARE DIN ROMÂNIA – ASRO MARGARETA MIHALACHE 6. EUROASIA SRL CHRISTIAN HEINRICH 7. OTD GLOBAL PRO SRL CHRISTIAN HEINRICH 8. POPI INVEST CORP SRL GHEORGHE NEAGU 9. MEDILEX TRAINING HUB SRL IOANA ȚENE În momentul în care lista va suporta modificări, vom publica deîndată revizuirea acesteia. În acest sens, vă rugăm să consultați în permanență site-ul ANMDMR pentru informații actualizate.
NOTĂ: ANMDMR monitorizează permanent activitatea prestatorilor de instruire. În acest sens, dacă sunteți nemulțumiți de prestația furnizorilor de instruire cu privire la modul de desfășurare al instruirii sau la calitatea serviciilor oferite, puteți sesiza aspectele negative la adresa da@anm.ro sau dgdm@anm.ro - Anunț important
09.08.2023
În atenția tuturor părților interesate
Anunț privind cursurile de formare profesională și instruire pentru personalul cu atribuții specifice de instalare și/sau mentenanță dispozitive medicale
descarca documentul…
- Anunț important
27.07.2023
În atenția tuturor părților interesate
Vă informăm că în data de 26.07.2023 a fost publicată ultima actualizare a Listei comune a testelor antigen COVID-19 a Uniunii Europene.
Puteți accesa această listă urmând linkul:
https://health.ec.europa.eu/system/files/2023-07/covid-19_eu-common-list-antigen-tests_en.pdf
În contextul pandemiei de COVID-19, Comitetul pentru Securitatea Sanitară (Health Security Committee (HSC) a înființat în mai 2021 un grup de lucru tehnic privind testele de diagnosticare COVID-19. Acest grup de lucru tehnic a reunit experți din cele 27 de țări ale Uniunii Europene și Norvegia, precum și reprezentanți ai Direcției Generale pentru Sănătate și Siguranță Alimentară (DG SANTE), Centrul Comun de Cercetare (JRC) și Centrul European pentru Prevenirea și Controlul Bolilor (ECDC).
Scopul Grupului de Lucru Tehnic (TWG) al HSC a fost să revizuiască propunerile prezentate de țările UE, precum și de producători, pentru ca dispozitivele să fie incluse în Lista comună a testelor antigen COVID-19 a Uniunii Europene.
În cazul în care grupul tehnic de lucru consideră că este necesară o actualizare a Listei comune la nivelul UE a testelor antigen pentru depistarea COVID-19, va fi prezentată o propunere Comitetului pentru Securitate Sanitară în vederea obținerii unui acord formal. Astfel de actualizări au vizat adăugări și/sau eliminări de teste antigen sau actualizări privind disponibilitatea datelor și informațiilor (de exemplu, publicarea de noi studii de validare). Alături de fiecare actualizare a listei comune a UE, a fost publicată o anexă, care stabilește detalii suplimentare și informații de bază cu privire la deciziile luate de grupul de lucru tehnic.
Această anexă poate fi accesată prin linkul:
https://health.ec.europa.eu/system/files/2023-07/covid-19_eu-common-list-antigen-tests_addendum_en.pdf - Anunț important
24.07.2023
În atenția producătorilor, reprezentanților autorizați, operatorilor economici și a tuturor părților interesate
Vă informăm că în data de 18 iulie 2023, Comisia Europeană a publicat Rev. 1 a ghidului cu privire la întrebări și răspunsuri privind aspectele practice legate de punerea în aplicare a Regulamentului (UE) 2023/607 de modificare a Regulamentelor (UE) 2017/745 și (UE) 2017/746 în ceea ce privește dispozițiile tranzitorii pentru anumite dispozitive medicale și dispozitive medicale de diagnostic in vitro.
Acest ghid de întrebări și răspunsuri are scopul de a facilita aplicarea Regulamentului (UE) 2023/607.
În cadrul Rev. 1 a ghidului au fost adăugate întrebări noi și au mai fost modificate/completate unele întrebări din ghidul publicat initial.
Anunțul poate fi descărcat de pe pagina web a Comisiei Europene accesând următorul link:
https://health.ec.europa.eu/system/files/2023-07/mdr_proposal_extension-q-n-a.pdf
descarca documentul…
- Anunț important
20.07.2023
În atenția persoanelor interesate
Lista furnizorilor de instruire având ca tematică legislația în domeniul dispozitivelor medicale, agreați de ANMDMR
Conform Normelor, pentru obținerea avizului de funcționare, operatorul economic trebuie să dispună de personal suficient și calificat/instruit pentru activitatea pe care o desfășoară/domeniul în care activează.
Persoana responsabilă de conformitatea cu reglementările (PRCR) specifice domeniului dispozitivelor medicale și șeful de depozit trebuie să facă dovada participării la cursuri de instruire având ca tematică legislația în domeniul dispozitivelor medicale.
Art. 9, alin. (3) din Norme, prevede:
(3) Cursurile de instruire vor fi efectuate de către persoane fizice autorizate și persoane juridice care au în obiectul de activitate prestarea instruirilor prevăzute la alin. (2) lit. b) și care fac dovada experienței profesionale în activități de reglementare sau de evaluare a conformității dispozitivelor medicale astfel:
a) în activități de reglementare cu experiență profesională de cel puțin patru ani în domeniul dispozitivelor medicale sau participarea în cadrul grupurilor de lucru specifice domeniului dispozitivelor medicale la nivelul Comisiei Europene/Consiliului Uniunii Europene;
b) în activități de evaluare a conformității dispozitivelor medicale în cadrul unui organism de evaluare a conformității notificat pe directivele specifice dispozitivelor medicale, cel puțin doi ani.
De la apariția OMS 566/2020 până în prezent ANMDMR a luat legătura cu firmele care au emis diplome/certificate ca urmare a susținerii unor cursuri de instruire având ca tematică legislația în domeniul dispozitivelor medicale și pe care le-am regăsit în dosarele depuse de operatorii economici în vederea avizării activității desfășurate. În baza procedurii interne de lucru, așa cum este specificat la art. 7 din Norme, s-au solicitat dovezile îndeplinirii cerințelor art. 9, alin. (3) de către lectorii utilizați pentru susținerea acestor cursuri.
Până la această dată, firmele care au făcut dovada îndeplinirii acestor cerințe sunt următoarele:Nr. crt. Denumire persoană juridică Nume, prenume lector 1. MEDTECH CONSULTING SRL MARGARETA MIHALACHE 2. MEDICAL DEVICE LEX SRL LAZĂR IORDACHE
MARGARETA MIHALACHE3. MEDIA KOMPASS SRL NICOLAE FOTIN 4. CERTINSPECT REGISTER SRL GHEORGHE NEAGU 5. ASOCIAȚIA DE STANDARDIZARE DIN ROMÂNIA – ASRO MARGARETA MIHALACHE 6. EUROASIA SRL CHRISTIAN HEINRICH 7. OTD GLOBAL PRO SRL CHRISTIAN HEINRICH 8. POPI INVEST CORP SRL GHEORGHE NEAGU În momentul în care lista va suporta modificări, vom publica deîndată revizuirea acesteia. În acest sens, vă rugăm să consultați în permanență site-ul ANMDMR pentru informații actualizate.
NOTĂ: ANMDMR monitorizează permanent activitatea prestatorilor de instruire. În acest sens, dacă sunteți nemulțumiți de prestația furnizorilor de instruire cu privire la modul de desfășurare al instruirii sau la calitatea serviciilor oferite, puteți sesiza aspectele negative la adresa da@anm.ro sau dgdm@anm.ro - Anunț important
22.06.2023
În atenția producătorilor, reprezentanților autorizați, operatorilor economici și a tuturor părților interesate
Vă informăm ca a fost publicat REGULAMENTUL DE PUNERE ÎN APLICARE (UE) 2023/1194 AL COMISIEI din 20 iunie 2023 de modificare a Regulamentului de punere în aplicare (UE) 2022/2346 în ceea ce privește dispozițiile tranzitorii privind anumite produse fără scop medical propus, menționate în Anexa XVI la Regulamentul (UE) 2017/745 al Parlamentului European și al Consiliului.
Regulamentul va fi aplicabil începând cu 22 iunie 2023 împreună cu Regulamentul de punere în aplicare (UE) 2022/2346 de stabilire a specificațiilor comune pentru produsele din Anexa XVI .
Ca o consecință a aplicabilității depline a Specificațiilor Comune, începând cu 22 iunie 2023, MDR va deveni aplicabil și produselor fără un scop medical propus care sunt enumerate în Anexa XVI la regulament.
Anunțul Comisiei Europene poate fi accesat la:
https://eur-lex.europa.eu/legal-content/RO/TXT/HTML/?uri=CELEX:32023R1194&qid=1687344268439 - Anunț important
19.05.2023
În atenția producătorilor, reprezentanților autorizați, operatorilor economici și a tuturor părților interesate
Vă informăm că în data de 12 mai 2023 Comisia Europeană a publicat revizia documentului MDCG 2020-3 cu îndrumări privind schimbările semnificative ale dispoziției tranzitorii de la articolul 120 din MDR referitoare la dispozitivele acoperite de certificate în conformitate cu MDD sau AIMDD.
Modificările aduse sunt următoarele:
În secțiunea 4.1 – Generalități:
• Modificare minoră a textului pentru a clarifica faptul că schimbările pentru a se conforma cu alte legislații ale Uniunii intră în domeniul de aplicare al ghidului numai dacă raportul risc/beneficiu al dispozitivului nu este afectat negativ.
• Modificarea minoră a textului și adăugarea unei note de subsol privind valabilitatea certificatelor în perioada de tranziție.
• Adăugarea unei note de subsol referitoare la declarațiile care listează modificări nesemnificative pentru dispozitivele de clasa I.
În secțiunea 4.2 – Modificări care nu privesc proiectarea sau scopul propus:
• Adăugarea unei note de subsol pentru a exclude schimbarea producătorului legal din primul exemplu.
• Adăugarea unei ultime propoziții referitoare la procedura de notificare convenită între producător și organismul notificat.
În secțiunea 4.3.2.3 – Modificări în proiectare:
• Text îmbunătățit în exemplele legate de modificările aduse carcasei dispozitivului și aspectul interfeței cu utilizatorul, pentru mai multă claritate.
• Includerea Notei (îngroșate) referitoare la raportul beneficiu/risc în fiecare subsecțiune, pentru o mai bună citire și înțelegere.
Anunțul Comisiei Europene poate fi accesat la: https://health.ec.europa.eu/latest-updates/update-mdcg-2020-3-rev1-guidance-significant-changes-regarding-transitional-provision-under-article-2023-05-12_en
descarca documentul…
- Anunț important
11.05.2023
În atenția producătorilor, reprezentanților autorizați, operatorilor economici și a tuturor părților interesate
Vă informăm că în data de 10 mai 2023, Comisia Europeană a publicat proiectul final al Regulamentului de punere în aplicare al Comisiei, de modificare a dispozițiilor tranzitorii stabilite în Regulamentul (UE) 2022/2346 de stabilire a specificațiilor comune pentru produsele fără un scop medical prevăzut, pe site-ul Comisiei și este deschis comentariilor până la data de 05.06.2023. Comentariile pot fi trimise Comisiei.
Acest proiect este propus din motive de coerență și pentru a oferi securitate juridică operatorilor economici prin alinierea prevederilor referitoare la perioadele de tranziție din Regulamentul de implementare R(EU) 2022/2346 pentru produsele care sunt acoperite de un certificat emis de un organism notificat conform Directivei 93/42/EEC cu cele din Regulamentul R(EU) 2017/745, așa cum au fost amendate de Regulamentul R(EU) 2023/607.
Anunțul Comisiei Europene poate fi accesat la: Amendment of common specifications for products without intended medical purpose listed in Ann. XVI – Reg. (EU) 2017/745 (europa.eu)
descarca documentul…
- Anunț important
31.03.2023
În atenția operatorilor economici care solicită avizarea activității de instalare și/sau mentenanță sisteme de distribuție gaze medicale
Ca urmare a apariției Ordinului nr. 2412 din 15.09.2022 pentru aprobarea reglementării tehnice „Normativ pentru construcții spitalicești, indicativ NP 015-2022” emis de Ministerul dezvoltării, lucrărilor publice și administrației și a numeroaselor solicitări de clarificări cu privire la prevederile acestui ordin, facem următoarele precizări.
descarca documentul…
- Anunț important
21.03.2023
În atenția producătorilor de dispozitive medicale și dispozitive medicale pentru diagnostic in vitro, reprezentanților autorizați, operatorilor economici și a tuturor părților interesate
Vă informăm că în data de 20 martie 2023, Comisia Europeană a publicat REGULAMENTUL (UE) 2023/607 AL PARLAMENTULUI EUROPEAN ȘI AL CONSILIULUI din 15 martie 2023 de modificare a Regulamentelor (UE) 2017/745 și (UE) 2017/746 în ceea ce privește dispozițiile tranzitorii pentru anumite dispozitive medicale și pentru anumite dispozitive medicale pentru diagnostic in vitro.
Prezentul regulament este adoptat ca urmare a unor circumstanțe excepționale generate de un risc iminent de penurie de dispozitive medicale și de riscul asociat de generare a unei crize de sănătate publică.
Dispozitiile tranzitorii pentru dispozitivele medicale
Certificatele eliberate de organismele notificate în conformitate cu directivele respective începând cu 25 mai 2017 care încă erau valabile la 26 mai 2021 și care au expirat înainte de 20 martie 2023 sunt considerate valabile până la datele prevăzute în tabelul de mai jos numai dacă este îndeplinită una dintre următoarele condiții:
(a) înainte de data expirării certificatului, producătorul și un organism notificat au semnat un acord scris pentru evaluarea conformității cu privire la dispozitivul care face obiectul certificatului expirat sau cu privire la un dispozitiv destinat să înlocuiască dispozitivul respectiv;
(b) o autoritate competentă a unui stat membru a acordat o derogare de la procedura aplicabilă de evaluare a conformității în conformitate cu articolul 59 alineatul (1) din Regulamentul 745/2017 sau a solicitat producătorului, în conformitate cu articolul 97 alineatul (1) din Regulamentul 745/2017, să efectueze procedura aplicabilă de evaluare a conformității.”;
Certificatele care încă erau valabile la 26 mai 2021 și care expiră după 20 martie 2023 sunt considerate valabile până la datele prevăzute în tabelul de mai jos dacă se va face dovada că cel târziu la 26 mai 2024, producătorul sau reprezentantul autorizat a depus la organismul notificat o cerere oficială în conformitate cu anexa VII secțiunea 4.3 primul paragraf pentru evaluarea conformității unui dispozitiv menționat la alineatul (3a) sau la alineatul (3b) din prezentul articol sau a unui dispozitiv destinat să înlocuiască dispozitivul respectiv și, cel târziu la 26 septembrie 2024, organismul notificat și producătorul au semnat un acord scris în conformitate cu anexa VII secțiunea 4.3 al doilea paragraf.
Dispozitivele medicale aflate în situația prezentată mai sus pot fi introduse pe piață sau puse în funcțiune până la următoarele date:Dispozitive clasa III și dispozitive implantabile clasa IIb, cu excepția materialelor de sutură, capselor, materialelor pentru plombe dentare, aparatelor dentare, coroanelor dentare, șuruburilor, penelor, firelor metalice pentru plăci, acelor, clemelor și a conectorilor; Dispozitive din clasa IIb, altele decât cele menționate anterior și dispozitive din clasa IIa și Is/Im; Dispozitive care se reclasifică în conformitate cu MDR. 31 Decembrie 2027 31 Decembrie 2028 31 Decembrie 2028 Dispozitivele medicale din clasa I puse în funcțiune în baza Directivei 93/42/EEC pentru care s-a emis declarația de conformitate înainte de 26.05.2021 și care se reclasifică în conformitate cu prevederile MDR pot fi introduse în continuare pe piață până la 31 Decembrie 2028 doar dacă sunt respectate condițiile menționate anterior.
Dispozitivele implantabile din clasa III fabricate la comandă pot fi introduse pe piață sau puse în funcțiune până la 26 mai 2026 fără un certificat eliberat de un organism notificat în conformitate cu procedura de evaluare a conformității doar dacă sunt respectate condițiile menționate anterior.
Dispozițiile tranzitorii pentru dispozitivele medicale pentru diagnostic in vitro
Regulamentul (UE) 2017/746 se modifică după cum urmează:
1. La articolul 110, alineatul (4) se înlocuiește cu următorul text:
„(4) Dispozitivele introduse pe piață în mod legal în temeiul Directivei 98/79/CE înainte de 26 mai 2022 și dispozitivele introduse pe piață în mod legal începând cu 26 mai 2022, în temeiul alineatului (3) din prezentul articol, pot fi în continuare puse la dispoziție pe piață sau puse în funcțiune.”
2. La articolul 112, al doilea paragraf se înlocuiește cu următorul text:
„În ceea ce privește dispozitivele menționate la articolul 110 alineatele (3) și (4) din prezentul regulament, Directiva 98/79/CE continuă să se aplice în măsura în care acest lucru este necesar pentru aplicarea alineatelor menționate.”
Anunțul Comisiei Europene poate fi regăsit accesând linkul următor: https://health.ec.europa.eu/medical-devices-sector/new-regulations_en#extension-of-the-transition-periods-provided-for-in-the-regulations
Comisia Europeană a pus la dispoziția părților interesate un ghid cu privire la Întrebări și răspunsuri privind aspectele practice legate de punerea în aplicare a Regulamentului (UE) 2023/607 de modificare a Regulamentelor (UE) 2017/745 și (UE) 2017/746 în ceea ce privește dispozițiile tranzitorii pentru anumite dispozitive medicale și dispozitive medicale de diagnostic in vitro care poate fi descărcat de pe pagina web a Comisiei Europene accesând următorul link:
https://health.ec.europa.eu/latest-updates/qa-practical-aspects-related-implementation-regulation-eu-2023607-extension-mdr-transitional-period-2023-03-28_en
descarca regulamentul…
descarca ghidul…
- Anunț important
14.03.2023
În atenția producătorilor,reprezentanților autorizați, operatorilor economici și a tuturor părților interesate
Vă informăm că în data de 08.03.2023, , Comisia Europeană a publicat REGULAMENTUL DELEGAT (UE) 2023/502 AL COMISIEI din 1 decembrie 2022 de modificare a Regulamentului (UE) 2017/745 al Parlamentului European și al Consiliului în ceea ce privește frecvența reevaluărilor complete ale organismelor notificate și REGULAMENTUL DELEGAT (UE) 2023/503 AL COMISIEI din 1 decembrie 2022 de modificare a Regulamentului (UE) 2017/746 al Parlamentului European și al Consiliului în ceea ce privește frecvența reevaluărilor complete ale organismelor notificate, prin care se modifică termenele de reevaluare a organismelor notificate de la 3 la 5 ani și stabilește frecvența reevaluărilor complete ulterioare a acestora la fiecare 5 ani.
Aceste regulamente le regăsiţi accesând linkul:
Directive si regulamente – Dispozitive medicale - Anunț important
28.02.2023
În atenția tuturor operatorilor economici
Vă aducem la cunoștință faptul că doar producătorii de dispozitive medicale din afara Uniunii Europene sunt obligați să desemneze un reprezentant autorizat unic pentru a introduce dispozitivul pe piața Uniunii.
Conform Regulamentului (UE) 2017/745 al Parlamentului European și al Consiliului din 5 aprilie 2017 privind dispozitivele medicale, „reprezentant autorizat” înseamnă orice persoană fizică sau juridică stabilită în Uniune, care a primit și a acceptat un mandat scris din partea unui producător din exteriorul Uniunii, pentru a acționa în numele producătorului în legătură cu sarcini specificate privind obligațiile acestuia din urmă care decurg din prezentul regulament.
În baza naţională de date a ANMDMR, doar reprezentanții autorizați cu sediul în România au obligația să se înregistreze atunci când introduc pe piaţă următoarele tipuri de dispozitive medicale:
a) dispozitive medicale din clasele I, IIa, IIb şi III, inclusiv cele sterile şi/sau cu funcţie de măsurare;
b) sisteme şi pachete de proceduri prevăzute la art. 22 din Regulament;
c) dispozitive medicale implantabile active.
Reprezentanții autorizați cu sediul în alte state membre ale Uniunii Europene NU SE ÎNREGISTREAZĂ în baza națională de date.
De asemenea, certificatul de liberă vânzare se emite pentru scop de export doar reprezentanților autorizați cu sediul în România. - Anunț important
15.02.2023
În atenția producătorilor,reprezentanților autorizați, operatorilor economici și a tuturor părților interesate
Vă informăm că din data de 13 februarie 2023 au intrat în vigoare Normele metodologice privind evaluarea clinică și investigațiile clinice prin publicarea în Monitorul Oficial al României, Partea I, Nr.120 bis/13.II.2023 a ORDINULUI Nr. 330 din 13 februarie 2023 privind evaluarea clinică și investigațiile clinice cu dispozitive medicale și pentru abrogarea Ordinului ministrului sănătății publice nr. 792/2006 privind desfășurarea procedurii de investigație clinică și a procedurii de evaluare a performanței pentru dispozitivele medicale.
Puteți accesa acest ordin în secțiunea Dispozitive medicale / Legislație – Dispozitive medicale/ Ordine de ministru / 2023. - Anunț important
14.02.2023
În atenția producătorilor, organismelor notificate, instituțiilor de sănătate și a tuturor părților interesate în domeniul dispozitivelor medicale pentru diagnostic in vitro
Vă informăm că în data de 10 februarie 2023, Comisia Europeană a publicat revizia a 2-a a ghidului MDCG 2020-16: Îndrumări privind regulile de clasificare ale dispozitivelor medicale pentru diagnostic in vitro sub Regulamentul (UE) 2017/746 destinat dispozitivelor medicale de diagnostic in vitro (IVDR).
Modificările aduse odată cu revizia a 2-a a ghidului se referă la modificări minore asupra exemplelor, adăugarea anexei 2 (diagramă ajutătoare la determinarea clasificării unui IVD ca CDx).
Acest ghid, referitor la aplicarea Regulamentului (UE) 2017/746 privind dispozitivele medicale de diagnostic in vitro (IVDR) abordează clasificarea dispozitivelor medicale de diagnostic (IVD) in vitro și oferă clarificări cu privire la regulile de clasificare prevăzute în anexa VIII.
Acest ghid de clasificare se aplică și pentru societățile ce oferă servicii informaționale sau de diagnostic efectuate pacienților din UE sau dispozitivelor puse în funcțiune prin vânzări la distanță.
Scopul principal al acestui document este de a oferi îndrumări producătorilor, organismelor notificate și instituțiilor de sănătate cu privire la modul de clasificare a unui IVD înainte de plasarea acestuia pe piață, punerea la dispoziție pe piață sau punerea în funcțiune în Uniune.
De asemenea, este destinat să informeze autoritățile de reglementare și alte părți interesate când evaluarea clasei atribuite unui IVD se face de către un producător sau de o instituție sanitară.
Prin urmare, și numai la cererea unui stat membru, sau din proprie inițiativă, Comisia, după consultarea Grupului de coordonare a dispozitivelor medicale (MDCG), decide, prin acte de punere în aplicare, cu privire la aplicarea anexei VIII unui anumit dispozitiv, sau categorie sau grup de dispozitive, în vederea stabilirii clasificării acestor dispozitive (articolul 47 (3-4) din IVDR).
Anunțul Comisiei Europene poate fi accesat la: https://health.ec.europa.eu/latest-updates/update-mdcg-2020-16-rev2-guidance-classification-rules-vitro-diagnostic-medical-devices-under-2023-02-10_en
descarca documentul…
- Anunț important
13.01.2023
În atenția profesioniștilor din domeniul sănătății și cercetătorilor instituțiilor de sănătate care își propun proiectarea, fabricarea, modificarea și utilizarea dispozitivelor in-house și a tuturor părților interesate în domeniul dispozitivelor medicale
Vă informăm că în data de 10 ianuarie 2023, Comisia Europeană a publicat ghidul MDCG 2023-1: Îndrumări privind derogările instituțiilor sanitare în temeiul articolului 5 alineatul (5) din Regulamentul (UE) 2017/745 destinat dispozitivelor medicale (MDR) și Regulamentul (UE) 2017/746 destinat dispozitivelor medicale de diagnostic in vitro (IVDR).
Dispozitivele medicale pot fi fabricate și utilizate în cadrul instituțiilor sanitare din UE (in-house devices), la scară neindustrială, pentru a răspunde nevoilor specifice ale unor grupuri țintă de pacienți care nu pot fi îndeplinite sau nu pot fi îndeplinite la nivelul corespunzător de performanță, de către un dispozitiv echivalent cu marcaj CE disponibil pe piață.
Dispozitivele medicale fabricate și utilizate numai în cadrul instituțiilor sanitare (in-house) sunt exceptate de la majoritatea prevederilor Regulamentului (UE) 2017/745 destinat dispozitivelor medicale (MDR) și Regulamentului (UE) 2017/746 destinat dispozitivelor medicale de diagnostic in vitro (IVDR), cu condiția ca instituția sanitară să respecte condițiile prevăzute la articolul 5 alineatul (5) din Regulament.
Pentru a asigura cel mai înalt nivel de protecție a sănătății, articolul 5 alineatul (5) stabilește un număr de reguli privind fabricarea și utilizarea unor astfel de dispozitive medicale in-house.
Prevederile articolului 5 alineatul (5) stau la baza controlului reglementar și a supravegherii dispozitivelor in-house. Acest document oferă îndrumări cu privire la aplicarea unora dintre aceste reguli.
În plus, acest document de orientare intenționează să încurajeze aplicarea armonizată a articolului 5 alineatul (5) de către autoritățile naționale competente.
Ambele Regulamente mai precizează că orice persoană fizică sau juridică ce oferă servicii de diagnostic sau terapeutice prin vânzări la distanță către pacienți din Uniune trebuie să utilizeze dispozitive care respectă MDR sau IVDR (articolul 6 alineatul (2)). Este important aici faptul că prevederea de derogare de la Articolul 5 alineatul (5) se aplică numai instituțiilor sanitare din Uniune.
În timp ce majoritatea recomandărilor din acest document se referă atât la dispozitivele medicale, cât și la dispozitive medicale de diagnostic in vitro (IVD), unele sunt specifice IVD-urilor; astfel de cazuri sunt în mod explicit menționate.
Regulamentul (UE) 2022/112 a amânat aplicarea unora, dar nu a tuturor prevederilor pentru IVD in-house. O prezentare schematică a momentului de aplicare a prevederilor articolului 5 alineatul (5) IVDR pot fi găsite în anexa B a prezentului ghid.
De reținut că articolul 5 alineatul (5) corespunzător din MDR este deja pe deplin aplicabil din 26 mai 2021.
Anunțul Comisiei Europene poate fi accesat la: https://health.ec.europa.eu/system/files/2023-01/mdcg_2023-1_en.pdf
descarca documentul…
- Anunț important
23.12.2022
În atenția producătorilor,reprezentanților autorizați, operatorilor economici și a tuturor părților interesate
Vă informăm că în data de 09 decembrie 2022, Comisia Europeană a publicat ghidul MDCG 2022-18 în vederea aplicării articolului 97 MDR pentru legacy devices pentru care MDD sau certificatul AIMDD expiră înaintea eliberării unui certificat MDR.
„Legacy devices” sunt definite ca dispozitive medicale, dispozitive medicale implantabile active și dispozitive medicale pentru diagnostic in vitro care sunt acoperite de un certificat de conformitate CE valabil emis în conformitate cu Directiva 93/42/CEE, Directiva 90/385/CEE sau Directiva 98/79/CE și care continuă să fie introduse pe piață după data aplicării Regulamentului (UE) 2017/745 (MDR) sau Regulamentului 2017/746 (IVDR).
Conform art. 94 din MDR, dacă evaluarea autorităților competente din statele membre a unor dispozitive medicale, motivată fie de posibilitatea prezentării unui risc inacceptabil pentru sănătatea sau siguranța pacienților, utilizatorilor sau altor persoane, sau care pot afecta sănătatea publică fie de nerespectarea altei cerințe ale MDR are ca rezultat constatarea neconformității dispozitivului medical cu anumite cerințe ale MDR (în cazul de față lipsa certificatului CE valabil) dar nedemonstrarea unor riscuri neacceptabile pentru sănătatea sau siguranța pacienților, utilizatorilor sau altor persoane, sau care pot afecta sănătatea publică, se poate aplica art. 97 din MDR.
Ghidul MDCG 2022-18 propune abordarea comună și uniformă în aplicarea articolului 97 din Regulamentul (UE) 2017/745 privind dispozitivele medicale (MDR) în situațiile în care un dispozitiv nu este în conformitate cu MDR deoarece are un certificat eliberat în conformitate cu Directiva 93/42/CEE (MDD) sau Directiva 90/385/CEE (AIMDD) ce a expirat sau expiră înainte de eliberarea certificatelor necesare în conformitate cu MDR.
Utilizarea articolului 97 MDR în aceste situații este menită să fie doar o soluție temporară. Va contribui la evitarea întreruperii aprovizionării cu dispozitive pe piața UE, necesare sistemelor de sănătate și pacienților.
Se aplică numai dispozitivelor care sunt „în tranziție” de la MDD sau AIMDD la MDR sau pentru care, în ciuda eforturilor rezonabile întreprinse de producător pentru a obține certificarea conform MDR, procedura relevantă de evaluare a conformității care implică un organism notificat nu a fost încheiată la timp.
Nu se aplică dispozitivelor pentru care certificatul eliberat sub MDD sau AIMDD a fost suspendat sau retras de către organismul notificat; cu alte cuvinte, certificatul întocmit pe directivă trebuie să fi fost valid la data expirării sale.
Anunțul Comisiei Europene poate fi accesat la: https://health.ec.europa.eu/latest-updates/mdcg-position-paper-application-art97-mdr-legacy-devices-which-mddaimdd-certificate-expires-issuance-2022-12-09_en
descarca documentul…
- Anunț important
13.12.2022
În atenția producătorilor, reprezentanților autorizați, operatorilor economici și a tuturor părților interesate
Vă informăm că a fost publicat în Monitorul Oficial Nr. 1180 din 9 decembrie 2022 Ordinul Nr. 3539 din 24 noiembrie pentru aprobarea Normelor metodologice privind introducerea pe piaţă a dispozitivelor medicale și înregistrarea operatorilor economici în Baza europeana de date referitoare la dispozitivele medicale (Eudamed), precum și în baza națională de date și de derogare de la procedurile de evaluare a conformităţii.
Acest ordin poate fi regăsit și în secțiunea Legislație – Dispozitive medicale – Ordine de ministru.
Formularele de solicitare se pot descărca din secțiunea Formulare si tarife – Dispozitive medicale. - Anunț important
12.12.2022
În atenția producătorilor de dispozitive medicale și dispozitive medicale pentru diagnostic in vitro și a tuturor părților interesate
Vă informăm că în data de 6 decembrie 2022, Comisia Europeană a publicat documentul MDCG 2022-17: Poziția Grupului de coordonare pentru dispozitive medicale cu privire la auditurile hibride.
Această lucrare prezintă poziția Grupului de coordonare a dispozitivelor medicale (MDCG) cu privire la posibila utilizare a auditurilor hibride de către organismele notificate în temeiul Regulamentului (UE) 2017/745 privind dispozitivele medicale (MDR) și al Regulamentului (UE) 2017/746 privind dispozitivele medicale de diagnostic in vitro (IVDR).
Documentul are ca scop oferirea unei definiții pentru auditurile hibride și clarificări cu privire la modul în care auditurile hibride pot fi utilizate în cadrul MDR și IVDR, așa cum s-a recomandat în urma publicării MDCG 2022-143. Anumite proceduri de evaluare a conformității conform MDR și IVDR impun organismului notificat să efectueze audituri ale sistemului de management al calității (SMC) al producătorului.
Procedura de evaluare trebuie să includă un audit la sediul producătorului atât pentru evaluarea inițială, cât și pentru supravegherea periodică. Aceeași cerință se aplică, după caz, pentru auditurile care au loc la sediul furnizorilor și/sau subcontractanților producătorului. Pe lângă termenii „sediu” sau „în incintă”, în MDR și IVDR sunt folosiți și „la fața locului” și „în afara amplasamentului” pentru a descrie locul în care au loc activitățile de evaluare a conformității.
Pentru a clarifica semnificația termenului „audit hibrid”, MDCG este de acord cu următoarea definiție:
Un „audit hibrid” ar trebui înțeles ca un audit la sediul producătorului sau furnizorilor și/sau subcontractanții săi cu cel puțin un auditor prezent la sediu și alți membri ai echipei de audit care participă din altă parte, folosind tehnologiile informației și comunicațiilor (TIC).
Anunțul Comisiei Europene poate fi accesat la: https://health.ec.europa.eu/latest-updates/mdcg-2022-17-mdcg-position-paper-hybrid-audits-december-2022-2022-12-06_en
descarca documentul…
- Anunț important
06.12.2022
În atenția producătorilor, reprezentanților autorizați, operatorilor economici și a tuturor părților interesate
Vă informăm că în data de 1 decembrie 2022, Regulamentele de implementare ale Comisiei Europene cu privire la stabilirea specificațiilor comune pentru grupurile de produse fără un scop medical prevăzut enumerate în anexa XVI la Regulamentul (UE) 2017/745 și normele de aplicare a Regulamentului (UE) 2017/745 în ceea ce privește reclasificarea grupurilor de anumite produsele active fără un scop medical prevăzut au fost publicate în Jurnalul Oficial.
Regulamentul (UE) 2017/745 stabilește norme privind introducerea pe piață, punerea la dispoziție pe piață sau punerea în funcțiune a dispozitivelor medicale de uz uman și a accesoriilor pentru astfel de dispozitive în Uniune. Regulamentul (UE) 2017/745 impune, de asemenea, Comisiei să adopte, pentru grupurile de produse fără un scop medical prevăzut, enumerate în anexa sa XVI, specificații comune care să abordeze cel puțin aplicarea managementului riscurilor, astfel cum este prevăzut în cerințele generale de siguranță și performanță stabilite. prevăzute în anexa I la regulamentul respectiv și, dacă este necesar, evaluarea clinică a siguranței.
Regulile de clasificare 9 și 10 privind dispozitivele active din secțiunile 6.1. și 6.2. din anexa VIII la Regulamentul (UE) 2017/745 se referă la un scop medical prevăzut, respectiv pentru terapie și diagnostic și, prin urmare, nu poate fi aplicat produselor active fără un scop medical prevăzut, menționat la articolul 1 alineatul (2) din regulamentul respectiv. Prin urmare, astfel de produse trebuie să fie clasificate în clasa I în conformitate cu regula 13 din secțiunea 6.5. din anexa VIII la Regulamentul (UE) 2017/745.
Anunțul Comisiei Europene poate fi accesat la: EUR-Lex – 32022R2346 – EN – EUR-Lex (europa.eu) și EUR-Lex – 32022R2347 – EN – EUR-Lex (europa.eu).
descarca documentul…
descarca documentul…
- Anunț important
06.12.2022
În atenția laboratoarelor pentru diagnostic in vitro și a tuturor părților interesate
Vă informăm că în data de 30 noiembrie 2022, Comisia Europeană a publicat un pachet informativ cu informații destinate candidaților la desemnarea laboratoarelor de referință EU.
Acest pachet de informații își propune să sintetizeze informațiile cheie într-un mod accesibil, poate suferi modificări. Vă rugăm să consultați legislația relevantă și textul apelului de candidaturi pentru detalii complete și/sau contactați ANMDMR pentru informații suplimentare.
Anunțul Comisiei Europene poate fi accesat la: https://health.ec.europa.eu/latest-updates/updated-information-pack-candidate-eu-reference-laboratories-published-2022-11-30_en
descarca documentul…
- Anunț important
23.11.2022
În atenția operatorilor economici și a tuturor părților interesate
Vă informăm că din data de 22 noiembrie 2022 au intrat în vigoare noile tarife aplicate pentru serviciile prestate de ANMDMR prin publicarea în Monitorul Oficial al României, Partea I, Nr.1123/22.XI.2022 a ORDINULUI Nr. 3467 din 17 noiembrie 2022 privind aprobarea cuantumului tarifelor pentru activitățile desfășurate de Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România în domeniul dispozitivelor medicale.
Puteți accesa acest ordin în secțiunea Dispozitive medicale/ Legislație– Dispozitive medicale/ Ordine de ministru/2022 urmând linkul:
https://www.anm.ro/_/DM/LEGISLATIE/Ordin%203467-2022.pdf
Formularele de plată pot fi descărcate din secțiunea Formulare si tarife – Dispozitive medicale:
https://www.anm.ro/dispozitive-medicale/formulare-si-tarife/ - Anunț important
07.11.2022
În atenția reprezentanților autorizați, producătorilor, operatorilor economici și a tuturor părților interesate
Vă informăm că în data de 31 octombrie 2022, Comisia Europeană a publicat ghidul MDCG 2022-16: Îndrumări privind reprezentanții autorizați pe regulamentul (UE) 2017/745 destinat dispozitivelor medicale (MDR) și Regulamentul (UE) 2017/746 destinat dispozitivelor medicale de diagnostic in vitro (IVDR).
Acest document de orientare este scris pentru reprezentanții autorizați, producători și alți operatori economici și intenționează să ofere îndrumări cu privire la cerințele relevante în temeiul celor două regulamente.
Acolo unde clarificarea este deja acoperită de alte orientări MDCG, este inclusă o referință.
Cerința de a avea un reprezentant autorizat nu se aplică dispozitivelor destinate investigațiilor clinice (MDR) sau studiului de performanță (IVDR).
În acest scop, articolul 62 alineatul (2) MDR și articolul 58 alineatul (4) IVDR precizează că „în cazul în care sponsorul unei investigații clinice sau al unui studiu de performanță nu este stabilit în Uniune, sponsorul respectiv se asigură că o persoană fizică sau juridică este stabilită în Uniunea în calitate de reprezentant legal al acesteia”.
Deoarece reprezentantul legal nu este definit ca reprezentant autorizat, aceste cerințe nu sunt incluse în acest ghid.
Anunțul Comisiei Europene poate fi accesat la: https://health.ec.europa.eu/latest-updates/mdcg-2022-16-guidance-authorised-representatives-regulation-eu-2017745-and-regulation-eu-2017746-2022-10-31_en
descarca documentul…
- Anunț important
31.10.2022
În atenția producătorilor de dispozitive medicale pentru diagnostic in vitro, organismelor notificate și a tuturor părților interesate
Vă informăm că în data de 04.07.2022, Comisia Europeană a publicat regulamentul (UE) 2022/1107 de stabilire a unor specificații comune pentru anumite dispozitive medicale pentru diagnostic in vitro din clasa D în ceea ce privește cerințele referitoare la caracteristicile de performanță în conformitate cu Regulamentul (UE) 2017/746 al Parlamentului European și al Consiliului.
În cazul anumitor dispozitive medicale pentru diagnostic in vitro din clasa D care intră în domeniul de aplicare al Regulamentului (UE) 2017/746 nu există standarde armonizate în ceea ce privește anumite cerințe din anexa I la regulamentul respectiv și a fost necesar să se abordeze preocupări din sfera sănătății publice întrucât riscul asociat utilizării respectivelor dispozitive este semnificativ pentru sănătatea publică și pentru siguranța pacienților. Prin urmare, au fost adoptate specificații comune pentru dispozitivele în cauză în ceea ce privește cerințele respective.
Acest regulament îl regăsiţi accesând linkul:
https://eur-lex.europa.eu/legal-content/RO/TXT/PDF/?uri=CELEX:32022R1107&from=EN - Anunț important
14.10.2022
În atenția producătorilor din domeniul dispozitivelor medicale și a tuturor părților interesate
În data de 13.10.2022 a fost publicată în Monitorul Oficial al României, partea I, nr.995,
Ordonanță de urgență privind stabilirea cadrului instituțional, precum și măsurile necesare pentru asigurarea aplicării directe a prevederilor Regulamentului (UE) 2017/746
al Parlamentului European și al Consiliului din 5 aprilie 2017 privind dispozitivele medicale pentru diagnostic in vitro și de abrogare a Directivei 98/79/CE și a Deciziei 2010/227/UE a Comisiei
Textul ordonanței poate fi consultat în secțiunea Dispozitive medicale – Legislație dispozitive medicale – Legi, ordonanțe și hotărâri de guvern – 2022 - Anunț important
10.10.2022
În atenția producătorilor de dispozitive fabricate la comandă, cu sediul în România
Vă informăm că a fost publicat în Monitorul Oficial Nr. 977 din 7 octombrie 2022 Ordinul Nr. 2.845 din 29 septembrie 2022 privind aprobarea Normelor metodologice pentru aplicarea prevederilor art. 13 din Ordonanţa de urgenţă a Guvernului nr. 46/2021 privind stabilirea cadrului instituţional şi a măsurilor pentru punerea în aplicare a Regulamentului (UE) 2017/745 al Parlamentului European şi al Consiliului din 5 aprilie 2017 privind dispozitivele medicale, de modificare a Directivei 2001/83/CE, a Regulamentului (CE) nr. 178/2002 şi a Regulamentului (CE) nr. 1.223/2009 şi de abrogare a Directivelor 90/385/CEE şi 93/42/CEE ale Consiliului, privind înregistrarea dispozitivelor fabricate la comandă introduse pe piaţă sub propriul nume de producătorii cu sediul în România.
Acest ordin poate fi regăsit și în secțiunea Legislație – Dispozitive medicale – Ordine de ministru.
Formularul de cerere se poate descărca din secțiunea Formulare si tarife – Dispozitive medicale. - Anunț important
19.09.2022
În atenția producătorilor de dispozitive medicale pentru diagnostic in vitro, operatorilor economici, organismelor notificate și a tuturor părților interesate
Vă informăm că în data de 14 septembrie 2022, Comisia Europeană a publicat ghidul MDCG 2022-15 cu privire la Îndrumări privind supravegherea adecvată cu privire la dispozițiile tranzitorii din Articolul 110 din IVDR cu privire la dispozitive acoperite de certificate emise conform IVDD.
Acest document oferă informații cu privire la Articolul 110 alineatul (2) și articolul 110 alineatul (3) din Regulamentul (UE) 2017/746 privind dispozitivele medicale de diagnostic in vitro (IVDR), precizează că dispozitivele care sunt acoperite de certificate valabile emise de un organism notificat conform Directivei 98/79/CE privind dispozitivele medicale de diagnostic in vitro (IVDD) pot fi puse pe piață sau puse în funcțiune după data aplicării IVDR și nu mai târziu de 26 mai 2025 în anumite condiții.
Condițiile menționate mai sus impun ca organismul notificat care a eliberat certificatul în temeiul IVDD continuă să efectueze o supraveghere adecvată în ceea ce privește aplicabilitatea cerințelor referitoare la dispozitivele pe care le-a certificat. Prin urmare, este important pentru producători, organisme notificate și autorități naționale să aibă claritate cu privire la activitățile ce iau parte la supravegherea corespunzătoare menționată la articolul 110 alineatul (3) din IVDR.
Pentru a aborda în mod corespunzător aplicarea dispozițiilor tranzitorii la dispozitivele vizate de certificate emise conform IVDD, acest ghid, elaborat în conformitate cu MDCG 2022-4 Guidance on appropriate surveillance regarding the transitional provisions under Article 120 of the MDR (https://health.ec.europa.eu/latest-updates/mdcg-2022-4-guidance-appropriate-surveillance-regarding-transitional-provisions-under-article-120-2022-02-16_en) și MDCG 2022-8 Regulation (EU) 2017/746 – application of IVDR requirements to ‘legacy devices’ and to devices placed on the market prior to 26 May 2022 (https://health.ec.europa.eu/latest-updates/mdcg-2022-8-regulation-eu-2017746-application-ivdr-requirements-legacy-devices-and-devices-placed-2022-05-20_en) , ar trebui citit împreună cu ghidul MDCG 2022-6 – Guidance on significant changes regarding the transitional provision under Article 110(3) of the IVDR (https://health.ec.europa.eu/latest-updates/mdcg-2022-6-guidance-significant-changes-regarding-transitional-provision-under-article-1103-ivdr-2022-05-04_en) .
În scopul acestui document, „legacy devices” ar trebui înțelese ca fiind dispozitive care, în conformitate cu articolul 110 alineatul (3) din IVDR, sunt introduse pe piață după data de aplicare a IVDR (26 mai 2022) și până la sfârșitul perioadei de tranziție respective prevăzute în articolul 110 alineatul (3) al 2-lea sau al 3-lea paragraf, dacă sunt îndeplinite anumite condiții.
În acest ghid sunt abordate numai dispozitivele acoperite de un certificat CE valabil, eliberat în conformitate cu IVDD înainte de 26 Mai 2022.
Anunțul Comisiei Europene poate fi accesat la: https://health.ec.europa.eu/system/files/2022-09/mdcg_2022-15_en.pdf - Anunț important
19.09.2022
În atenția producătorilor de dispozitive medicale pentru diagnostic in vitro, operatorilor economici, organismelor notificate și a tuturor părților interesate
Vă informăm că în data de 14 septembrie 2022, Comisia Europeană a publicat ghidul MDCG 2021-22 Rev.1 cu privire la Clarificarea privind „prima certificare pentru acel tip de dispozitiv” și procedurile corespunzătoare care trebuie urmate de organismele notificate în contextul consultării grupului de experți menționat la art 48(6) din Regulamentul (UE) 2017/746.
Acest document oferă informații cu privire la dispozitivelele de clasa D, articolul 48 alineatul (6) din Regulamentul (UE) 2017/746 privind dispozitivele medicale de diagnostic in vitro (IVDR) – stabilește condițiile care trebuie aplicate de către organismul notificat pentru a determina dacă trebuie să consulte grupul de experți cu privire la raportul de evaluare a performanței al producătorului.
Aceste condiții sunt: (1) absența unor specificații comune pentru dispozitivul de clasa D în cauză,
(2) unde este prima certificare pentru acel tip de dispozitiv.
Acest ghid oferă clarificări cu privire la semnificația acestor condiții și la procedurile corespunzătoare care trebuie urmate de către organismul notificat.
Anunțul Comisiei Europene poate fi accesat la: https://health.ec.europa.eu/system/files/2022-09/mdcg_2021-22_en.pdf - Anunț important
14.09.2022
În atenția persoanelor interesate
În atenția operatorilor economici (OE) care solicită avizarea activității de import dispozitive medicale, conform art. 2, lit. a) din Normele metodologice de aplicare a titlului XX din legea 95/2006 privind reforma în domeniul sănătății, referitoare la avizarea activităților în domeniul dispozitivelor medicale (DM), aprobate cu OMS 566/2020 (Norme).
descarca documentul…
- Anunț important
13.09.2022
În atenția tuturor părților interesate (utilizatori, distribuitori etc.)
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți utilizatorii de anestezic local pe bază de benzocaină, TOPIGEL, producător LABORATORIOS CLARBEN, SA, Spania, încadrat greșit în categoria dispozitivelor medicale (clasă I), să oprească de îndată utilizarea, să returneze produsele către distribuitorii de la care le-au achiziționat și să sesizeze situația proprie către Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România – Serviciul Supraveghere Piață.
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți distribuitorii de anestezic local pe bază de benzocaină, TOPIGEL, producător LABORATORIOS CLARBEN, SA, Spania să oprească de îndată punerea la dispoziție a acestui produs pe piața din România, să notifice Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România privind stocul deținut și privind furnizorii de la care s-au aprovizionat cu aceste produse. - Anunț important
09.09.2022
În atenția persoanelor interesate
Consecințele legale ale refuzului sau întârzierii unui control inopinat
În calitate de autoritate de supraveghere a pieței, ANMDMR acționează în interesul operatorilor economici, al utilizatorilor finali și al personalului de specialitate utilizator pentru a asigura că interesele publice care intră sub incidența legislației de armonizare a Uniunii relevante privind dispozitivele medicale sunt permanent menținute și protejate prin intermediul unor măsuri de asigurare a aplicării legislației adecvate, precum și că respectarea acestei legislații este asigurată de-a lungul lanțului de aprovizionare prin controale adecvate. În această calitate, ANMDMR are competența de a efectua inspecții la fața locului și controale fizice ale produselor fără a le anunța în prealabil, competența de a intra în orice sediu, pe orice teren sau în orice mijloc de transport pe care operatorul economic în cauză îl utilizează în scopuri legate de activitatea sa comercială, de afaceri sau profesională, pentru a identifica neconformitatea și a obține elemente de probă (art.14 alin(4) din Regulamentul (UE) 2019/1020 privind supravegherea pieței și conformitatea produselor și de modificare a Directivei 2004/42/CE și a Regulamentelor (CE) nr. 765/2008 și (UE) nr. 305/2011).
Art. 93 din Regulamentul 2017/745 privind dispozitivele medicale prevede că autoritatea competentă desfășoară atât inspecţii anunţate cât și în cazul în care este necesar, inspecţii neanunţate la sediile operatorilor economici precum și la sediile furnizorilor și/sau ale subcontractanţilor și acolo unde este necesar, în unităţile utilizatorilor profesioniști.
De asemenea, prin art. 928 din Legea 95/2006 republicată, se stabilește că dispozitivele medicale puse în funcţiune şi aflate în utilizare se supun următoarelor modalități de control: inspecţie şi testare inopinată, supraveghere în utilizare.
Prin art. 8 din Hotărârea nr. 306 din 23 martie 2011 privind unele măsuri de supraveghere a pieţei produselor reglementate de legislaţia Uniunii Europene care armonizează condiţiile de comercializare a acestora, se precizează că Supravegherea produselor introduse pe piaţă şi/sau puse în funcţiune se realizează inclusiv prin organizarea de controale inopinate şi de verificări punctuale.
Având în vedere cele de mai sus, vă informăm căîmpiedicarea fără drept, sub orice formă, a persoanelor împuternicite să îşi exercite atribuţiile prevăzute în prezentul titlu, constituie contravenție și se sancționează cu amendă de la 5.000 lei la 10.000 lei conform art. 935 alin. 1) lit. g) din Legea 95/2006 republicată.
Prin art.18 din O.G. 2/2001 privind regimul juridic al contravenţiilor se prevede că în caz de refuz, pentru legitimarea contravenientului, agentul constatator poate apela la poliţişti, jandarmi sau poliţişti locali. (“Art.18. Contravenientul este obligat să prezinte agentului constatator, la cerere, actul de identitate ori documentele în baza cărora se fac menţiunile prevăzute la art. 16 alin.(1) şi (11). În caz de refuz, pentru legitimarea contravenientului, agentul constatator poate apela la poliţişti, jandarmi sau poliţişti locali.”)
Prin verificările efectuate și eliminarea dispozitivelor medicale neconforme, ne dorim să asigurăm un nivel înalt de protecţie a sănătăţii şi siguranţei pacienţilor și a utilizatorilor, aceste acțiuni vizând interesul public general. - Anunț important
08.09.2022
În atenția reprezentanților legali și a persoanelor responsabile cu dispozitivele medicale din cadrul spitalelor
În calitate de autoritate de supraveghere a pieței, ANMDMR acționează în interesul operatorilor economici, al utilizatorilor finali și al personalului de specialitate utilizator, pentru a asigura că interesele publice care intră sub incidența legislației de armonizare a Uniunii relevante privind dispozitivele medicale sunt permanent menținute și protejate prin intermediul unor măsuri de asigurare a aplicării legislației adecvate, precum și că respectarea acestei legislații este asigurată de-a lungul lanțului de aprovizionare prin controale adecvate. În această calitate, ANMDMR are competența de a efectua inspecții la fața locului și controale fizice ale produselor, fără a le anunța în prealabil, competența de a intra în orice sediu, pe orice teren sau în orice mijloc de transport pe care operatorul economic în cauză le utilizează în scopuri legate de activitatea sa comercială, de afaceri sau profesională, pentru a identifica neconformitatea și a obține elemente de probă (art. 14 alin (4) din Regulamentul (UE) 2019/1020 privind supravegherea pieței și conformitatea produselor și de modificare a Directivei 2004/42/CE și a Regulamentelor (CE) nr. 765/2008 și (UE) nr. 305/2011.Art 93 din Regulamentul 2017/745 privind dispozitivele medicale prevede că autoritatea competentă desfășoară atât inspecţii anunţate, cât și, în cazul în care este necesar, inspecţii neanunţate la sediile operatorilor economici, precum și la sediile furnizorilor și/sau ale subcontractanţilor, și, acolo unde este necesar, în unităţile utilizatorilor profesioniști.
Vă informăm că în perioada următoare, în cadrul activității de supraveghere de piață și a tematicilor de control stabilite la nivelul ANMDMR/DGDM/DRSP se vor desfășura controale la unitățile spitalicești, care vor viza verificarea respectării prevederilor legale în vigoare în domeniul dispozitivelor medicale aflate în utilizare.
În cadrul controalelor respective se vor verifica în principal următoarele aspecte:
– dacă este desemnată o persoană responsabilă cu menţinerea evidenţei dispozitivelor medicale aflate în utilizare şi ca persoană de contact în relaţia cu ANMDMR;
– dacă este instituit un registru al dispozitivelor medicale aflate în utilizare conform normelor metodologice în vigoare;
– dacă este asigurată instalarea, mentenanţa şi repararea dispozitivelor medicale cu unităţi avizate pentru efectuarea acestor servicii;
– dacă este asigurată verificarea periodică a dispozitivelor medicale utilizate, conform prevederilor legale;
– dacă dispozitivele medicale sunt utilizate numai în perioada de valabilitate a acestora, când este cazul, şi că nu prezintă abateri de la performanţele funcţionale şi de la cerinţele de securitate aplicabile;
– dacă sunt asigurate condiţii optime de păstrare şi depozitare a dispozitivelor medicale, conform cerinţelor specificate de producător;
– dacă eticheta şi instrucţiunile de utilizare ale dispozitivelor medicale/accesoriilor dispozitivelor medicale și a consumabilelor aflate în utilizare/depozit respectă cerinţele prevăzute în anexa I cap. III pct. 23 din Regulamentul (UE) 2017/745, respectiv cerinţele prevăzute în anexa I cap. III pct. 20 din Regulamentul (UE) 2017/746 în cazul dispozitivelor medicale pentru diagnostic in vitro.La următoarea adresă: https://www.anm.ro/dispozitive-medicale/supraveghere-in-utilizare/
sunt evidențiate o parte din obligațiile legale ale utilizatorilor profesioniști de dispozitive medicale.
Legislația avută în vedere în cadrul tematicii de control este următoarea:–Legea Nr. 95 Republicată*) din 14 aprilie 2006 privind reforma în domeniul sănătăţii-Titlul XX
*) Cuprinde toate modificările aduse actului oficial publicate în M.Of., inclusiv cele prevăzute în: O.G. Nr. 37/31.08.2022 Publicată în M.Of. Nr. 857/31.08.2022
Legea respectivă se poate accesa la link-ul de mai jos:
(https://www.anm.ro/_/DM/LEGISLATIE/legea%2095_titlul%20XX_05.09.2022.pdf )– ORDIN Nr. 2.219 din 14 iulie 2022 privind controlul prin verificare periodică a dispozitivelor medicale aflate în utilizare, evaluarea performanţelor dispozitivelor medicale secondhand puse în funcţiune şi eliberarea avizului de utilizare pentru dispozitivele medicale din dotarea mijloacelor de intervenţie pentru asistenţă medicală de urgenţă prespitalicească;
Ordinul respectiv se poate accesa la link-ul de mai jos:
(https://www.anm.ro/_/DM/LEGISLATIE/15.2.%20ORDIN%202219%20DIN%2014%20IULIE%202022.pdf )– Ordinul ministrului sănătății nr. 2882/2021 privind modalitatea de raportare a incidentelor grave suspectate în legătură cu dispozitivele medicale;
Ordinul respectiv se poate accesa la link-ul de mai jos:
(https://www.anm.ro/_/DM/Ordin%202882-2021.pdf )– Ordinul nr. 566/2020 pentru aprobarea Normelor metodologice de aplicare a titlului XX din Legea nr. 95/2006 privind reforma în domeniul sănătății, referitoare la avizarea activităților în domeniul dispozitivelor medicale;
Ordinul respectiv se poate accesa la link-ul de mai jos:
(https://www.anm.ro/_/DM/Ordinul%20nr.%20566%20si%20Anexe.pdf )– REGULAMENTUL (UE) 2017/745 AL PARLAMENTULUI EUROPEAN ȘI AL CONSILIULUI din 5 aprilie 2017 privind dispozitivele medicale, de modificare a Directivei 2001/83/CE, a Regulamentului (CE) nr. 178/2002 și a Regulamentului (CE) nr. 1223/2009 și de abrogare a Directivelor 90/385/CEE și 93/42/CEE ale Consiliului;
Regulamentul respectiv se poate accesa la link-ul de mai jos:
(https://eur-lex.europa.eu/legal-content/EN/TXT/?uri=CELEX%3A02017R0745-20200424&qid=1651491231964 )– ORDONANȚĂ DE URGENȚĂ nr. 46 din 9 iunie 2021privind stabilirea cadrului instituțional și a măsurilor pentru punerea în aplicare a Regulamentului (UE) 2017/745 al Parlamentului European și al Consiliului din 5 aprilie 2017 privind dispozitivele medicale, de modificare a Directivei 2001/83/CE, a Regulamentului (CE) nr. 178/2002 și a Regulamentului (CE) nr. 1.223/2009 și de abrogare a Directivelor 90/385/CEE și 93/42/CEE ale Consiliului.
OUG se poate accesa la link-ul de mai jos:
(https://legislatie.just.ro/Public/DetaliiDocument/243191 )– REGULAMENTUL (UE) 2017/746 AL PARLAMENTULUI EUROPEAN ȘI AL CONSILIULUI din 5 aprilie 2017 privind dispozitivele medicale pentru diagnostic in vitro și de abrogare a Directivei 98/79/CE și a Deciziei 2010/227/UE a Comisiei.
Regulamentul respectiv se poate accesa la link-ul de mai jos:
(https://eur-lex.europa.eu/legal-content/EN/TXT/?uri=CELEX%3A02017R0746-20220128&qid=1651491186034 )Prin verificările efectuate și eliminarea dispozitivelor medicale neconforme ne dorim să asigurăm un nivel înalt de protecţie a sănătăţii şi siguranţei pacienţilor și a utilizatorilor, aceste acțiuni vizând interesul public general.
- Anunț important
30.08.2022
În atenția tuturor părților interesate de emiterea unei derogări de la procedurile de evaluare a conformității
În baza unei cereri justificate, ANMDMR autorizează introducerea pe piață sau punerea în funcțiune pe teritoriul României, a unui anumit dispozitiv pentru care procedurile de evaluare a conformității nu au fost efectuate, dar a cărui utilizare este în interesul sănătății publice sau sănătății pacienților, în conformitate cu prevederile art. 59 din Regulamentul (UE) 2017/745 privind dispozitivele medicale.
Această derogare națională se aplică pentru o perioadă limitată de timp (perioada considerată rezonabilă pentru finalizarea procedurii de evaluare a conformității sau de necesitatea în utilizare a dispozitivelor medicale care fac obiectul derogării naționale), doar în cazuri excepționale, bine justificate, când nu există un produs similar pe piață, când producătorul demonstrează că a demarat procedurile de evaluare a conformității sau, după caz, că a fost împiedicat să finalizeze sau să inițieze aceste proceduri de circumstanțe excepționale și imprevizibile.
Pentru obținerea derogării, solicitantul transmite la ANMDMR o cerere însoțită de de documente care să justifice faptul că produsul este sigur în utilizare (declarație de conformitate emisă de producător, certificat de conformitate emis de un organism notificat (după caz), specificație tehnică, etichetă, instrucțiuni de utilizare, dovezi referitoare la lipsa reclamațiilor /incidentelor, dovezi referitoare la demersurile întreprinse în ceea ce privește certificarea, alte certificate/avize/autorizații obțiute) precum și dovezi referitoare la necesitatea dispozitivului medical pe piață (lipsa unui înlocuitor și necesitatea acoperirii segmentului respectiv).
Pentru soluționarea cererii, ANMDMR poate solicita suplimentar documente prevăzute în legislația aplicabilă tipului de dispozitiv medical. - Anunț important
30.08.2022
În atenția persoanelor interesate
Ghid privind capacitatea organismelor notificate și disponibilitatea dispozitivelor medicale
Vă informăm că în data de 26 August 2022, Grupul de Coordonare privind dispozitivele medicale (MDCG) al Comisiei Europene a emis un document de poziție, MDCG 2022-14 ”Transition to the MDR and IVDR. Notified body capacity and availability of medical devices and IVDs” al cărui conținut poate fi consultat la : https://health.ec.europa.eu/latest-updates/mdcg-2022-14-transition-mdr-and-ivdr-notified-body-capacity-and-availability-medical-devices-and-2022-08-26_en. - Anunț important
16.08.2022
În atenția tuturor părților interesate de dispozitivele fără scop medical
Vă informăm că proiectul final al Regulamentului de punere în aplicare privind reclasificarea grupelor de produse active fără scop medical enumerate în anexa XVI din Regulamentul (UE) 2017/745 al Parlamentului European și al Consiliului din 5 aprilie 2017 privind dispozitivele medicale, de modificare a Directivei 2001/83/CE, a Regulamentului (CE) nr. 178/2002 și a Regulamentului (CE) nr. 1223/2009 și de abrogare a Directivelor 90/385/CEE și 93/42/CEE ale Consiliului, a fost publicat spre consultare pe site-ul Comisiei Europene, DG SANTE la https://ec.europa.eu/info/law/better-regulation/have-your-say/initiatives/12972-Medical-devices-reclassification-of-products-without-an-intended-medical-purpose_en
Toti cei interesați pot trimite comentarii până la data de 8 Septembrie 2022. - Anunț important
26.07.2022
În atenția tuturor părților interesate de emiterea unei negații
Vă informăm că în data de 25 iulie 2022 a fost publicat în Monitorul Oficial nr. 745 Ordinul ministrului sănătății nr. 2.242/2022 privind aprobarea procedurii de emitere a negațiilor pentru produsele care nu intră în domeniul de aplicare al Regulamentului (UE) 2017/745 al Parlamentului European și al Consiliului din 5 aprilie 2017 privind dispozitivele medicale, de modificare a Directivei 2001/83/CE, a Regulamentului (CE) nr. 178/2002 și a Regulamentului (CE) nr. 1.223/2009 și de abrogare a Directivelor 90/385/CEE și 93/42/CEE ale Consiliului.
Părtile interesate de emiterea unei negații pot consulta acest document în secțiunea “Legislație – Dispozitive medicale“.
Formularul de cerere se poate descărca din secțiunea “Formulare si tarife – Dispozitive medicale“.
Negațiile se emit pentru produsele pentru care nu există certitudinea încadrării acestora sub incidenţa definiţiei dispozitivului medical și nu pentru toate produsele puse în circulație pe piața UE, care nu sunt dispozitive medicale. - Anunț important
25.07.2022
În atenția laboratoarelor din domeniul diagnostic in vitro din România și a tuturor părților interesate
Direcția Generală pentru Sănătate și Siguranța Alimentelor a Comisiei Europene (DG SANTE) lansează oficial un apel la candidaturi pentru desemnarea laboratoarelor de referință UE în domeniul dispozitivelor medicale de diagnostic in vitro, în temeiul Regulamentului (UE) 2017/ 746 privind dispozitivele medicale de diagnostic in vitro.
În conformitate cu articolul 100 alineatul (1) din Regulamentul (UE) 2017/746, cererile pot fi depuse numai de către statele membre prin autoritatea competentă.
Laboratoarele care intenţionează să se înregistreze în vederea desemnării ca Laborator de referinţă UE trebuie să respecte cu stricteţe o serie de cerinţe şi termenele limită de depunere a cererilor.
Statelor membre li se solicită să depună cereri de înregistrare în vederea desemnării până pe 31 martie 2023, ora 12:00, ora Europei Centrale. Nu este posibilă prelungirea termenului limită și orice cerere depusă după acest termen nu va fi luată în considerare.
Pentru respectarea acestui termen, este recomandat ca laboratoarele candidate să-și trimită cererile în statele lor membre până pe 5 ianuarie 2023, ora 12:00, ora Europei Centrale.
Sarcinile și criteriile pe care trebuie să le îndeplinească laboratoarele de referință ale Uniunii Europene în domeniul dispozitivelor medicale pentru diagnostic in vitro se regăsesc în REGULAMENTUL DE PUNERE ÎN APLICARE (UE) 2022/944 AL COMISIEI din 17 iunie 2022 de stabilire a normelor de aplicare a Regulamentului (UE) 2017/746 al Parlamentului European și al Consiliului.
Acest regulament şi mai multe informaţii regăsiţi accesând linkul:
https://health.ec.europa.eu/latest-updates/setting-scene-eu-reference-labs-high-risk-diagnostics-2022-06-21_en
Cei interesaţi sunt invitaţi să contacteze Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale din România pentru obţinerea tuturor informaţiilor necesare în vederea înregistrării candidaturilor pe adresa de mail dgdm@anm.ro. - Anunț important
25.07.2022
În atenția producătorilor de dispozitive medicale pentru diagnostic in vitro, operatorilor economici organismelor notificate și a tuturor părților interesate
Vă informăm că a fost implementată o nouă versiune de producție a modulelor de înregistrare a actorilor EUDAMED, UDI/Dispozitive și NB-uri și certificate.
• EUDAMED restricționat
• EUDAMED public
Această versiune aduce îmbunătățiri și asigură remedierea erorilor. Documentația relevantă este disponibilă în meniul Ajutor EUDAMED și pot găsi, de asemenea, mai jos notele de lansare.
Odată cu această versiune, s-a lansat prima versiune BETA a noului Centru de informare EUDAMED pentru producția EUDAMED, disponibilă în Ajutor > Ghid de utilizare.
Principalele îmbunătățiri ale Centrului de informații EUDAMED:
• consolidează toate Ghidurile utilizatorului de producție EUDAMED;
• acces rapid și structurat la informații;
• documente complet descărcabile
• formular de contact pentru a ajunge la Echipa de SUPORT EUDAMED
descarca documentul…
- Anunț important
22.07.2022
În atenția persoanelor interesate
ORDIN Nr. 2.219 din 14 iulie 2022 privind controlul prin verificare periodică a dispozitivelor medicale aflate în utilizare, evaluarea performanţelor dispozitivelor medicale secondhand puse în funcţiune şi eliberarea avizului de utilizare pentru dispozitivele medicale din dotarea mijloacelor de intervenţie pentru asistenţă medicală de urgenţă prespitalicească
descarca documentul…
- Anunț important
21.07.2022
În atenția medicilor dentiști, importatorilor și distribuitorilor de dispozitive medicale
ANMDMR atenționează medicii dentiști, importatorii și distribuitorii de dispozitive medicale faptul că în perioada 12 Martie 2017 – 4 Martie 2022, producătorul SADENT, Grecia a introdus pe piața UE dispozitivul medical dentar SADENT COMPOSITE, marcat CE 0653, în condițiile în care nu deținea un certificat de conformitate CE, emis de Organismul Notificat 0653 – NATIONAL EVALUATION CENTER OF QUALITY AND TECHNOLOGY IN HEALTH S.A.- EKAPTY.
Întrucât pentru introducerea pe piața UE a acestui tip de dispozitiv medical, evaluarea conformității cu cerințele de reglementare aplicabile trebuia să fie efectuată cu implicarea unui Organism Notificat, solicităm părților interesate să nu utilizeze sau să pună la dispoziție pe piața din România acest tip de compozit, introdus pe piață în perioada mai sus menționată și să informeze ANMDMR la adresa de e-mail: mdevice@anm.ro dacă dețin informații privind prezența pe piața din România a acestui dispozitiv medical. - Anunț important
19.07.2022
În atenția operatorilor economici (OE) care solicită Avizul de funcționare
În conformitate cu cod indicator 12 din Opis documentație evaluare activitate de import/distribuție dispozitive medicale (DM), respectiv cod indicator 13 din Opis documentație evaluare activitate de instalare și/sau mentenanță DM, operatorii economici trebuie să facă dovada că, pentru procesele și activitățile supuse avizării, au documentate, implementate și menținute proceduri/instrucțiuni de lucru conforme. Pentru evitarea neconformităților în elaborarea procedurilor/instrucțiunilor de lucru, ANMDMR vă pune la dispoziție un ghid cu recomandări referitoare la elaborarea procedurilor/instrucțiunilor de lucru, întocmit în concordanță cu cerințele legislative aplicabile DM și a specificațiilor din standarde de management al calității.
descarcă documentul …
- Anunț important
18.07.2022
În atenția producătorilor de dispozitive medicale din România și a oraganismelor notificate
Autoritățile de supraveghere a pieței pentru domeniul dispozitivelor medicale din Statele Membre au hotărât să emită o informare asupra punerii pe piață a dispozitivelor medicale de tip spray nazal, din care rezultă următoarele:
– Spray-urile nazale care își exercită principala acțiune prin mijloace farmacologice, imunologice sau metabolice nu sunt dispozitive medicale. Acestea pot fi produse medicinale în conformitate cu Directiva 2001/83/EC și pot face obiectul unei autorizații de comercializare.
– Spray-urile nazale care se încadrează în definiția de la art. 2(1) din MDR și își exercită acțiunea prin mijloace fizice sau mecanice consituie dispozitive medicale. Clasificarea acestora se va face potrivit regulilor din anexa VIII a MDR. Ca regulă generală, se aplică regula 21 când spray-ul conține o substanță sau o combinație de substanțe care se introduce în corpul uman printr-un orificiu natural și sunt absorbite sau dispersate local în corpul uman.
– Spray-urile nazale care se încadrează în definiția de la art. 2(1) din MDR și incorporează o substanță care utilizată separate poate fi considerată produs medicinal și va fi clasificat conform regulii 14.
– Clasificarea spray-urilor nazale este minim în clasa IIa, iar procedurile de evaluarea conformității implcă un organism notificat.
– Producătorii care nu au solicitat unui organism notificat evaluarea conformității, sunt încurajați să procedeze la aceasta.
Textul integral al informării se poate vizualiza aici.
Reamintim producătorilor români de dispozitive medicale de tip spray nazal, încadrate în clasa I conform MDD, HG 54/2009, că în temeiul art.120 (3) din MDR, pot pune la dispoziție pe piață aceste produse până la 26 mai 2024, cu condiția întocmirii declarației de reclasificare conform regulilor din Anexa VIII MDR. Având în vedere durata mare de timp pentru parcurgerea procesului de evaluarea conformității până la obținerea certificatului, recomandăm producătorilor să contacteze cât mai curând un organism notificat.
Lista acestora poate fi consultată pe site-ul ANMDMR la rubrica Dispozitive medicale / Organisme notificate. - Anunț important
15.07.2022
În atenția producătorilor de dispozitive medicale pentru diagnostic in vitro, operatorilor economici, organismelor notificate și a tuturor părților interesate
Vă informăm că în data de 13 iulie 2022, Comisia Europeană a publicat Ghidul cu privire la practicile administrative armonizate și soluții tehnice alternative până când Eudamed este pe deplin funcțional (pentru Regulamentul (UE) 2017/746 privind dispozitivele medicale de diagnostic in vitro).
Acest document oferă îndrumări statelor membre și altor părți relevante cu privire la aplicarea anumitor prevederi IVDR în timpul absenței lui Eudamed. În acest scop, acest ghid intenționează să descrie practici administrative armonizate și soluții tehnice alternative pentru schimbul de informații până când Eudamed devine pe deplin funcțional.
descarcă documentul …
- Anunț important
06.07.2022
În atenția producătorilor din domeniul dispozitivelor medicale și a tuturor părților interesate
Vă informăm că în luna iunie Grupul de Coordonare privind dispozitivele medicale (MDCG) a emis un document de poziție, MDCG 2022-11 ” Notificare către producători pentru a asigura conformitatea în timp util cu cerințele MDR”, al cărui conținut poate fi consultat mai jos:
MDCG 2022-11 …
Acesta constituie un apel către producătorii de dispozitive medicale, de a se alinia cât mai curând la cerințele MDR și de a depune solicitările de evaluarea conformității către organismele notificate, astfel încât procedurile necesare să poată fi finalizate până la sfârșitul perioadei de tranziție, 26 mai 2024 - Anunț important
04.07.2022
În atenția laboratoarelor din domeniul diagnostic in vitro din România și a tuturor părților interesate
Vă informăm că în data de 22.06.2022 au fost publicate în Jurnalul Oficial al Uniunii europene două acte de implementare referitoare la aplicarea Regulamentului (UE) 2017/746, și anume:
Regulamentul de punere în aplicare (UE) 2022/944 al Comisiei din 17 iunie 2022
de stabilire a normelor de aplicare a Regulamentului (UE) 2017/746 al Parlamentului European și al Consiliului în ceea ce privește sarcinile și criteriile pentru laboratoarele de referință ale Uniunii Europene în domeniul dispozitivelor medicale pentru diagnostic in vitro
Regulamentul de punere în aplicare (UE) 2022/945 al Comisiei din 17 iunie 2022
de stabilire a normelor de aplicare a Regulamentului (UE) 2017/746 al Parlamentului European și al Consiliului în ceea ce privește taxele care pot fi percepute de către laboratoarele de referință ale UE în domeniul dispozitivelor medicale pentru diagnostic in vitro
acestea se referă la cerințele care trebuie îndeplinite de către laboratoare pentru a fi recunoscute ca laboratoare de referință ale UE, atribuțiile acestora și tarifele care vor fi practicate de ele în desfășurarea activităților specifice
Evaluarea și desemnarea acestor laboratoare se va face de către Comisia Europeană, cu colaborarea Joint Research Center (JRC), pe baza propunerilor autorităților naționale.
ANMDMR, în calitate de autoritate națională responsabilă, primește solicitările din partea laboratoarelor din România care intenționează să devină laboratoare de referință, în vederea evaluării preliminare.
Solicitările de informații se primesc pe adresa de e-mail: dgdm@anm.ro.
Regulamentele sunt postate la secțiunea Directive si regulamente – Dispozitive medicale. - Anunț important
07.06.2022
În atenția operatorilor economici care desfășoară activitățile de import, distribuție dispozitive medicale pentru diagnostic in vitro și a tuturor părților interesate
Vă informăm că în data de 24 mai 2022, Comisia Europeană a publicat documentul de înștiințare a părților interesate în ceea ce privește situația Elveției raportată la piața dispozitivelor medicale de diagnostic in vitro în Europa.
Până acum, Elveția a participat la piața internă a Uniunii Europene pentru dispozitive medicale de diagnostic in vitro prin capitolul dispozitive medicale din acordul de recunoaștere reciprocă (MRA) EU -Switzerland.
Capitolul Dispozitive medicale din MRA a prevăzut recunoașterea certificatelor de evaluare a conformității între Uniunea Europeană și Elveția pe baza echivalenței Directivei 98/79/CE privind dispozitivele medicale de diagnostic in vitro și legislația elvețiană corespunzătoare. Aceasta a facilitat comerțul fără întreruperi de dispozitive medicale de diagnostic in vitro între părți.
Noul Regulament (UE) 2017/746 privind dispozitivele medicale de diagnostic in vitro devine aplicabil la 26 mai 2022, înlocuind Directiva 98/79/CE.
În lipsa unei actualizări MRA care să includă Regulamentul (UE) 2017/746, partea din capitolul MRA care acoperă dispozitivele medicale de diagnostic in vitro încetează să se aplice începând cu 26 mai 2022.
Ca urmare, efectele de facilitare a comerțului ale MRA pentru dispozitivele medicale de diagnostic in vitro, inclusiv recunoașterea reciprocă a rezultatelor evaluării conformității, absența necesității unui reprezentant autorizat și a alinierii reglementărilor tehnice, încetează să se aplice de la acea dată.
Prin urmare, părțile interesate ar trebui să noteze următoarele consecințe începând cu 26 mai 2022:
– Pentru toate dispozitivele medicale de diagnostic in vitro noi, producătorii elvețieni vor fi tratați ca orice alt producător dintr-o țară terță care intenționează să-și pună dispozitivele pe piata UE. În special, dispozitivele medicale de diagnostic in vitro ale producătorilor elvețieni care necesită certificare pe baza unei evaluări a conformității procedura trebuie să fie certificată de organismele de evaluare a conformității stabilite în cadrul Uniunii Europene.
– Certificatele eliberate în temeiul MRA de către organismele de evaluare a conformității stabilite în Elveția nu vor mai fi recunoscute ca valabile în UE chiar dacă au fost emise înainte de 26 mai 2022.
– Pentru dispozitivele medicale de diagnostic in vitro introduse pe piață după 26 mai 2022, producătorii elvețieni și producătorii din țări terțe a căror reprezentanți autorizați au fost stabiliți anterior în Elveția trebuie să desemneze un reprezentant autorizat stabilit în UE.
Anunțul poate fi accesat la link-ul: Notice to Stakeholders: Status of the EU-Switzerland Mutual Recognition Agreement (MRA) for in vitro diagnostic medical devices (europa.eu) - Anunț important
31.05.2022
În atenția producătorilor de dispozitive medicale și/ sau de dispozitive medicale pentru diagnostic in vitro din România și a tuturor părților interesate
Vă informăm că puteți consulta lista standardelor armonizate pentru dispozitive medicale și dispozitive medicale pentru diagnostic in vitro la secțiunea Directive si regulamente – Dispozitive medicale. - Anunț important
02.05.2022
În atenția producătorilor de dispozitive medicale / reprezentanților autorizați
Vă informăm că în data de 28.04.2022 a fost publicat în Monitorul Oficial nr. 408 Ordinul ministrului sănătății nr. 1.171/2022 privind aprobarea procedurii de emitere a certificatului de liberă vânzare pentru dispozitivele medicale, norme de procedură în aplicarea art. 6 din OUG 46/2021.
Producătorii/ reprezentanții autorizați cu sediul în România, care doresc emiterea certificatelor de liberă vânzare, pot consulta acest document în secțiunea legislație, ordine de ministru.
Formularul de cerere se poate descărca din secțiunea Dispozitive medicale – formulare. - Anunț important
02.03.2022
În atenția producătorilor de dispozitive medicale pentru diagnostic in vitro din România și a tuturor părților interesate
Vă informăm că pe site-ul Comisiei Europene a fost lansată o consultare publică privind Proiectul de regulament de punere în aplicare și anexa acestuia privind specificațiile comune pentru anumite dispozitive medicale clasa D conform Regulamentul privind dispozitivele medicale pentru diagnostic in vitro 2017/746 (IVDR). Termenul de transmitere a observațiilor este 09.03.2022.
Acesta poate fi accesat la link-ul: In vitro diagnostic medical devices – common specifications (europa.eu) - Anunț important
22.02.2022
În atenția operatorilor economici care desfășoară activitate de import, distribuție și/sau instalare/mentenanță dispozitive medicale
Lista furnizorilor de instruire având ca tematică legislația în domeniul dispozitivelor medicale, agreați de ANMDMR
Conform OMS nr. 566/2020 pentru aprobarea Normelor metodologice de aplicare a titlului XX din Legea nr. 95/2006 privind reforma în domeniul sănătății, referitoare la avizarea activităților în domeniul dispozitivelor medicale, pentru obținerea avizului de funcționare, operatorul economic trebuie să dispună de personal suficient și calificat/instruit pentru activitatea pe care o desfășoară/domeniul în care activează.
Persoana responsabilă de conformitatea cu reglementările specifice domeniului dispozitivelor medicale și șeful de depozit trebuie să facă dovada participării la cursuri de instruire având ca tematică legislația în domeniul dispozitivelor medicale.
Art. 9, alin. (3) al OMS nr. 566/2020, mai sus menționat, prevede următoarele:
(3) Cursurile de instruire vor fi efectuate de către persoane fizice autorizate și persoane juridice care au în obiectul de activitate prestarea instruirilor prevăzute la alin. (2) lit. b) și care fac dovada experienței profesionale în activități de reglementare sau de evaluare a conformității dispozitivelor medicale astfel:
a) în activități de reglementare cu experiență profesională de cel puțin patru ani în domeniul dispozitivelor medicale sau participarea în cadrul grupurilor de lucru specifice domeniului dispozitivelor medicale la nivelul Comisiei Europene/Consiliului Uniunii Europene;
b) în activități de evaluare a conformității dispozitivelor medicale în cadrul unui organism de evaluare a conformității notificat pe directivele specifice dispozitivelor medicale, cel puțin doi ani.
De la apariția OMS 566/2020 până în prezent ANMDMR a luat legătura cu firmele care au emis diplome/certificate ca urmare a susținerii unor cursuri de instruire având ca tematică legislația în domeniul dispozitivelor medicale și pe care le-am regăsit în dosarele depuse de operatorii economici în vederea avizării activității desfășurate. În baza procedurii interne de lucru, așa cum este specificat la art. 7 al OMS 566/2020, s-au solicitat dovezile îndeplinirii cerințelor art. 9, alin. (3) de către lectorii utilizați pentru susținerea acestor cursuri.
Până la data publicării acestui anunț, firmele care au făcut dovada îndeplinirii acestor cerințe sunt următoarele:Nr. crt. Denumire persoană juridică Nume, prenume lector 1. MEDICAL DEVICE CONSULTING SERVICES SRL LAZĂR IORDACHE 2. MEDTECH CONSULTING SRL MARGARETA MIHALACHE 3. MEDICAL DEVICE LEX SRL LAZĂR IORDACHE
MARGARETA MIHALACHE4. MEDIA KOMPASS SRL NICOLAE FOTIN 5. CERTINSPECT REGISTER SRL GHEORGHE NEAGU 6. ASOCIAȚIA DE STANDARDIZARE DIN ROMÂNIA – ASRO MARGARETA MIHALACHE 7. MEDICAL DEVICE TRAINING SRL LAZĂR IORDACHE 8. EUROASIA SRL CHRISTIAN HEINRICH 9. OTD GLOBAL PRO SRL CHRISTIAN HEINRICH 10. POPI INVEST CORP SRL GHEORGHE NEAGU În momentul în care lista va suporta modificări, vom publica deîndată revizuirea acesteia. În acest sens, vă rugăm să consultați în permanență site-ul ANMDMR pentru informații actualizate.
- Anunț important
21.02.2022
În atenția producătorilor de dispozitive medicale pentru diagnostic in vitro din România și a tuturor părților interesate
REGULAMENTUL (UE) 2022/112 AL PARLAMENTULUI EUROPEAN ȘI AL CONSILIULUI din 25 ianuarie 2022 de modificare a Regulamentului (UE) 2017/746 în ceea ce privește dispozițiile tranzitorii pentru anumite dispozitive medicale pentru diagnostic in vitro și amânarea aplicării condițiilor pentru dispozitivele produse intern
Vă informăm că în data de 28 ianuarie 2022, Jurnalul Oficial al Uniunii Europene a publicat Regulamentul (UE) 2022/112 din 25 ianuarie 2022 care modifică Regulamentul (UE) 2017/746 privind dispozitivele medicale pentru diagnostic in vitro (IVDR) prin crearea de dispoziții tranzitorii pentru dispozitivele medicale pentru diagnostic in vitro specifice și prin amânarea aplicării condițiilor pentru dispozitivele produse intern.
Regulamentul (UE) 2022/112, lăsând neschimbată data aplicării IVDR la 26 mai 2022:
– prevede că dispozitivele introduse în mod legal pe piață printr-un certificat eliberat de un organism notificat în conformitate cu Directiva actuală privind dispozitivele medicale de diagnostic in vitro (Directiva 98/79/CE; IVDD) înainte de 26 mai 2022 pot continua să fie introduse pe piață sau puse în funcțiune până la 26 mai 2025.
– introduce perioade de tranziție adaptate pentru dispozitivele care trebuie să fie supuse unei evaluări a conformității care implică pentru prima dată organisme notificate în temeiul Regulamentului (IVDR), dar care au o Declarație de conformitate emisă în temeiul Directivei (IVDD) înainte de 26 mai 2022. Durata perioadei de tranziție depinde de clasa de risc a dispozitivului în cauză. Dispozitivele cu risc mai mic (dispozitive din clasa B și clasa A în stare sterilă), pot fi introduse pe piață sau puse în funcțiune până la 26 mai 2027, în timp ce dispozitivele cu risc mai mare (dispozitive de clasa D și clasa C) pot fi introduse pe piață sau puse în funcțiune numai până la 26 mai 2025 și, respectiv, 26 mai 2026. În timpul acestor perioade de tranziție extinse, dispozitivele trebuie să continue să respecte Directiva 98/79/CE. Acestea nu trebuie să aibă modificări semnificative în proiectarea și scopul propus.
– acordă timp suplimentar instituțiilor sanitare care produc dispozitive pentru a fi utilizate în propriile sedii (adică așa-numitele dispozitive produse intern) pentru a îndeplini condițiile prevăzute la articolul 5 din Regulamentul (UE) 2017/746 (IVDR).
Regulamentul (UE) 2022/112 poate fi accesat la link-ul: EUR-Lex – 32022R0112 – EN – EUR-Lex (europa.eu) - Anunț important
28.12.2021
În atenția persoanelor interesate
Din cauza unor lucrări de revizie a instalației electrice și cuplare a unui generator, furmizarea de energie electrică va fi întreruptă astăzi 28 decembrie 2021 în instituție între orele 15:30 și 17:00. Acest lucru va cauza și întreruperea accesului pe site-ul ANMDMR în acest interval. - Anunț important
23.12.2021
În atenția tuturor utilizatorilor / distribuitorilor de PRP Blood Collection Tubes (Platelet Rich Plasma) / producător ANHUI SINIC LABORATORY MEDICINE TECHNOLOGY CO. LTD., China
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți utilizatorii și distribuitorii de produse PRP Collection Tubes (Platelet Rich Plasma) producător ANHUI SINIC LABORATORY MEDICINE TECHNOLOGY CO. LTD., China să oprească imediat utilizarea sau punerea la dispoziție pe piață a acestor produse, pentru care introducerea pe piața UE s-a efectuat în baza unor documente de conformitate falsificate.
Dacă ați intrat în posesia acestor produse – PRP (Sodium Heparin), PRP (Sodium citrate + gel), PRP (Sodium citrate + gel + hyaluronic acid) sau orice alt tip de PRP Blood Collection Tubes al acestui producător, însoțite de documentele atașate, nu le utilizați sau puneți la dispoziție pe piață și sesizați Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România – Serviciul Supraveghere Piață la datele de contact existente pe site-ul ANMDMR.
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare.
descarca documentele …
- Anunț important
14.12.2021
În atenția spitalelor din România și a tuturor părților interesate
Invitație pentru spitale de a explora soluții de trasabilitate pentru seturi chirurgicale nesterile – Soluții pentru a capta identificatorul unic de dispozitiv complet (UDI-DI și UDI-PI)
Noile reglementări UE MDR 2017/745 introduc un sistem de identificare a dispozitivelor medicale bazat pe un identificator unic de dispozitiv (UDI), care permite o trasabilitate mai ușoară a acestora. Aceste reglementări impun ca instituțiile sanitare să stocheze și să păstrează, de preferință în format electronic, UDI ale dispozitivelor pe care le-au furnizat sau care le-au fost furnizate, dacă dispozitivele respective aparțin clasei III de dispozitive implantabile. Pentru alte dispozitive implantabile decât cele din clasa III, Statele Membre încurajează instituțiile sanitare și le pot solicita acestora să stocheze și să păstreze, de preferință în format electronic, UDI ale dispozitivelor care le-au fost furnizate.
Pentru a se găsi cele mai bune soluții de implementare a acestor cerințe în cadrul spitalelor, în urma solicitării Comisiei Europene s-a hotărât formarea unui grup cu părțile interesate din spitale și producătorii de dispozitive medicale, care va fi condus de MedTech Europe.
Invitația de participare în cadrul acestui grup o regăsiți atașată.
descarca invitația …
- Anunț important
06.12.2021
În atenția persoanelor interesate
Transmiterea și recepționarea mesajelor prin poșta electronică (e-mail@anm.ro)
Conform procedurilor de securitate IT&C ale A.N.M.D.M.R. publicate la adresa https://www.anm.ro/politica-de-securitate-itc/ cât și a recomandărilor Comisiei Europene, pentru a contracara phishingul, autentificarea mesajelor, raportarea și conformitatea se va face doar pe bază de domeniu (Domain-based Message Authentication, Reporting and Conformance – DMARC).
Aspecte de securitate necesare pentru livrarea mesajelor de poșta electronică către domeniul anm.ro:
✓ DMARC (Domain-based Message Authentication, Reporting and Conformance)
✓ SPF (Sender Policy Framework)
✓ Reverse DNS
✓ No Open Relay - Anunț important
24.11.2021
În atenția producătorilor români de dispozitive medicale pentru diagnostic in vitro și a tuturor părților interesate
Ghid privind evaluarea performanței dispozitivelor medicale pentru diagnostic in vitro – SARS-CoV-2 și document Q&A privind dispozitivele medicale pentru diagnostic in vitro – SARS-CoV-2
Documentul MDCG 2021-21 – Guidance on performance evaluation of SARS-CoV-2 in vitro diagnostic medical devices al Grupului de coordonare a dispozitivelor medicale oferă îndrumări cu privire la evaluarea performanței diferitelor tipuri de dispozitive medicale pentru diagnostic in vitro – SARS-CoV-2. Acesta este relevant atât pentru dispozitivele medicale pentru diagnostic in vitro care sunt introduse pe piață în temeiul Directivei 98/79/CE cât și al Regulamentului (UE) 2017/746. Poate fi accesat la link-ul: https://ec.europa.eu/health/sites/default/files/md_sector/docs/mdcg_2021-21_en.pdf
De asemenea recomandăm parcurgerea documentului Q&A al Comisiei Europene care prezintă îndrumări de bază privind dispozitivele medicale pentru diagnostic in vitro – SARS-CoV-2 în conformitate cu Directiva 98/79/EC:
https://ec.europa.eu/health/sites/default/files/md_sector/docs/covid-19_ivd-qa_en.pdf
https://ec.europa.eu/health/sites/default/files/md_sector/docs/covid-19_ivd-qa_ro.pdf
Toate ghidurile aprobate de Grupul de coordonare a dispozitivelor medicale pot fi accesate la link-ul: https://ec.europa.eu/health/md_sector/new_regulations/guidance_en - Anunț important
15.11.2021
În atenția producătorilor români de dispozitive medicale
Înregistrare UDI/Dispozitive – în EUDAMED
Noile reglementări UE MDR 2017/745 și IVDR 2017/746 introduc un sistem de identificare a dispozitivelor medicale bazat pe un identificator unic de dispozitiv (UDI), care permite o trasabilitate mai ușoară a acestora. Aceste reglementări impun ca producătorii de dispozitive medicale să transmită informațiile privind UDI/Dispozitiv pentru toate dispozitivele medicale pe care le introduc pe piață. Modulul UDI-DI/Dispozitiv al EUDAMED este utilizat în acest scop.
Din octombrie 2021 modulul UDI-DI/Dispozitiv al EUDAMED este disponibil iar producătorii pot introduce deja informațiile UDI/Dispozitiv în sistem în mod voluntar.
Pentru mai multe informații vă recomandăm să accesați site-ul Comisiei Europene la link-ul: https://ec.europa.eu/health/md_eudamed/udi_devices_registration_ro
Ghidul care vă oferă toate informațiile necesare înregistrării UDI/Dispozitive în Eudamed îl puteți accesa la link-ul: https://ec.europa.eu/health/sites/default/files/md_eudamed/docs/md_eudamed_udi-devices-user-guide_en.pdf - Anunț important
21.10.2021
În atenția tuturor părților interesate
ANMDMR atenționează părțile interesate referitor la existența pe piața din România a unor kituri pentru testări prenatale NIFTY, proceduri oferite femeilor însărcinate de către laboratoare de analize medicale în scopul identificării riscului de apariție a trisomiilor 21, 18, 13 la făt, care conțin recipiente/ dispozitive medicale (IVD) neconforme din punct de vedere al etichetării.
În activitatea de supraveghere piață, ANMDMR a interzis utilizarea unor astfel de teste în cadrul a 2 laboratoare de analize de pe teritoriul Municipiului București.
Solicităm tuturor laboratoarelor de analize medicale din România, care efectuează acest tip de testare NIFTY, să informeze ANMDMR, cu privire la desfășurarea acestei activități, la adresa de e-mail: mdevice@anm.ro în vederea verificării conformității dispozitivelor medicale (IVD) utilizate. - Anunț important
17.09.2021
În atenția tuturor părților interesate
ANMDMR informează toate părțile interesate faptul că începând de la data prezentului anunț, date privind controalele desfășurate de Direcția Generală Dispozitive Medicale – Serviciul Supraveghere Piață precum și măsurile dispuse în cauză se vor posta exclusiv în secțiunea Dispozitive medicale – Supraveghere piață.
descarca documentul …
- Anunț important
02.08.2021
În atenția persoanelor interesate
Vă informăm că la data de 11 iunie 2021 a fost publicata ORDONANȚĂ DE URGENȚĂ nr. 46 din 9 iunie 2021privind stabilirea cadrului instituțional și a măsurilor pentru punerea în aplicare a Regulamentului (UE) 2017/745 al Parlamentului European și al Consiliului din 5 aprilie 2017 privind dispozitivele medicale, de modificare a Directivei 2001/83/CE, a Regulamentului (CE) nr. 178/2002 și a Regulamentului (CE) nr. 1.223/2009 și de abrogare a Directivelor 90/385/CEE și 93/42/CEE ale Consiliului
Actul legislativ poate fi consultat la adresa
ORD DE URGENTA 46 09/06/2021 – Portal Legislativ (just.ro) - Anunț important
28.07.2021
În atenția operatorilor economici care desfășoară activitate de import, distribuție dispozitive medicale
La data de 26 mai 2021 Comisia Europeană a emis o notificare oficială cu privire la situația Acordului dintre Uniunea Europeană – Elveția privind recunoașterea reciprocă a dispozitivelor medicale în urma aplicării Regulamentului UE privind dispozitivele medicale 2017/745.
În virtutea acordului dintre Uniunea Europeană – Elveția privind recunoașterea reciprocă a dispozitivelor medicale, Elveția a făcut parte din piața internă a Uniunii Europene în ceea ce privește dispozitivele medicale. Regulamentul UE 2017/745 al dispozitivelor medicale a devenit pe deplin aplicabil la data de 26 mai 2021, înlocuind directivele anterioare privind dispozitivele medicale 90/385/CEE și 93/42/CEE. Cu toate acestea, Regulamentul UE privind dispozitivele medicale nu a fost acoperit în totalitate de Acordul dintre Uniunea Europeană – Elveția privind recunoașterea reciprocă a dispozitivelor medicale.
Drept urmare, până la atingerea unui potențial acord reciproc Uniunea Europeană- Elveția, efectele vechiului acord pentru dispozitivele medicale, inclusiv recunoașterea reciprocă a rezultatelor evaluării conformității, absența necesității unui reprezentant autorizat și alinierea la reglementări tehnice, încetează să se aplice de la data 26 mai 2021.
Elveția va avea toate obligațiile instituite prin Regulamentul dispozitivelor medicale 2017/745 statelor terțe:
– Certificatele de conformitate CE emise de organismele Notificate din Elveția nu mai sunt valabile pentru introducerea pe piață a dispozitivelor medicale în Uniunea Europeană.
– Reprezentanții autorizați cu sediul în Elveția nu mai sunt recunoscuți în UE. Aceasta înseamnă că nu sunt capabili să îndeplinească sarcini în numele producătorului în scopul introducerii dispozitivelor pe piața UE.
– Atât producătorii cu sediul în afara UE care aveau desemnat până în prezent un reprezentant autorizat cu sediul în Elveția cât și producătorii cu sediul în Elveția trebuie să desemneze un reprezentant autorizat cu sediul în UE.
Notificarea Comisiei Europene poate fi consultată la adresa
https://ec.europa.eu/commission/presscorner/detail/en/IP_21_2684 - Anunț important
23.07.2021
În atenția tuturor părților interesate referitor la dispozitivele de ventilație Trilogy 100, Trilogy 200, Garbin Plus, Aeris, LifeVent, BiPAP V30 şi BiPAP A30/A40 Series, precum și dispozitivele de ventilație CPAP și Bi-Level PAP, ale producătorului Philips Respironics, Inc. SUA (toate seriile fabricate anterior datei de 26 Aprilie 2021)
Ca urmare a depistării de către producătorul Philips Respironics, Inc. SUA a 2 probleme generate de spuma poliuretanică pe bază de poliester (PE-PUR), folosită la aceste dispozitive pentru amortizarea sunetului, respectiv: susceptibilitate de degradare și pătrundere în căile aeriene ale dispozitivului, de unde pot fi ingerate sau inhalate de utilizator, precum şi emisie de compuşi organici volatili toxici, Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România, în acord cu opinia producătorului și a Autorității Competente coordonatoare, cuprinsă în cele 2 Note de atenționare emise cu această ocazie, precum și în acord cu opinia European Respiratory Society (ERS), recomandă pacienților/utilizatorilor consultarea medicului / furnizorului de servicii medicale la domiciliu, anterior operării oricăror modificări în terapia prescrisă cu dispozitivele de ventilație respective.
Numai împreună cu medicul, printr-o analiză individualizată, valabilă fiecărui pacient în parte, se pot determina cele mai potrivite opțiuni pentru continuarea tratamentului și stabili în ce măsură beneficiul continuării terapiei cu dispozitivul utilizat depășește riscurile identificate de producător.
De asemenea, recomandăm pacienților să raporteze medicului / furnizorului de servicii medicale / distribuitorului sau Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România (mdevice@anm.ro) în cazul apariției unuia sau mai multor efecte adverse, care pot fi generate de utilizarea dispozitivelor de ventilație mai sus menționate și asociate celor 2 probleme identificate de producător, după cum urmează:
Riscurile potenţiale ale expunerii la particule includ iritare (piele, ochi, tract respirator), reacţie inflamatorie, durere de cap, astm, efecte adverse la alte organe (de ex., rinichi şi ficat) şi pot include inclusiv potențiale efecte toxice și cancerigene.
Riscurile potenţiale ale expunerii chimice la emisiile de compuşi organici volatili toxici includ durere de cap/ameţeală, iritare (ochi, nas, tract respirator, piele), hipersensibilitate, greaţă/vomă, potențiale efecte toxice și cancerigene.
Distribuitorii ventilatoarelor în cauză au obligația de a ține în permanență legătura cu producătorul și de a informa atât pacienții cât și medicii / furnizorii de servicii medicale la domiciliu cu privire la acțiunile propuse de producător a fi luate, în funcție de investigațiile care sunt încă în desfășurare.
Luând în considerare amploarea acestei situații, care vizează, la tipurile mai sus menționate de ventilatoare, toate seriile fabricate anterior datei de 26 Aprilie 2021, distribuitorii se vor asigura că toate ventilatoarele afectate vor fi înregistrate pe site-ul producătorului, astfel încât repararea sau înlocuirea acestora să fie luată în considerare de producător în cel mai scurt timp posibil, în beneficiul pacienților.
Linkuri utile:
https://www.philips.ro/healthcare/e/sleep/communications/src-update
https://www.ersnet.org/news-and-features/news/announcement-ers-releases-statement-on-the-philips-recall-notice/ - Anunț important
21.07.2021
În atenția operatorilor economici care desfășoară activitate de import, distribuție și/sau instalare/mentenanță dispozitive medicale
Lista furnizorilor de instruire având ca tematică legislația în domeniul dispozitivelor medicale
Conform OMS nr. 566/2020 pentru aprobarea Normelor metodologice de aplicare a titlului XX din Legea nr. 95/2006 privind reforma în domeniul sănătății, referitoare la avizarea activităților în domeniul dispozitivelor medicale, pentru obținerea avizului de funcționare, operatorul economic trebuie să dispună de personal suficient și calificat/instruit pentru activitatea pe care o desfășoară/domeniul în care activează.
Persoana responsabilă de conformitatea cu reglementările specifice domeniului dispozitivelor medicale și șeful de depozit trebuie să facă dovada participării la cursuri de instruire având ca tematică legislația în domeniul dispozitivelor medicale.
Art. 9, alin. (3) al OMS nr. 566/2020, mai sus menționat, prevede următoarele:
(3) Cursurile de instruire vor fi efectuate de către persoane fizice autorizate și persoane juridice care au în obiectul de activitate prestarea instruirilor prevăzute la alin. (2) lit. b) și care fac dovada experienței profesionale în activități de reglementare sau de evaluare a conformității dispozitivelor medicale astfel:
a) în activități de reglementare cu experiență profesională de cel puțin patru ani în domeniul dispozitivelor medicale sau participarea în cadrul grupurilor de lucru specifice domeniului dispozitivelor medicale la nivelul Comisiei Europene/Consiliului Uniunii Europene;
b) în activități de evaluare a conformității dispozitivelor medicale în cadrul unui organism de evaluare a conformității notificat pe directivele specifice dispozitivelor medicale, cel puțin doi ani.
De la apariția OMS 566/2020 până în prezent ANMDMR a luat legătura cu firmele care au emis diplome/certificate ca urmare a susținerii unor cursuri de instruire având ca tematică legislația în domeniul dispozitivelor medicale și pe care le-am regăsit în dosarele depuse de operatorii economici în vederea avizării activității desfășurate. În baza procedurii interne de lucru, așa cum este specificat la art. 7 al OMS 566/2020, s-au solicitat dovezile îndeplinirii cerințelor art. 9, alin. (3) de către lectorii utilizați pentru susținerea acestor cursuri.
Până la data publicării acestui anunț, firmele care au făcut dovada îndeplinirii acestor cerințe sunt următoarele:Nr. crt. Denumire persoană juridică 1. MEDICAL DEVICE CONSULTING SERVICES SRL 2. MEDTECH CONSULTING SRL 3. MEDICAL DEVICE LEX SRL 4. MEDIA KOMPASS SRL 5. CERTINSPECT REGISTER SRL 6. ASOCIAȚIA DE STANDARDIZARE DIN ROMÂNIA – ASRO 7. MEDICAL DEVICE TRAINING SRL În momentul în care lista va suporta modificări, vom publica deîndată revizuirea acesteia. În acest sens, vă rugăm să consultați în permanență site-ul ANMDMR pentru informații actualizate.
- Anunț important
20.07.2021
În atenția producătorilor români de dispozitive medicale/reprezentanților autorizați
Înregistrarea „Legacy devices” în EUDAMED
„Legacy devices” sunt definite ca dispozitive medicale, dispozitive medicale implantabile active și dispozitive medicale pentru diagnostic in vitro care sunt acoperite de un certificat de conformitate CE valabil emis în conformitate cu Directiva 93/42/CEE, Directiva 90/385/CEE sau Directiva 98/79/CE și care continuă să fie introduse pe piață după data aplicării Regulamentul (UE) 2017/745 (MDR) sau Regulamentul 2017/746 (IVDR).
„Legacy devices” sunt supuse cerințelor de înregistrare MDR sau IVDR, cu unele excepții, cum ar fi atribuirea unui UDI-DI de bază și a unui UDI-DI.
Producătorii vor avea posibilitatea de a înregistra oricare dintre „legacy devices” în EUDAMED. Indicații privind înregistrarea „Legacy devices” în EUDAMED sunt furnizate în documentul „MDCG 2019-5 Registration of legacy devices in EUDAMED April 2019“ (https://ec.europa.eu/docsroom/documents/34922).
Chiar dacă atribuirea unui UDI-DI de bază și UDI-DI nu este necesară pentru un „legacy device”, pentru a păstra aceeași structură standard și elemente de identificare pentru toate dispozitivele înregistrate în EUDAMED, un element de identificare EUDAMED DI (echivalentul UDI-DI de bază) va fi necesar și un ID EUDAMED (în cazul în care nu a fost atribuit niciun UDI-DI) va fi generat din EUDAMED DI.
UDI-DI de bază nu va fi niciodată aplicabil și atribuit unui „legacy device”, doar EUDAMED DI.
UDI-DI poate fi utilizat pentru a identifica un dispozitiv vechi în EUDAMED, însă un singur identificator de dispozitiv va fi atribuit unui „legacy device” astfel:
• fie un UDI-DI (unde EUDAMED DI este generat automat),
• fie un EUDAMED DI (unde ID-ul EUDAMED este generat automat).
Pentru mai multe informații vă recomandăm să parcurgeți documentul “Management of Legacy Devices – MDR EUDAMED” disponibil la linkul: https://ec.europa.eu/health/sites/default/files/md_eudamed/docs/legacy_dvc_management_en.pdf - Anunț important
20.07.2021
În atenția persoanelor interesate
Vă informăm că începând cu data de 11 iunie 2021 Ordinul ministrului sănătății nr. 1.009/2016 privind înregistrarea dispozitivelor medicale în baza națională de date a fost abrogat (cu excepția prevederilor art. 4 lit. b), art. 5, art. 7 alin. (1)-(3), art. 8, art. 12, art. 13, anexei nr. 1 și anexei nr. 4), conform Art. 33 din Ordonanța de urgență nr. 46 din 9 iunie 2021 privind stabilirea cadrului instituțional și a măsurilor pentru punerea în aplicare a Regulamentului (UE) 2017/745 al Parlamentului European și al Consiliului din 5 aprilie 2017 privind dispozitivele medicale, de modificare a Directivei 2001/83/CE, a Regulamentului (CE) nr. 178/2002 și a Regulamentului (CE) nr. 1.223/2009 și de abrogare a Directivelor 90/385/CEE și 93/42/CEE ale Consiliului,
Prin urmare, producătorii, reprezentanții autorizați ai producătorilor, importatorii sau distribuitorii stabiliți în România sau în orice alt Stat Membru nu mai au obligaţia să notifice ANMDMR punerea în funcţiune pe teritoriul României a următoarelor tipuri de dispozitive medicale (formularul F3):
– dispozitive medicale din clasele IIa, IIb şi III;
– dispozitive medicale pentru diagnostic in vitro care fac obiectul anexei nr. 2 la Hotărârea Guvernului nr. 798/2003, cu modificările şi completările ulterioare;
– dispozitive medicale pentru diagnostic in vitro de autotestare;
– dispozitive medicale implantabile active
Potrivit Regulamentului (UE) 2017/745 privind dispozitivele medicale, dispozitivele ar trebui, ca regulă generală, să poarte marcajul CE, pentru a indica faptul că sunt conforme cu prezentul regulament, astfel încât acestea să poată circula liber în interiorul Uniunii și să poată fi puse în funcțiune în conformitate cu scopul propus.
Statele membre ar trebui să nu genereze obstacole în calea introducerii pe piață sau a punerii în funcțiune a dispozitivelor care sunt conforme cu cerințele prevăzute de prezentul regulament. - Anunț important
07.06.2021
În atenția producătorilor români de dispozitive medicale/ reprezentanților autorizați
Nomenclatorul european al dispozitivelor medicale (EMDN)
Vă informăm că incepând cu 04.05.2021, nomenclatorul dispozitivelor medicale (EMDN), așa cum este definit de articolul 26 din Regulamentul (UE) 2017/745 privind dispozitivele medicale (MDR) și articolul 23 din Regulamentul (UE) 2017/746 privind dispozitivele medicale de diagnostic in vitro (IVDR), platforma sa și consultarea de validare a traducerii în limba engleza sunt oficial online și pot fi accesate la adresa https://webgate.ec.europa.eu/dyna2/emdn/.
Versiunea italiană a nomenclatorului este considerată finală și oficială. Versiunea în limba engleză face obiectul validării prin intermediul acestei consultări online, timp de o lună.
EMDN este utilizat de producători pentru înregistrarea dispozitivelor medicale în EUDAMED, unde va fi asociat fiecărui identificator unic de dispozitiv – identificator de dispozitiv (UDI-DI). EMDN este destinat să sprijine toți actorii în activitățile lor în cadrul MDR / IVDR și oferă descrieri cheie ale dispozitivelor medicale.
EMDN se caracterizează prin structura sa alfanumerică care este stabilită într-un arbore ierarhic pe mai multe niveluri. Acesta grupează dispozitivele medicale în trei niveluri principale. Primul nivel ierarhic este nivelul „Categorie”, al doilea este nivelul „Grup”, iar al treilea este nivelul „Tip”.
Fiecare dispozitiv medical este clasificat printr-un cod alfanumeric care conține o literă referitoare la „Categorie”, 2 numere care se referă la „Grup” și între 1 și 5 numere din două cifre care se referă la „Tip”, până la maximum 7 niveluri de detaliu.
Există 22 de categorii pentru primul nivel ierarhic „Categorie”. Fiecare este identificat printr-o literă a alfabetului. Fiecare categorie include dispozitive reglementate în MDR sau IVDR. Categoriile sunt împărțite în 8 categorii anatomice.
Al doilea nivel ierarhic „Grup” conține 146 grupuri de dispozitive medicale anatomice / funcționale. Acestea reprezintă diferențierile pentru a face distincția între dispozitivele din aceste categorii și sunt identificate prin numere din două cifre de la 01 la 99 pentru fiecare categorie. Numărul 90 identifică grupurile de dispozitive care posedă diverse caracteristici care nu sunt legate de grupurile existente, în timp ce numărul 99 („altele”) este rezervat dispozitivelor medicale care nu sunt incluse în grupurile deja existente și vor fi clasificate în actualizările ulterioare.
„Tipul” constituie al treilea nivel ierarhic. Se poate extinde până la 7 niveluri de detaliu, fiecare definit în cod printr-un număr din două cifre. Fiecare nivel de tip include dispozitive medicale caracterizate printr-o afinitate mare de utilizare, utilizarea intenționată sau o metodă clinică similară.
În ceea ce privește accesoriile, fiecare accesoriu va moșteni codul de clasificare EMDN al dispozitivului medical cu care este asociat. Dacă accesoriul poate fi utilizat cu mai multe dispozitive aparținând diferitelor grupuri, acestuia i se va atribui codul tipului predominant.
Deși EUDAMED nu este încă total funcțional, implementarea primului modul privind înregistrarea actorilor a început în decembrie 2020, în timp ce al doilea modul privind înregistrarea UDI a fost anunțat pentru septembrie 2021. Prin urmare, producătorii sunt sfătuiți să înceapă deja pregătirea pentru aceste cerințe de înregistrare EUDAMED pentru a fi gata să trimită informațiile solicitate imediat ce diferitele module ale bazei de date vor deveni operaționale. - Anunț important
24.05.2021
În atenția tuturor părților interesate
ANMDMR informează toate părțile interesate faptul că începând de la data prezentului anunț, toate informările privind certificatele falsificate sau copiile falsificate ale unor certificate de conformitate CE emise de Organisme Notificate pentru producători de dispozitive medicale, depistate pe piața UE, se vor posta pe site-ul ANMDMR, exclusiv în secțiunea Certificate de conformitate CE falsificate / Copii falsificate ale unor certificate de conformitate CE emise de Organisme Notificate.
De asemenea pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut vă reamintim să aveți în vedere informațiile din anunțul postat în 04.09.2020 pe site-ul nostru, în secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE și redat mai jos.
”04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Ca urmare a multiplelor informări primite de instituția noastră, potrivit cărora sunt depistate în permanență pe piața UE copii falsificate ale unor Certificate de conformitate CE emise de Organismele Notificate TÜV SÜD Product Service GmbH, Germania (0123) și TÜV Rheinland LGA Products GmbH, Germania (0197) sau care se pretind a fi emise de aceste Organisme Notificate, mai ales ca urmare a crizei generate de pandemia COVID-19, venim, în sprijinul părților interesate, cu următoarele clarificări:
1. Un Certificat de conformitate CE intrat în posesia unui operator economic sau prezentat de un operator economic unei unități sanitare contractante (ex. în cadrul unei licitații publice) și nominalizat într-un anunț postat în secțiunea Anunțuri importante – dispozitive medicale de pe site-ul ANMDMR poate fi valid doar în condițiile în care acel certificat se regăsește cu informații identice în baza de date cu certificatele emise, disponibilă pe site-ul Organismului Notificat respectiv (0123 sau 0197), baze de date care pot fi consultate accesând link-urile:
TÜV SÜD Product Service GmbH, Germania (0123) – Baza de date cu certificatele emise
https://www.tuvsud.com/de-de/dienstleistungen/produktpruefung-und-produktzertifizierung/zertifikatsdatenbank
(criteriu de căutare al doilea grup de cifre din numărul de certificat – ex. 068194 – pentru anunțul postat în 04.08.2020).
TÜV Rheinland LGA Products GmbH, Germania (0197) – Baza de date cu certificatele emise
https://www.certipedia.com/ (criteriu de căutare al doilea grup de cifre din numărul de certificat – ex. 60131859 – pentru anunțul postat în 30.04.2020).
2. Întrucât au fost depistate multiple modalități de falsificare a unui certificat, în condițiile în care Certificatul de conformitate CE nominalizat în anunțul ANMDMR se regăsește ca fiind valid în baza de date a respectivului Organism Notificat (menționată la pct. 1), pentru identificarea elementelor care încadrează o copie a acelui certificat în categoria celor falsificate, se va consulta baza de date cu certificatele falsificate a respectivului Organism Notificat, respectiv:
TÜV SÜD Product Service GmbH, Germania (0123) – Baza de date cu certificatele falsificate
https://www.tuvsud.com/de-de/dienstleistungen/produktpruefung-und-produktzertifizierung/zertifikatsdatenbank/tuev-sued-pruefzeichen/liste-gefaelschter-zertifikate
TÜV Rheinland LGA Products GmbH, Germania (0197) – Baza de date cu certificatele falsificate
https://www.tuv.com/world/en/black-list/
3. În condițiile în care Certificatul de conformitate CE nominalizat în anunțul ANMDMR nu se regăsește încă în baza de date cu certificatele falsificate a respectivului Organism Notificat (menționată la pct. 2), actualizarea acesteia fiind responsabilitatea exclusivă a acelui Organism (în conformitate cu procedurile proprii), recomandăm părților interesate să solicite clarificări de la Organismul Notificat emitent, referitor la validitatea copiei de Certificat de conformitate CE deținute.”
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
24.05.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
ANMDMR atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Thermometer, Pulse Oximeter, signs Monitor, Multiparameter Patient Monitor, fabricate de producătorul HEYUAN LEYUAN INTELLIGENT TECHNOLOGY CO.,LTD, China, dacă au intrat în posesia Certificatului de conformitate CE falsificat nr. G1 076561 0010 Rev.00, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123) la data de 2020-03-02, valabil până la data de 2024-05-26.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul ANMDMR la Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul ANMDMR pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
21.05.2021
În atenția unităților sanitare
Ca urmare a evenimentelor recent survenite cu implicarea sistemelor de distribuție a gazelor medicale (SDGM), ANMDMR aduce la cunoștința unităților sanitare, utilizatorii acestor sisteme de distribuție, obligațiile care le revin și care, dacă sunt îndeplinite, pot preveni apariția în viitor a incidentelor anterior menționate.
descarca documentul…
- Anunț important
21.05.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
ANMDMR atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Sterile Gauze Swab with/without X-Ray, Sterile Lap Sponge with/without X-Ray, Sterile Lap Sponge with Barium Strip, Sterile Gauze Ball with/without X-Ray, Infusion Set for Single Use(with Needle), Sterile Hypodermic Syringe for Single Use(with Needle), Disposable Sterile Hypodermic Needle, Oxygen Mask, Nebulizer Mask, Latex Surgical Gloves, fabricate de producătorul Shaoxing Medply Medical Products Co. Ltd., China, dacă au intrat în posesia unei copii falsificate a Certificatului de conformitate CE nr. G2 093943 0003 Rev.01 emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123) la data de 2021-02-14, valabil până la data de 2023-02-13.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul ANMDMR la Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
21.05.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
ANMDMR atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Surgical Drape, Surgical Gown, Surgical Pack, Latex Examination Glove, Nitrile Examination Glove, Medical Face Mask, Medical Cap, Medical Shoe Cover, Vaginal Speculum, fabricate de producătorul HeNan YADU Industrial Co., Ltd., China, dacă au intrat în posesia unei copii falsificate a Certificatului de conformitate CE nr. G2S 104411 0002 Rev. 00 emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123) la data de 2019-11-08, valabil până la data de 2024-05-26.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul ANMDMR la Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
21.05.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
ANMDMR atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Nitrile examination gloves, fabricate de producătorul Guangzhou Pidegree Medical Technology Co., Ltd., China, dacă au intrat în posesia Certificatului de conformitate CE falsificat nr. 6706GB415100225, care ar fi emis de Organismul Notificat MEDCERT Zertifizierungs- und Prüfungsgesellschaft für die Medizin GmbH, Germania (0482) la data de 2020-02-25, valabil până la data de 2025-11-09, în conformitate cu Anexa II – Essential Requirements according to the PPE-Directive 89/686/EEC.
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul ANMDMR pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
20.05.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de orice tip, dacă intră în posesia unui Certificat de conformitate CE care ar fi emis de 3EC International Certifications Private Limited, India sub numărul de identificare 2265, număr care aparține de drept Organismului Notificat 3EC International a.s., Slovacia.
Potrivit Organismului Notificat 3EC International a.s., Slovacia, nu există nicio legatură între acest Organism și 3EC International Certifications Private Limited, India.
Puteți verifica aceste informații și consultând site-ul Organismului Notificat 2265:
https://www.3ec.sk/en
Anunt postat în 11.05.2021 sub numele Information about 3EC International trade name misuse
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare - Anunț important
18.05.2021
În atenția persoanelor interesate
Sistemul unic de identificare a dispozitivelor (UDI) în conformitate cu Regulamentele UE 2017/745 și 2017/746 privind dispozitivele medicale.
descarca documentul…
- Anunț important
13.05.2021
În atenția operatorilor economici care desfășoară activitate de import, distribuție și/ sau instalare/mentenanță dispozitive medicale
Lista furnizorilor de instruire având ca tematică legislația în domeniul dispozitivelor medicale, agreați de ANMDMR
Conform OMS nr. 566/2020 pentru aprobarea Normelor metodologice de aplicare a titlului XX din Legea nr. 95/2006 privind reforma în domeniul sănătății, referitoare la avizarea activităților în domeniul dispozitivelor medicale, pentru obținerea avizului de funcționare, operatorul economic trebuie să dispună de personal suficient și calificat/instruit pentru activitatea pe care o desfășoară/domeniul în care activează.
Persoana responsabilă de conformitatea cu reglementările specifice domeniului dispozitivelor medicale și șeful de depozit trebuie să facă dovada participării la cursuri de instruire având ca tematică legislația în domeniul dispozitivelor medicale.
Art. 9, alin. (3) al OMS nr. 566/2020, mai sus menționat, prevede următoarele:
(3) Cursurile de instruire vor fi efectuate de către persoane fizice autorizate și persoane juridice care au în obiectul de activitate prestarea instruirilor prevăzute la alin. (2) lit. b) și care fac dovada experienței profesionale în activități de reglementare sau de evaluare a conformității dispozitivelor medicale astfel:
a) în activități de reglementare cu experiență profesională de cel puțin patru ani în domeniul dispozitivelor medicale sau participarea în cadrul grupurilor de lucru specifice domeniului dispozitivelor medicale la nivelul Comisiei Europene/Consiliului Uniunii Europene;
b) în activități de evaluare a conformității dispozitivelor medicale în cadrul unui organism de evaluare a conformității notificat pe directivele specifice dispozitivelor medicale, cel puțin doi ani.
De la apariția OMS 566/2020 până în prezent ANMDMR a luat legătura cu firmele care au emis diplome/certificate ca urmare a susținerii unor cursuri de instruire având ca tematică legislația în domeniul dispozitivelor medicale și pe care le-am regăsit în dosarele depuse de operatorii economici în vederea avizării activității desfășurate. În baza procedurii interne de lucru, așa cum este specificat la art. 7 al OMS 566/2020, s-au solicitat dovezile îndeplinirii cerințelor art. 9, alin. (3) de către lectorii utilizați pentru susținerea acestor cursuri.
Până la data publicării acestui anunț, firmele care au făcut dovada îndeplinirii acestor cerințe sunt următoarele:Nr. crt. Denumire persoana juridica Nume, prenume lector 1 MEDICAL DEVICE CONSULTING SERVICES SRL LAZĂR IORDACHE 2 MEDTECH CONSULTING SRL MARGARETA MIHALACHE 3 MEDICAL DEVICE LEX SRL LAZĂR IORDACHE 4 MEDIA KOMPASS SRL NICOLAE FOTIN 5 CERTINSPECT REGISTER SRL GHEORGHE NEAGU 6 ASOCIAȚIA DE STANDARDIZARE DIN ROMÂNIA – ASRO MARGARETA MIHALACHE În momentul în care lista va suporta modificări, vom publica deîndată revizuirea acesteia. În acest sens, vă rugăm să consultați în permanență site-ul ANMDMR pentru informații actualizate.
- Anunț important
10.05.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Sterile Hypodermic Syringe for Single Use – Type: Hypodermic Syringe, Safety Syringe and Insulin Syringe, fabricate de de producătorul International Company for Medical Necessities (I.CO), Egipt, pentru care a fost depistată pe piața UE o copie falsificată a Certificatului de conformitate CE nr. 2020-MDD/QS-107, emis de Organismul Notificat 3EC International a.s., Slovacia (2265) la data de 2020-08-12, valabil până la data de 2024-05-26.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile disponibile pe site-ul Organismului Notificat 3EC International a.s., Slovacia, accesând linkurile:
https://www.3ec.sk/en/services/falsificates/
https://www.3ec.sk/en/services/suspension-or-withdrawal-of-certification/
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
10.05.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Sterile Medical Syringes with Needles (Size: 1 ml, 3 ml (Infant), 3 ml (Adult), 5 ml, 10 ml), fabricate de de producătorul SAS Co. for Syringes Manufacturing, Egipt, pentru care a fost depistată pe piața UE o copie falsificată a Certificatului de conformitate CE nr. 2018-MDD/QS-011, emis de Organismul Notificat 3EC International a.s., Slovacia (2265) la data de 2018-06-13, valabil până la data de 2023-06-12.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile disponibile pe site-ul Organismului Notificat 3EC International a.s., Slovacia, accesând linkurile:
https://www.3ec.sk/en/services/falsificates/
https://www.3ec.sk/en/services/suspension-or-withdrawal-of-certification/
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
21.04.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Hy-Silk™ Light, Hy-Silk™ Deep, Hy-Silk™ Ultra Deep, respectiv Crosslinked Hyaluronic Acid With Lidocaine With provision for Inclusion of Biocompatible Materials less than 2% Weight, fabricate de producătorul +Biio-P Pharmaceutical Manufacturing, Coreea, dacă au intrat în posesia Certificatelor de conformitate CE falsificate nr. 1434-MDD-327/2020 și respectiv nr. 1434-MDD-328/2020, care ar fi emise de Organismul Notificat Polish Centre for Testing and Certification, Polonia (1434), valabile de la data de 27.08.2020 până la data de 27.05.2024.
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
21.04.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Sterile Gauze Swab with/without X-Ray, Sterile Lap Sponge with/without X-Ray, Sterile Lap Sponge with Barium Strip, Sterile Gauze Ball with/without X-Ray, Infusion Set for Single Use(with Needle), Sterile Hypodermic Syringe for Single Use(with Needle), Disposable Sterile Hypodermic Needle, Oxygen Mask, Nebulizer Mask, Latex Surgical Gloves fabricate de producătorul Shaoxing Medply Medical Products Co. Ltd., China, dacă au intrat în posesia Certificatului de conformitate CE falsificat nr. G2 093943 0003 Rev.01 care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123), valabil de la data de 2021-02-14 până la data de 2023-02-13.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România la Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
12.04.2021
În atenția persoanelor interesate
Comisia Europeana a facut public în 18.02.2021 (https://ec.europa.eu/commission/presscorner/detail/en/mex_21_682) comunicatul EU Health Security Committee (HSC) prin care este agreată o listă cu testele rapide antigen de determinare a COVID – 19 care conține și testele ale căror rezultate sunt recunoscute mutual și un set comun de date standardizate ce vor fi incluse în certificatele care conțin rezultatele testelor COVID-19. Acest document a fost întocmit în urma Recomandării Consiliului din 20.01.2021 și nu are un caracter obligatoriu (https://data.consilium.europa.eu/doc/document/ST-5451-2021-INIT/en/pdf).
Documentul conține în primul rând o listă comună (Anexa I) cu testele rapide de tip antigen pentru determinarea COVID-19 ce sunt considerate a fi adecvate pentru utilizare în situațiile și contextele menționate la punctul 6 din Recomandarea Consiliului din 20.01.2021.
Dintre testele Anexei I au fost selectate 16 teste antigenice rapide ale căror rezultate sunt recunoscute reciproc de către statele membre.
În anunțul postat pe pagina Comisiei Europene se evidențiază faptul că testele rapide de antigen sunt cruciale pentru încetinirea răspândirii COVID-19. Dacă se solicită sau se recomandă teste negative COVID-19 pentru desfășurarea oricărei activități, este esențial ca acestea să fie recunoscute reciproc și rezultatele testelor înscrise în certificate recunoscute în întreaga UE. Acest lucru este esențial, în special în contextul călătoriilor. Cetățenii UE au nevoie de claritate și predictibilitate.
Actualizarea listei va fi postată de către ANMDMR cu regularitate. - Anunț important
12.04.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Soft Contact Lens, fabricate de producătorul YIWU QIAOTI E-commerce CO., LTD, China, dacă au intrat în posesia Certificatului de conformitate CE falsificat nr. HD 60117242 0001, care ar fi emis pentru acest producător de Organismul Notificat TÜV Rheinland LGA Products GmbH, Germania (0197) la data de 2017-05-27, valabil până la data de 2022-03-15.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România la Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
29.03.2021
În atenția importatorilor și distribuitorilor de teste PCR și centrelor de testare COVID-19
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de teste PCR precum și centrele de testare COVID-19 că au fost depistate pe piața UE teste PCR falsificate pentru depistarea COVID-19, lot 04/2020, item 0097654236, fabricate de producătorul SHENZHEN PHARMACEUTICAL CO. LTD., China.
Dacă ați intrat în posesia acestor produse, însoțite de documentul ”EC-Declaration of Conformity for CE-Marking accordion to Council Directive 98/79/EEC” care se pretinde a fi emis de Organismul TUV Rheinland LGA Products GmbH, Germania, la finalul căruia se precizează:
Declaration of conformity: Detection Test for Coronavirus disease 2020
COVID-19 PCR RAPID TEST
GIVD CODE: 28.08.36.91
The validity with the date of issue.
August 28, 2020
pe capacul de plastic al tamponului de recoltare fiind vizibil marcajul CE 0373, nu le utilizați și sesizați Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România – Serviciul Supraveghere Piață.
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
22.03.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul ”Latex and Nitrile Surgical Powder free Glove, Sterile / Trade mark: Superieur Gloves”, fabricate de un producător cu denumire neidentificată, Route 1, Long Thanh Industrial Zone Long Thanh District, Dong Nai Province 76211, Vietnam, dacă au intrat în posesia Certificatului de conformitate CE falsificat nr. G2 0493 Rev. 03, care ar fi emis Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123), valabil de la data de 2020-02-19 până la data de 2024-07-28.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din Româniala Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
11.03.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Cross-linked Hyaluronic Acid Dermal Filler with PDRN, pentru care a fost depistată pe piața UE o copie falsificată a Certificatului de conformitate CE nr. 2017-MDD/QS-044, emis de Organismul Notificat 3EC International a.s., Slovacia (2265) la data de 2017-10-02, valabil până la data de 2022-10-01.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile disponibile pe site-ul Organismului Notificat 3EC International a.s., Slovacia, accesând linkurile:
https://www.3ec.sk/en/services/falsificates/
https://www.3ec.sk/en/services/suspension-or-withdrawal-of-certification/
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
03.03.2021
În atenția persoanelor interesate
Referitor la comercializarea testelor rapide de detecție a antigenelor SARS Cov-2, ANMDMR revine asupra adresei publicate pe site, pe data de 25.11.2020 cu următoarele clarificări:
În urma unei reevaluări a încadrării acestor dispozitive medicale, Ministerul Sănătății, Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România și Colegiul Farmaciștilor din România consideră testele rapide pentru depistarea infecției cu SARS – CoV- 2 ca fiind permise a fi comercializate cu amănuntul, prin farmaciile comunitare.
Având în vedere instrucțiunile de utilizare ale producătorului, este obligatoriu ca eliberarea testelor rapide să fie însoțită de avertismentul: „Prelevarea probelor și interpretarea rezultatelor trebuie facută doar de către personal medico-sanitar calificat”. - Anunț important
26.02.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Protective Clothing & Equipment, Sterile NaCl-solutions – Physical acting products for the treatment of gastro-intestinal disorders – Physical acting products for the treatment of topical applications – Products for the treatment of dry eyes – Products for the treatment of vaginal disorders – Products for alleviation of haemorrhoidal disorders – Products for the treatment of sore throat, dry cough and hoarseness – Physically acting products for the application on mucous membranes, fabricate de producătorul Medi-Inn GmbH, Germania, dacă au intrat în posesia Certificatului de conformitate CE falsificat nr. 3558GB414200519, care ar fi emis pentru acest producător de Organismul Notificat MEDCERT Zertifizierungs- und Prüfungsgesellschaft für die Medizin GmbH, Germania (0482), la data de 2020-05-19, valabil până la data de 2024-05-27.
Deținătorul de drept al certificatului de conformitate CE nr. 3558GB414200519, emis de Organismul Notificat MEDCERT Zertifizierungs- und Prüfungsgesellschaft für die Medizin GmbH, Germania (0482) la data de 2020-05-19, valabil până la data de 2024-05-27, este producătorul Hälsa Pharma GmbH, Germania, pentru dispozitivele medicale de tipul Isotonic NaCl-solutions – Sterile NaCl-solutions – Physical acting products for the treatment of gastro-intestinal disorders – Physical acting products for the treatment of topical applications – Products for the treatment of dry eyes – Products for the treatment of vaginal disorders – Products for alleviation of haemorrhoidal disorders – Products for the treatment of sore throat, dry cough and hoarseness – Physically acting products for the application on mucous membranes.
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
26.02.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Laser therapy devices – Laser probes, Pulsewave blood pressure monitors, fabricate de producătorul SHENZHEN AFKMED CO., LTD., China, dacă au intrat în posesia Certificatului de conformitate CE falsificat nr. 7120GB410201209A, care ar fi emis pentru acest producător de Organismul Notificat MEDCERT Zertifizierungs- und Prüfungsgesellschaft für die Medizin GmbH, Germania (0482), la data de 2020-12-09, valabil până la data de 2024-05-27.
Deținătorul de drept al certificatului de conformitate CE nr. 7120GB410201209A, emis de Organismul Notificat MEDCERT Zertifizierungs- und Prüfungsgesellschaft für die Medizin GmbH, Germania (0482) la data de 2020-12-09, valabil până la data de 2024-05-27, este producătorul Shenzhen Raycome Health Technology Co., China.
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
23.02.2021
În atenția persoanelor interesate
NOU! Posturi vacante la ANMDMR
Având în vedere prevederile art. 9, din Ordinul ministrului sănătăţii nr. 1.839/30.10.2020, privind modificarea Ordinului ministrului sănătăţii nr. 905/2020 pentru aprobarea Metodologiei privind ocuparea, fără concurs, a posturilor vacante sau temporar vacante din cadrul Ministerului Sănătăţii şi unităţilor aflate în subordinea, coordonarea şi sub autoritatea Ministerului Sănătăţii, inclusiv funcţiile publice de execuţie şi conducere, pe perioadă determinată, în contextul instituirii stării de alertă pe teritoriul României, conform art. 11 din Legea nr. 55/2020 privind unele măsuri pentru prevenirea şi combaterea efectelor pandemiei de COVID-19, Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România organizează ocuparea fără concurs a mai multor posturi vacante de execuție. LISTA COMPLETĂ ANUNȚURI - Anunț important
19.02.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul ”Non Sterile Latex Surgical Gloves(Powdered & Powder Free)Latex Examination Gloves( Powdered & Powder Free), Nitrile Examination Gloves( Powdered & Powder Free), Plastic Gloves, Vinyl Gloves, Household Gloves, Disposable Mask, Cap, Apron, Gowns, Shoe cover & Leggings”, fabricate de producătorul John Holbert Medical Holding, Polonia, dacă au intrat în posesia Certificatului de conformitate CE falsificat nr. G2S 12 03 62218 009, care ar fi emis Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123), valabil de la data de 2020-03-21 până la data de 2023-04-17.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România la Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
11.02.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Termometre cu infraroșu Pykori modelele PKR-T1, PKR-T2, PKR-T3, PKR-T4, fabricate de producătorul Anhui Paikerui Medical Equipment Co., Ltd, China, dacă au intrat în posesia documentului falsificat Review Report no. 0H200323S.APM0D78, care ar fi emis de Organismul Notificat ECM – Ente Certificazione Macchine, Italia (1282) la data de 23 Martie 2020, valabil până la data de 22 Martie 2025, pentru produsele Infrared Termometer (Not Sterile), modele: PKR-T1, PKR-T2, PKR-T3, PKR-T4.
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
05.02.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Disposable safety syringe with hypodermic needle, disposable auto-disable syringe with hypodermic needle, disposable sterile syringe with hypodermic needle, disposable insulin syringe, disposable safety insulin syringe, insulin pen needle and disposable hypodermic needle, fabricate de producătorul Shanghai Sol-Millennium Medical Products Co., Ltd., China, dacă au intrat în posesia Certificatului de conformitate CE falsificat nr. 4614GB414121205, care ar fi emis Organismul Notificat MEDCERT Zertifizierungs- und Prüfungsgesellschaft für die Medizin GmbH, Germania (0482) la data de 2017-12-07, valabil până la data de 2022-11-11.
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
26.01.2021
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Sterile Surgical Gloves, fabricate de producătorul Woodex Company limited, Thailanda, dacă au intrat în posesia Certificatului de conformitate CE falsificat nr. DD 60076256 0001, care ar fi emis Organismul Notificat TÜV Rheinland LGA Products GmbH, Germania (0197), valabil de la data de 2019-06-14 până la data de 2021-06-13.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din Româniala Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
14.01.2021
În atenția persoanelor interesate
Impactul BREXIT asupra operatorilor economici cu activitate în domeniul distribuției de dispozitive medicale
Începând cu 1 ianuarie 2021, Regatul Unit al Marii Britanii este considerat THIRD STATE- țară terță. Începând cu această dată i se aplică prevederile oricărui alt stat din afara Uniunii Europene.
Dacă producătorii, reprezentanții autorizați sau distribuitorii / furnizorii doresc să introducă în continuare dispozitive medicale certificate pe piața UE-27 după Brexit, trebuie luate în considerare următoarele aspecte:
1. Producătorii și reprezentanții autorizați care introduc pe piață dispozitive medicale care sunt certificate de organismele notificate din Regatul Unit vor trebui să se asigure că certificatele au fost transferate la un organism notificat UE-27 înainte de data retragerii.
Certificatele de conformitate CE emise de organismele Notificate din Regatul Unit nu mai sunt valabile pentru introducerea pe piață a dispozitivelor medicale, chiar dacă evaluarea a fost efectuată înainte de 1 ianuarie 2021, cu excepția cazului în care dispozitivele au fost deja introduse pe piața UE înainte de 1 ianuarie 2021.
Dacă dispozitivele medicale au fost introduse pe piața UE înainte de 1 ianuarie 2021, în conformitate cu termenii Acordului de retragere, acestea pot rămâne pe piața UE. Producătorii, importatorii sau distribuitorii trebuie să dovedească momentul încheierii tranzacției.
2. Producătorii care au desemnat un reprezentant autorizat din Regatul Unit trebuie să desemneze un reprezentant autorizat din UE-27.
Reprezentanții autorizați din Regatul Unit nu mai sunt recunoscuți în UE-27. Aceasta înseamnă că nu sunt capabili să îndeplinească sarcini în numele producătorului în scopul introducerii dispozitivelor pe piața UE-27.
Atât producătorii cu sediul în afara UE care aveau desemnat până în prezent un reprezentant autorizat cu sediul în Regatul Unit cât și producătorii din Regatul Unit trebuie să desemneze un reprezentant autorizat cu sediul în UE.
Va fi necesară notificarea Autorităților Competente din Statele Membre UE în care reprezentantul autorizat are sediul (conform Art. 14 (1) si (2) din MDD – Directiva 93/42/EEC pentru dispozitive medicale; Art. 10a (2) din AIMD – Directiva 90/385/EEC pentru dispozitive medicale implantabile active; Art. 10 (3) din IVDD – Directiva 98/79/EC pentru dispozitive medicale pentru diagnostic in vitro).
3. Regatul Unit devenind țară non-UE, dispozitivele medicale care provin din Regatul Unit vor fi considerate import, cu toate implicațiile aferente.
Operatorii economici care în prezent sunt distribuitori pentru dispozitive medicale ale producătorilor din Regatul Unit vor deveni importatori. Același lucru va fi valabil pentru dispozitivele medicale venite din țări non-UE și introduse pentru prima dată pe piața din UK.
4. Dispozitivele medicale introduse pe piața din Regatul Unit și puse în funcțiune (vândute deja) pe piața UE-27 înainte, de la data retragerii Regatului Unit, când ajung pe piața UE-27 vor fi considerate a fi o nouă introducere pe piață.
Legendă:
UE-27 = statele membre ale Uniunii Europene, mai puțin Regatul Unit
Informațiile vor fi actualizate în conformitate cu noile acorduri care vor fi încheiate între Regatul Unit și UE-27. - Anunț important
12.01.2021
În atenția producătorilor români de dispozitive medicale/ reprezentanților autorizați / importatorilor
Utilizarea modulului de înregistrare a “actorilor” din EUDAMED și a numărului unic de înregistrare (SRN)
Crearea unei baze de date europene privind dispozitivele medicale (EUDAMED) este unul dintre aspectele cheie ale noilor regulamente privind dispozitivele medicale (Regulamentul (UE) 2017/745) și dispozitivele medicale de diagnostic in vitro (Regulamentul (UE) 2017/746).
EUDAMED va oferi o imagine reală a ciclului de viață al dispozitivelor medicale puse la dispoziție în Uniunea Europeană (UE). Acesta va integra diferite sisteme electronice pentru a strânge și prelucra informații despre dispozitive medicale și companii conexe (de exemplu, producători). În acest sens, EUDAMED își propune să sporească transparența generală, inclusiv printr-un acces mai bun la informații pentru public și profesioniștii din domeniul sănătății și să consolideze coordonarea între diferitele state membre din UE.
EUDAMED este compus din șase module, după cum urmează:
1.înregistrarea actorilor,
2.identificarea unică a dispozitivului (UDI) și înregistrarea dispozitivelor medicale,
3.organisme notificate și certificate emise,
4.investigații clinice și studii de performanță,
5.vigilență
6. supravegherea pieței.
Începând cu 1 decembrie 2020 este activ modulul de înregistrare a actorilor.
În conformitate cu articolul 30 (1) al MDR, modulul de înregistrare a actorilor trebuie să permită crearea unui număr unic de înregistrare („SRN”) și culegerea și procesarea informațiilor necesare pentru identificarea producătorului (inclusiv producătorii de sisteme / pachete de proceduri) și, dacă este cazul, a reprezentantului autorizat și a importatorului. Ca atare, modulul de înregistrare a actorilor constituie o condiție prealabilă pentru utilizarea celorlalte module EUDAMED și facilitează un mod sigur de accesare a EUDAMED.
Actorii implicați în EUDAMED sunt:
• Organisme de supraveghere
– Comisia Europeană
– Autoritățile competente (AC), inclusiv autoritățile de desemnare
– Organisme notificate (NB)
• Operatori economici
– Producători
– Producătorii de pachete de sisteme și proceduri
– Reprezentanți autorizați
– Importatori
• Sponsori (finanțatori investigație clinică)
În urma evaluării și aprobării cererii de către autoritatea națională competentă în cauză (ANMDMR), EUDAMED generează SRN-ul operatorului economic către autoritatea națională competentă și îl transferă operatorului economic solicitant.
Mai multe informații găsiți la https://ec.europa.eu/health/md_eudamed/actors_registration_ro.
Ghidul care vă oferă toate informațiile necesare înregistrării actorilor în Eudamed îl puteți accesa la adresa:
https://ec.europa.eu/health/sites/health/files/md_eudamed/docs/md_user_guide_actor_module_en.pdf. - Anunț important
14.12.2020
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Respiratory device producing oxygen, fabricate de producătorul BBDS ENERJI SANAYI TICARET Ltd. Ști, Turcia, dacă au intrat în posesia Certificatului de conformitate CE falsificat nr. D1055301645, care ar fi emis Organismul Notificat mdc medical device certification GmbH, Germania (0483), valabil de la data de 2020-07-09 până la data de 2023-07-08.
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
14.12.2020
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale sterile și nesterile fabricate de producătorul Lars Qvist, Danemarca, dacă au intrat în posesia Certificatului falsificat nr. D1263400016, de conformitate cu cerințele EN ISO 374, având ca scop “production and distribution of sterile and non-sterile disposable medical devices”, certificat care ar fi emis Organismul Notificat mdc medical device certification GmbH, Germania (0483), valabil de la data de 2019-10-07 până la data de 2022-09-01.
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
07.12.2020
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Electrocardiograph, Patient Monitor, Pulse Oximeter, fabricate de producătorul CMICS Medical Instrument Co., Ltd., China, dacă au intrat în posesia Certificatului falsificat nr. G1 16 07 39561 015, care ar fi emis Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123), valabil de la data de 2016-11-08 până la data de 2021-11-07.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din Româniala Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
07.12.2020
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Latex and Nitrile Surgical Powderfree Glove, Sterile, fabricate de producătorul GLOVESCARE LIMITED., UK, dacă au intrat în posesia Certificatului falsificat nr. G2 055729 0008 Rev. 01, care ar fi emis Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123), valabil de la data de 2020-02-19 până la data de 2024-05-26.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din Româniala Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
03.12.2020
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Pulse oximeter, pocket fetal doppler, visual stethoscope, patient monitor, fetal monitor, B-ultrasound diagnostic system, ECG, ECG acquisition box, ambulatory blood pressure monitor, EEG, anaesthesia machine, ventilator, holter, electrosurgical unit, infusion pump and syringe pump, fabricate de producătorul Shanghai Sunbright Industrial Co., Ltd, China, dacă au intrat în posesia Certificatului de conformitate CE falsificat nr. 6730GB410101220, care ar fi emis de Organismul Notificat MEDCERT Zertifizierungs- und Prüfungsgesellschaft für die Medizin GmbH, Germania (0482) la data de 2014-12-20, valabil până la data de 2022-06-01.
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Comunicat de presă
25.11.2020
Ministerul Sănătății: Comunicat de presă privind utilizarea testelor rapide antigen
Testele rapide de detecție a antigenelor SARS Cov-2, la fel ca toate dispozitive medicale, trebuie utilizate în conformitate cu instrucțiunile producătorilor.
În România, testele rapide antigen sunt folosite în prezent pentru triajul simptomaticilor în unitățile de primiri urgențe și în compartimentele de primiri urgențe, având în vedere necesitatea de a descongestiona cât mai rapid, dar și în siguranță, aceste zone. Această decizie a fost adoptată conform recomandărilor OMS și ECDC și susținută de Comisia de management clinic si epidemiologic al infectiei COVID a Ministerului Sănătății.
Pentru a crește accesul populației la diagnostic, Ministerul Sănătății încurajează extinderea utilizării acestui tip de testare, dar într-un cadru reglementat, în conformitate cu recomandările organismelor internaționale OMS și ECDC și în beneficiul superior al persoanelor testate și al populației generale.
În acest context, la cererea ministrului Sănătății, Nelu Tătaru, experți din cadrul Ministerului Sănătății, ai ANMDM, INSP împreună cu reprezentanții Colegiului Farmaciștilor lucrează la adaptarea legislației naționale actuale, astfel încât comercializarea și utilizarea testelor rapide antigen să se realizeze în condiții adecvate. Noul demers legislativ va completa eventuale discontinuități ale legislației actuale, atât pentru aceste teste, cât pentru alte dispozitive medicale, în cazul în care este necesar.
“A avut loc o primă întâlnire e experților pentru identificarea soluțiilor de utilizare a testelor rapide în afara UPU/CPU, într-un cadru reglementat și adaptat. Testarea trebuie realizată în deplină siguranță pentru persoana testată și pentru ca să existe beneficiu pentru sănătatea publică, rezultatul trebuie raportat, monitorizat și cuantificat”, a declarat ministrul Tătaru.
Conform recomandărilor ECDC, testele rapide antigen au o capacitate mai redusă de a identifica persoanele bolnave, comparativ cu testarea RT –PCR și sunt recomandate pentru utilizare numai în anumite condiții și de către profesioniști. În mod particular aceste teste sunt destinate pentru a fi utilizate numai de către profesioniști, ceea ce înseamnă că se recomandă ca prelevarea probei și interpretarea rezultatelor să se facă de către personal medical calificat. Dacă testele rapide nu sunt utilizate de către profesioniști, așa cum producătorul menționează în instrucțiunile de utilizare, rezultatele pot fi compromise.
Sursa: Ministerul Sănătății - Anunț important
25.11.2020
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Latex and Nitrile Surgical Powderfree Glove, Sterile, fabricate de producătorul WITWONG, dacă au intrat în posesia unei copii falsificate a Certificatului de conformitate CE nr. G2 055729 0008 Rev. 01,emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123), valabil de la data de 2019-10-19 până la data de 2024-12-24.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din Româniala Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din Româniapentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
25.11.2020
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Patient Monitor, ECG, Pulse Oximeter, Thermometer Syringe pump, Infusion pumpfabricate de producătorul Shanghai Sunbright Industrial Co., Ltd, China, dacă au intrat în posesia unei copii falsificate a Certificatului de conformitate CE nr. G1 097976 0005 Rev. 00,emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123), valabil de la data de 2019-09-02 până la data de 2022-07-04.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din Româniala Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din Româniapentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
25.11.2020
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Digital Thermometers, Blood Pressure Monitor, Infrared Forehead Thermometer fabricate de producătorul Yangcheng Kellyunion Import and Export Co., Ltd., China, dacă au intrat în posesia unei copii falsificate a Certificatului de conformitate CE nr. G2 17 12 02927 002,emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123), valabil de la data de 2018-05-08 până la data de 2023-05-07.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din Româniala Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din Româniapentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
25.11.2020
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Lap Sponges; Sterile Gauze Sponges, Face Masks fabricate de producătorul
Nantong Jianan Medical Products Co., Ltd., China, daca au intrat in posesia unei copii falsificate a Certificatului de conformitate CE nr. DD 60133982 0001,emis de Organismul Notificat TÜV Rheinland LGA Products GmbH, Germania (0197), valabil de la data de 2018-11-15 până la data de 2023-11-03, care include aceste categorii de dispozitive medicale.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din Româniala Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din Româniapentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
13.11.2020
În atenția operatorilor economici care comercializează teste rapide pentru diagnosticul COVID-19
Testul antigen este cel mai nou tip de testare şi, în acest moment, este singurul test rapid care detectează virusul COVID-19. Acest test detectează antigeni, respectiv partea de virus pe care sistemul nostru imunitar o recunoaşte.
Testul antigen poate indica infecţia în faza acută a bolii. Acest lucru este valabil şi pentru persoanele fără simptome, dacă infecţia este activă.
Testul este de uz profesional, ceea ce înseamnă că se recomandă ca prelevarea probei și interpretarea rezultatelor să se facă de către personal medical calificat.
Art. 15 din Hotarârea de Guvern nr. 798 / 2003 privind stabilirea condiţiilor de introducere pe piaţă şi de utilizare a dispozitivelor medicale pentru diagnostic in vitro reglementează că în cazul acestor teste, în scopul aplicării marcajului CE, producătorul trebuie să urmeze procedura menţionată în anexa nr. 3 şi să emită declaraţia de conformitate CE înainte de introducerea pe piaţă a dispozitivelor.
Produsele sunt introduse pe piață în baza declarației de conformitate dată de producător.
În spaţiul media au apărut recomandări pentru utilizarea inviduală a acestor teste. Menţionăm că aceste proceduri trebuie făcute doar de persoanele care au experienţă în domeniul medical!
Atragem atenția că aceste teste nu sunt de autotestare. Testele rapide pentru autotestare au un alt regim de introducere pe piață, cu implicarea unui organism notificat care evaluează conformitatea acestor produse.
Astfel, conform art. 16,
În cazul tuturor dispozitivelor pentru autotestare, cu excepţia celor cuprinse în anexa nr. 2 şi a dispozitivelor pentru evaluarea performanţei, înainte de a emite declaraţia de conformitate menţionată la art. 15, producătorul trebuie să îndeplinească cerinţele suplimentare stabilite în anexa nr. 3 pct. 6. În locul acestei proceduri, producătorul poate aplica procedura prevăzută la art. 17 sau 18.
Anexa 3 a Hotarârii de Guvern 798/2003, pct. 6 menționează: Pentru dispozitivele pentru autotestare, producătorul trebuie să depună o cerere pentru examinarea proiectului la un organism notificat, ales în conformitate cu art. 23 din hotărâre.
Anexa 1 la Hotarârea de Guvern 798/2003, pct. 7. Cerinţe pentru dispozitivele pentru autotestare
Dispozitivele pentru autotestare trebuie să fie proiectate şi realizate conform condiţiilor de îndeplinire a scopului prevăzut, ţinându-se seama de îndemânarea şi de mijloacele disponibile ale celor care le utilizează, precum şi de influenţa care rezultă din variaţiile care pot fi raţional anticipate în priceperea utilizatorilor şi condiţiile de mediu. Instrucţiunile şi informaţiile furnizate de producător trebuie să fie uşor de înţeles şi de aplicat de către utilizator.
7.1. Dispozitivele pentru autotestare trebuie să fie proiectate şi realizate astfel încât:
a) să asigure utilizarea uşoară a dispozitivului de către utilizator în toate etapele procedurii;
b) să reducă pe cât posibil riscul erorilor de manipulare şi de interpretare a rezultatelor.
7.2. Dispozitivele pentru autotestare trebuie să prevadă, acolo unde este posibil, controlul utilizatorului, cum ar fi, de exemplu, procedura prin care utilizatorul verifică în timpul utilizării că produsul va îndeplini scopul prevăzut.
8. Informaţii furnizate de către producător
8.1. Fiecare dispozitiv trebuie să fie însoţit de informaţiile necesare pentru a identifica producătorul şi pentru a fi folosit în siguranţă, ţinându-se seama de pregătirea şi de cunoştinţele utilizatorilor potenţiali.
Aceste informaţii trebuie să apară pe etichetă şi în instrucţiunile de folosire.
8.4. Eticheta trebuie să poarte următoarele indicaţii:
…………………
k) dacă dispozitivul este destinat autotestării, acest fapt trebuie clar precizat.
8.7. Instrucţiunile de folosire trebuie să conţină următoarele:
t) specificaţii pentru dispozitivele pentru autotestare:
– rezultatele trebuie să fie exprimate şi prezentate astfel încât să fie înţelese uşor de un neprofesionist; informaţiile trebuie să fie furnizate asociat cu îndrumări pentru utilizator asupra modului de a acţiona (în caz de rezultat pozitiv, negativ sau neconcludent) şi asupra posibilităţii de rezultate fals pozitive sau fals negative;
– anumite particularităţi pot fi omise cu condiţia ca alte informaţii furnizate de producător să fie suficiente pentru a permite utilizatorului să folosească dispozitivul şi să înţeleagă rezultatele oferite de dispozitiv;
– informaţiile furnizate trebuie să includă un enunţ care să îl determine pe utilizator să nu ia nici o decizie medicală relevantă înainte de a-şi consulta medicul curant;
– informaţiile trebuie de asemenea să precizeze că, în cazul în care dispozitivul pentru autotestare este utilizat pentru monitorizarea unei afecţiuni existente, pacientul trebuie doar să-şi adapteze tratamentul dacă a fost pregătit corespunzător în acest sens;
u) data apariţiei sau a ultimei revizuiri a instrucţiunilor de utilizare.
Ca o concluzie, Anexa 1 a Hotarârii de Guvern 798/2003, CERINŢE ESENŢIALE, pct. A. Cerinţe generale menționează foarte clar:
Dispozitivele trebuie să fie proiectate şi realizate astfel încât, utilizate în condiţiile şi pentru scopul propus, să nu compromită, direct sau indirect, starea clinică ori siguranţa pacienţilor, siguranţa şi sănătatea celor care le utilizează sau, acolo unde este cazul, a altor persoane ori siguranţa proprietăţii.
Atât timp cât testele rapide nu sunt utilizate de către profesioniști, așa cum producătorul menționează în instrucțiunile de utilizare, rezultatele pot fi compromise.
Distribuția dispozitivelor medicale pentru diagnostic in vitro de uz profesional se poate realiza către:
– Alți operatori economici din lanțul de distribuție, care dețin aviz de funcționare pentru distribuție dispozitive medicale, în vederea revânzării sau donării produselor;
– Utilizatorii finali (unități sanitare, cabinete, clinici, etc, care desfășoara activitate de testare)
Conform art. 2 din Legea farmaciei nr. 266/2008, prin farmaciile comunitare se por distribui doar dispozitive medicale de uz individual. Ca urmare, dispozitivele medicale pentru diagnostic in vitro de uz profesional nu se pot distribui prin farmacii.
Referitor la comercializarea în sistem on line a unor dispozitive medicale destinate utilizării de către profesioniști, în acest moment nu există prevederi legale care să interzică această practică.
În calitate de autoritate competentă, neexistând reglementări în acest sens, nu putem interzice comercializarea acestor produse în sistem on line. Putem recomanda evitarea acestei modalități de comercializare sau, în cazul în care se recurge la această formă de distribuție, recomandăm ca vânzarea testelor rapide să fie insoțită de un avertisment în conformitate cu instrucțiunile de utilizare și anume “DOAR PENTRU UZ PROFESIONAL”, sau ca operatorul economic să se asigure că cel care achizitionează produsele respective este unitate medicală. În caz contrar, operatorul economic poate fi sancționat pentru practică comercială înșelătoare.
Toate aceste informații și recomandări sunt valabile și pentru comercializarea și utilizarea testelor utilizate în evaluarea stării imunologice a pacienților suspecți de coronavirus, prin determinarea calitativă a prezenței anticorpilor IgM/IgG împotriva SARS-CoV-2. - Anunț important
11.11.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Gauze Swabs, Lap Sponges, Gauze in Rolls, Gauze in Zigzag, fabricate de producătorul Taizhou Xinzhou Medical Supplies Co., Ltd., China, dacă au intrat în posesia unei copii falsificate a Certificatului de conformitate CE nr. G2S 003599 0003 Rev.00 emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123), valabil de la data de 2019-04-11 până la data de 2024-04-10.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România la Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
11.11.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Latex and Nitrile Surgical Powder free Glove, Sterile, fabricate de producătorul IGLOVE Group Production, Malaezia, pentru care dețin Certificatul de conformitate CE falsificat nr. G2 032745 0003 Rev. 03, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123), valabil de la data de 2020-05-20 până la data de 2020-05-26.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România la Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
03.11.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Infusion Set, Burette Infusion Sets, Blood Transfusion Set (with Needles) for Single Use, Suction Connecting Tube with and without Yankauer, Injection Caps and Valves, Scalp Vein Set for Single Use, 3-way Stopcock, Extension Set for Single Use, fabricate de producătorul Wenzhou K.L.F. Medical Plastics Co., Ltd, China dacă au intrat în posesia Certificatului de conformitate CE falsificat nr. G2 17 11 47985 027, având date ilizibile privind perioada de valabilitate și care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123) pentru acest producător.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul ANMDMR la Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul ANMDMR pentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
06.10.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Disposable Latex Surgical Gloves fabricate de producatorul Sainty International Group Jiangsu Sumex Imp.&Exp.Co.Ltd, China daca au intrat in posesia unei copii falsificate a Certificatului de conformitate CE nr. G2 074980 0012 Rev. 01 emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123) la data de 2020-03-04, valabil pana la data de 2024-05-26.
Pentru verificari proprii privind validitatea Certificatului de conformitate CE detinut se vor consulta informatiile din urmatorul anunt, postat pe site-ul ANMDMR la Sectiunea ANUNTURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
In atentia tuturor partilor interesate (unitati sanitare contractante, importatori si distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
06.10.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Non-contact Infrared Forehead Thermometers (TEMP-02C), fabricate de producatorul Henan Million Medical Electronics Co., Ltd., China, pentru care detin Certificatul de conformitate CE falsificat nr. DD 60105871 0001 care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH, Germania (0197) la data de 2020-07-20, valabil pana la data de 2023-07-19.
Pentru verificari proprii privind validitatea Certificatului de conformitate CE detinut se vor consulta informatiile din urmatorul anunt, postat pe site-ul ANMDMR la Sectiunea ANUNTURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
In atentia tuturor partilor interesate (unitati sanitare contractante, importatori si distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
06.10.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Children’s flat protective mask KB-01, fabricate de producatorul Anhui Kangbao sanitary products Co.,Ltd, China, pentru care detin Certificatul de conformitate CE falsificat nr. G4 063479 0032 Rev.01 care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123) la data de 2020-02-25, valabil pana la data de 2024-05-26.
Pentru verificari proprii privind validitatea Certificatului de conformitate CE detinut se vor consulta informatiile din urmatorul anunt, postat pe site-ul ANMDMR la Sectiunea ANUNTURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
In atentia tuturor partilor interesate (unitati sanitare contractante, importatori si distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
05.10.2020
În atenția persoanelor interesate
Din motive de siguranță medicală, până la stabilizarea situației epidemiologice, începând cu data de 06.10.2020 conducerea ANMDMR a decis suspendarea, la sediul instituției din Bd. Nicolae Titulescu, nr. 58, a relației cu publicul.
În acest context, activitatea de relații cu publicul se va desfășura prin poștă, poștă electronică, telefonic și fax.
Menționăm că, în această perioadă, persoanele interesate pot transmite documente:
– prin postă/ curier la adresa: Bd. Nicolae Titulescu 58, Sector 1, 011144, București, Romania
– prin fax la nr.: +4021-222.86.83
– electronic: către dgdm@anm.ro
Pentru a intra în posesia documentelor emise de ANMDMR, se recomandă, în această perioadă, apelarea la serviciile de curierat.
Persoanele interesate care doresc să obțină informații privind diferite aspecte din sfera de competență a ANMDMR cu privire la dispozitivele medicale, pot contacta reprezentații ANMDMR la numărul de tel: 0212.228.652 – centrală;
Vă mulțumim pentru înțelegere și colaborare. - Anunț important
02.10.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Face masks fabricate de producatorul Jiangsu Eyoung Medical Devices Co., Ltd., China daca au intrat in posesia unei copii falsificate a Certificatului de conformitate CE nr. DD 60132306 0001 emis de Organismul Notificat TÜV Rheinland LGA Products GmbH, Germania (0197) la data de 2018-09-11, valabil pana la data de 2023-09-10, care include aceasta categorie de dispozitive medicale.
Pentru verificari proprii privind validitatea Certificatului de conformitate CE detinut se vor consulta informatiile din urmatorul anunt, postat pe site-ul ANMDMR la Sectiunea ANUNTURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
In atentia tuturor partilor interesate (unitati sanitare contractante, importatori si distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
02.10.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Pulse Oximeter, B-Ultrasonic Diagnostic, Fetal Monitor, Fetal Doppler, Infusion Pump, Syringe Pump, Holter, Operating Table, Operating Lamp, Medical Furniture fabricate de producatorul SOMO INTERNATIONAL CO., LTD, China, daca au intrat in posesia unei copii falsificate a Certificatului de conformitate CE nr. G1 088320 0005 Rev. 01 emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123) la data de 2019-10-16, valabil pana la data de 2024-05-26, care include aceste categorii de dispozitive medicale.
Pentru verificari proprii privind validitatea Certificatului de conformitate CE detinut se vor consulta informatiile din urmatorul anunt, postat pe site-ul ANMDMR la Sectiunea ANUNTURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
In atentia tuturor partilor interesate (unitati sanitare contractante, importatori si distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
02.10.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Powdered and Powder Free latex gloves; Powdered and Powder Free nitrile gloves, fabricate de producatorul Ever Global (Vietnam) Ent. Corp Giang Dien Factory, Vietnam, pentru care detin Certificatul de conformitate CE falsificat nr. G1 15 03 37893 033 care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123), valabil de la data de 2015-09-17 pana la data de 2020-09-10.
Pentru verificari proprii privind validitatea Certificatului de conformitate CE detinut se vor consulta informatiile din urmatorul anunt, postat pe site-ul ANMDMR la Sectiunea ANUNTURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
In atentia tuturor partilor interesate (unitati sanitare contractante, importatori si distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
17.09.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Sleep Apnea Therapy Devices, Respiratory Insufficiency Ventilators and Accessories: CPAP, Auto CPAP, BPAP, Humidifier and Masks. Sleep Apnea Diagnosis Devices and Accessories: Sleep Screener, Polysomnograph, Portable Sleep Diagnostic System, fabricate de producatorul SHOULDERSINK ApS, Danemarca, pentru care detin Certificatul de conformitate CE falsificat nr. G1 17 07 81775 008 care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123), valabil de la data de 2018-04-01 pana la 2023-03-31.
Pentru verificari proprii privind validitatea Certificatului de conformitate CE detinut se vor consulta informatiile din urmatorul anunt, postat pe site-ul ANMDMR la Sectiunea ANUNTURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
In atentia tuturor partilor interesate (unitati sanitare contractante, importatori si distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
17.09.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Sterile Surgical Gowns, Sterile Surgical Drapes, Sterile Surgical Packs, fabricate de producatorul Changzhou HolyMED Products Co., Ltd., China, daca au intrat in posesia unei copii falsificate a Certificatului de conformitate CE nr. G2S 005447 0002 Rev.00 care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123) la data de 2018-10-30, valabil pana la data de 2023-10-29.
Pentru verificari proprii privind validitatea Certificatului de conformitate CE detinut se vor consulta informatiile din urmatorul anunt, postat pe site-ul ANMDMR la Sectiunea ANUNTURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
In atentia tuturor partilor interesate (unitati sanitare contractante, importatori si distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
14.09.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Respiratory protective devices to EN 149:2001-A1:2009:- Filtering half mask to protect against particules Model: FFP2,FFP3,3M (1860 & 1860S,8201V,9001,9100,8210V) & OTHERS, fabricate de producatorul LÖFFL & HOLZNER GMBH, Germania, pentru care detin Certificatul de conformitate CE falsificat nr. G1 16 11 11858 057 care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123), valabil de la data de 2017-01-21 pana la data de 2022-01-20.
Pentru verificari proprii privind validitatea Certificatului de conformitate CE detinut se vor consulta informatiile din urmatorul anunt, postat pe site-ul ANMDMR la Sectiunea ANUNTURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
In atentia tuturor partilor interesate (unitati sanitare contractante, importatori si distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
14.09.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul „Nitrile / Latex Patiente Eamination Gloves” fabricate de producatorul RUNGKIT GLOVE CO., LTD., Tailanda, pentru care detin Certificatul de conformitate CE falsificat nr. G2 86 03 80980 008 care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123), valabil de la data de 2016-05-19 pana la data de 2021-04-11.
Pentru verificari proprii privind validitatea Certificatului de conformitate CE detinut se vor consulta informatiile din urmatorul anunt, postat pe site-ul ANMDMR la Sectiunea ANUNTURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
In atentia tuturor partilor interesate (unitati sanitare contractante, importatori si distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
14.09.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Surgical Drape, Surgical Gown, Surgical Pack, Equipment Cover, Liquid Collection Pouch, Medical Face Mask, Medical Cap, Medical Shoe Cover, Vaginal Speculum / HeNan YADU Industrial Co., Ltd., daca au intrat in posesia unei copii falsificate a Certificatului de conformitate CE nr. G2S 104411 0002 Rev. 00 emis de Organismul Notificat TÜV SÜD Product Service GmbH, Germania (0123) la data de 2019-11-06, valabil pana la data de 2024-05-26.
Pentru verificari proprii privind validitatea Certificatului de conformitate CE detinut se vor consulta informatiile din urmatorul anunt, postat pe site-ul ANMDMR la Sectiunea ANUNTURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
In atentia tuturor partilor interesate (unitati sanitare contractante, importatori si distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
04.09.2020
In atentia producatorilor romani de dispozitive medicale / reprezentantilor autorizati / importatorilor
Utilizarea modulului de inregistrare a “actorilor” din EUDAMED si a numarului unic de inregistrare (SRN) in statele membre
Articolul 33 din Regulamentul privind dispozitivele medicale (UE) 2017/745 al Parlamentului European si al Consiliului din 5 aprilie 2017 (denumit in continuare „MDR”) stabileste ca, dupa consultarea cu Grupul de coordonare in domeniul dispozitivelor medicale (MDCG), Comisia va crea, intretine si gestiona baza europeana de date privind dispozitivele medicale (EUDAMED). EUDAMED este compusa din mai multe sisteme electronice (asa numitele „module”), inclusiv un sistem electronic de inregistrare a operatorilor economici, denumit modulul de inregistrare a actorilor.
In conformitate cu articolul 30 (1) al MDR, modulul de inregistrare a actorilor trebuie sa permita crearea unui numar unic de înregistrare („SRN”) si culegerea si procesarea informatiilor necesare pentru identificarea producatorului (inclusiv producătorii de sisteme / pachete de proceduri) si, daca este cazul, a reprezentantului autorizat si a importatorului. Ca atare, modulul de inregistrare a actorilor constituie o conditie prealabila pentru utilizarea celorlalte module EUDAMED si faciliteaza un mod sigur de accesare a EUDAMED.
Responsabilitatea de a atribui SRN operatorilor economici revine ANMDMR, in calitate de autoritate competenta. In acest scop, articolul 31 alineatul (2) prevede ca, dupa verificarea și validarea datelor introduse in EUDAMED de un operator economic, autoritatea competenta a unui stat membru trebuie sa obtina un SRN de la modulul de inregistrare a actorilor si sa aprobe eliberarea acestuia catre producatorul, reprezentantul autorizat sau importatorul care a solicitat acest lucru.
La 30 octombrie 2019, Comisia a publicat o informare prin care a concluzionat ca functionalitatea integrala a EUDAMED necesita disponibilitatea si functionarea completa a tuturor celor șase module si confirmarea printr-un audit. Informarea prevede lansarea unei EUDAMED pe deplin functionala pentru mai 2022.
Cu toate acestea, in cadrul reuniunii sale din 12 martie 2020, MDCG a convenit ca fiecare modul EUDAMED poate fi disponibil, in mod gradual, imediat ce acesta este operational. Comisia a confirmat disponibilitatea de a lansa modulul de inregistrare a actorilor incepand cu 1 decembrie 2020. Membrii MDCG incurajeaza cu tarie utilizarea modulului de inregistrare a actorilor de catre toti actorii relevanti de pe teritoriile lor, inclusiv utilizarea SRN de catre actori, asa cum este stipulat în MDR (de exemplu, indicarea SRN pe certificate).
Membrii MDCG sunt de acord ca cerintele de inregistrare dubla pentru actori sa fie evitata cat mai mult posibil. Prin urmare, ar trebui luati in considerare actorii care obtin un SRN in conformitate cu cerintele de inregistrare a actorilor (pentru producatori, reprezentanti autorizati, importatori, producatori de pachete de sisteme / proceduri) in masura in care legislatia nationala permite acest lucru. In astfel de cazuri, actorii ar trebui sa respecte obligatiile si cerintele MDR legate atat de inregistrarea actorilor relevanti (prin intermediul modulului de inregistrare “actori”) si utilizarea SRN-ului lor, dupa cum este necesar.
ANMDMR si-a anuntat intentia de a participa la inregistrarea in regim voluntar in EUDAMED, imediat ce modulul de inregistrare a actorilor va fi functional.
Preluare din: https://ec.europa.eu/health/sites/health/files/md_sector/docs/2020-15-position-paper-actor-registration-module_en.pdf - Anunț important
04.09.2020
In atentia tuturor partilor interesate (unitati sanitare contractante, importatori si distribuitori de dispozitive medicale s.a.)
Ca urmare a multiplelor informari primite de institutia noastra, potrivit carora sunt depistate in permanenta pe piata UE copii falsificate ale unor Certificate de conformitate CE emise de Organismele Notificate TÜV SÜD Product Service GmbH, Germania (0123) si TÜV Rheinland LGA Products GmbH, Germania (0197) sau care se pretind a fi emise de aceste Organisme Notificate, mai ales ca urmare a crizei generate de pandemia COVID-19, venim in sprijinul partilor interesate cu urmatoarele clarificari:
1. Un Certificat de conformitate CE intrat in posesia unui operator economic sau prezentat de un operator economic unei unitati sanitare contractante (ex. in cadrul unei licitatii publice) si nominalizat intr-un anunt postat in sectiunea Anunturi importante – dispozitive medicale de pe site-ul ANMDMR poate fi valid doar in conditiile in care acel certificat se regaseste cu informatii identice in baza de date cu certificatele emise, disponibila pe site-ul Organismului Notificat respectiv (0123 sau 0197), baze de date care pot fi consultate accesand link-urile:
TÜV SÜD Product Service GmbH, Germania (0123) – Baza de date cu certificatele emise
https://www.tuvsud.com/de-de/dienstleistungen/produktpruefung-und-produktzertifizierung/zertifikatsdatenbank (criteriu de cautare al doilea grup de cifre din numarul de certificat – ex. 068194 – pentru anuntul postat in 04.08.2020).
TÜV Rheinland LGA Products GmbH, Germania (0197) – Baza de date cu certificatele emise
https://www.certipedia.com/ (criteriu de cautare al doilea grup de cifre din numarul de certificat – ex. 60131859 – pentru anuntul postat in 30.04.2020).
2. Intrucat au fost depistate multiple modalitati de falsificare a unui certificat, in conditiile in care Certificatul de conformitate CE nominalizat in anuntul ANMDMR se regaseste ca fiind valid in baza de date a respectivului Organism Notificat (mentionata la pct. 1), pentru identificarea elementelor care incadreaza o copie a acelui certificat in categoria celor falsificate se va consulta baza de date cu certificatele falsificate a respectivului Organism Notificat, respectiv:
TÜV SÜD Product Service GmbH, Germania (0123) – Baza de date cu certificatele falsificate
https://www.tuvsud.com/de-de/dienstleistungen/produktpruefung-und-produktzertifizierung/zertifikatsdatenbank/tuev-sued-pruefzeichen/liste-gefaelschter-zertifikate
TÜV Rheinland LGA Products GmbH, Germania (0197) – Baza de date cu certificatele falsificate
https://www.tuv.com/world/en/black-list/
3. In conditiile in care Certificatul de conformitate CE nominalizat in anuntul ANMDMR nu se regaseste inca in baza de date cu certificatele falsificate a respectivului Organism Notificat (mentionata la pct. 2), actualizarea acesteia fiind responsabilitatea exclusiva a acelui Organism (in conformitate cu procedurile proprii), recomandam partilor interesate sa solicite clarificari de la Organismul Notificat emitent referitor la validitatea copiei de Certificat de conformitate CE detinute.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
06.08.2020
În atenția parților interesate
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Non Sterile Latex Surgical Gloves (Powdered & Powder Free)Latex Examination Gloves( Powdered & Powder Free), Nitrile Examination Gloves( Powdered & Powder Free), Plastic Gloves, Vinyl Gloves, Household Gloves, Disposable Mask, Cap, Apron, Gowns, Shoe cover & Leggings – clasa I steril, fabricate de producatorul UAB Kostadena, Lituania pentru care detin Certificatul de conformitate CE falsificat nr. G2S 12 03 62218 009, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2018-03-21, valabil pana la data de 2021-04-17.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
04.08.2020
În atenția parților interesate
Avand in vedere contextul epidemiologic actual, ca urmare a necesitatii asigurarii pietei de dispozitive medicale din Romania cu produse tip masti, halate, combinezoane…etc., teste rapide pentru detectarea SARS–COV 2 (dosare tip F1/F2), tinand cont de multiplele solicitari primite de ANMDMR referitoare la stadiul dosarelor de notificare a punerii în functiune pe teritoriul Romaniei a dispozitivelor medicale (dosare tip F3), pana la finalizarea starii de alerta in care ne aflam, a fost sistata inregistrarea in baza nationala de date a dosarelor tip F3.
Va readucem la cunostinta faptul ca inregistrarea in baza nationala de date a dispozitivelor medicale puse in functiune pe teritoriul Romaniei nu reprezinta o aprobare sau autorizare din partea Agentiei Nationale a Medicamentului si a Dispozitivelor Medicale din Romania si nu poate constitui un motiv pentru restrictionarea liberei circulatii a unui dispozitiv medical. - Anunț important
04.08.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Surgical Drape, Surgical Gown, Sterile Surgical Kit, Face Mask – clasa I steril, indiferent de cine sunt fabricate, pentru care detin Certificatul de conformitate CE falsificat nr. G2S 068194 0008 Rev. 00, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123), valabil de la data de 2019-01-23 pana la data de 2024-01-22.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
04.08.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Non Sterile Latex Surgical Gloves (Powdered & Powder Free), Latex Examination Gloves (Powdered & Powder Free), Nitrile Examination Gloves (Powdered & Powder Free), Plastic Gloves, Vinyl Gloves, Household Gloves – clasa I steril, fabricate de producatorul SFH FOOD GMBH, Germania pentru care detin Certificatul de conformitate CE falsificat nr. G2S 12 03 62218 009, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2018-03-21, valabil pana la data de 2021-04-17.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
04.08.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Latex and Nitrile Surgical Powder free Glove, Sterile – clasa IIa, fabricate de producatorul Premier Flex Sdn. Bhd., Malaezia pentru care detin Certificatul de conformitate CE falsificat nr. G2 055729 0008 Rev. 01, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2020-02-19, valabil pana la data de 2024-05-26.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
31.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Anaestetic Mask, Protective Face Mask, Medical Face Mask and Disposable Surgical Mask – clasa IIa, fabricate de producatorul Shen Zhen Moph Biotech CO. LTD, China pentru care detin Certificatul de conformitate CE falsificat nr. G1 002317 0002 Rev. 00, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2020-03-20, valabil pana la data de 2021-08-10.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
31.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Sterile Latex / Nitrile Surgical Gloves – clasa I steril, fabricate de producatorul Lohmann & Rauscher International GmbH & CO. KG., Germania pentru care detin Certificatul de conformitate CE falsificat nr. G2 12 05 62722 006, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2016-06-18, valabil pana la data de 2022-06-17.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
31.07.2020
In atentia partilor implicate in procesul de achizitie dispozitive medicale pentru diagnostic in vitro COVID-19
ANMDMR aduce la cunostinta tuturor partilor interesate de procesul de achizitie de teste, in vederea utilizarii de catre specialistii in domeniul sanatatii in contextul testarii COVID-19, faptul ca, in urma postarii Anuntului din 19.06.2020 potrivit caruia a fost facuta publica de catre Comisia Europeana o baza de date cu dispozitivele medicale pentru diagnostic in vitro COVID-19, atat cu marcaj CE cat si dezvoltate in-house (Research Use Only), baza de date care va fi actualizata de catre Comisia Europeana si se poate consulta accesand linkul:
https://covid-19-diagnostics.jrc.ec.europa.eu/
nu se mai justifica actualizarea de catre ANMDMR a informatiilor cuprinse in tabelul atasat Anuntului din 15.05.2020.
Se vor lua in considerare informatiile disponibile pe site-ul Comisiei Europene si doar in conditiile in care nu toate dispozitivele se vor regasi in acea baza de date, va puteti adresa ANMDMR pentru verificari suplimentare. - Anunț important
23.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Gauze Pads, Disposable Shoe Covers, Gauze Rolls, Disposable Sterile Surgical Masks, Disposable Sterile Surgical Caps, Disposable Sterile Surgical Gown, Disposable Sterile Surgical Drapes, Disposable Sterile Bed Sheet, Disposable Sterile Pad, Disposable Sterile Towel, indiferent de cine sunt fabricate, pentru care detin Certificatul de conformitate CE falsificat nr. G2S 095916 0006 Rev. 00, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2019-04-26, valabil pana la data de 2022-03-12.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
23.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Latex and Nitrile Surgical Powder free Glove, Sterile – clasa IIa, fabricate de producatorul TOP GLOVE, Malaezia, pentru care detin Certificatul de conformitate CE falsificat nr. G2 055729 0008 Rev. 01, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2020-02-19, valabil pana la data de 2024-05-26, certificat in care se specifica o adresa incorecta a producatorului, respectiv Lot 396, Jalan Mekanikal 2 Nilai 7, Nilai Negari Sembilan, 71800.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
23.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Surgical Drape, Surgical Gown, Sterile Surgical Kit, Face Mask – clasa I steril, indiferent de cine sunt fabricate, pentru care detin Certificatul de conformitate CE falsificat nr. G2S 068194 0008 Rev.00, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2019-01-23, valabil pana la data de 2024-01-22.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
21.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Surgical Set, Surgical Gown, Surgical Drape, Tube Cover, Liquid Collection Pouch, Warm Blanket and Surgical Hood, indiferent de cine sunt fabricate din afara UE, avand reprezentant autorizat in UE firma Shanghai International Holding Corp. GmbH (Europe), Germania pentru care detin Certificatul de conformitate CE falsificat nr. G2S 18 01 83528 008, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123), valabil de la data de 2018-04-23 pana la data de 2023-04-22.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
21.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul 3ply Surgical Disposable Face Mask; N95 Respiratory Face Mask; Preventive and Hazard suits; latex Gloves, fabricate de producatorul Medical Industrial Company Worldwide AG, pentru care detin Certificatul de conformitate CE falsificat nr. DD 80087278 8001, care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH (0197), valabil de la data de 2018-08-02 pana la data de 2022-04-23.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
20.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Disposable Surgical Gowns, Disposable Medical Caps, Disposable Medical Masks, Disposable Gauze Sponges, Disposable Sterile Surgical Packs, Disposable Dressing Packs, Disposable Surgical Drapes – clasa I steril si IIa, indiferent de cine sunt fabricate, pentru care detin Certificatul de conformitate CE falsificat nr. DD 60126611 0001, care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH (0197) la data de 2018-02-28, valabil pana la data de 2023-01-22.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
20.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Sterile Urine Drainage Bag, Sterile Vaginal Speculum, Disposable Umbilical Cord Clamps, Disposable I.D. Bracelets, Disposable Dressing Kits, Disposable Gynecological Sets, Gauze Swab (Sponges), Gauze Bandages, Absorbent Cotton Rolls, Absorbent Cotton Balls, First Aid Kits, Bandages, Sterile Wound Plaster, Sterile Wound Dressing, Surgical Gowns, Face Masks, Shoe Covers, Cotton Swab (Cotton Tipped Applicators), Tongue Depressor, Sterile Feeding Tubes, Disposable Stomach Tubes, Disposable Mucus Extractors, Sterile Latex Examination Gloves – clasa I steril, indiferent de cine sunt fabricate, pentru care detin Certificatul de conformitate CE falsificat nr. G2S 16 10 89326 007, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2018-03-30, valabil pana la data de 2021-01-12.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
20.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitivele medicale de clasa IIa si IIb, fabricate de producatorul Phoenix Pharma bv, Olanda, care fac obiectul Certificatului de conformitate CE falsificat nr. HD 60133038 0001, care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH (0197), valabil de la data de 2019-11-07 pana la data de 2023-07-11.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
20.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Disposable Nitrile and Latex Surgical Gloves, fabricate de producatorul PROTECT-Laserschutz GmbH, Germania pentru care detin Certificatul de conformitate CE falsificat nr. G2 12 03 62218 008, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) valabil de la data de 2016-07-12 pana la data de 2021-07-11.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
20.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul General non-active, non-implantable medical devices; Non-active devices for anaesthesia, emergency and intensive care; Non-active devices for injection, infusion, transfusion and dialysis; Non-active instruments; Bandages and would dressings; Medical Gloves (detaliate in anexa), indiferent de cine sunt fabricate, pentru care detin Certificatul de conformitate CE falsificat fara numar, dar cu nr. raport SH1929915, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2019-08-27, valabil pana la data de 2021-04-17.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
20.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Surgical Gowns, Surgical Drapes and Surgical Packs – clasa I steril, fabricate de producatorul GRAVE VIEW TRADERS CO. LTD., Pakistan, pentru care detin Certificatul de conformitate CE falsificat nr. G2S 12 06 80763 00, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2012-09-26, valabil pana la data de 2020-09-25.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
20.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Sterile Drapes, Sterile Surgical Gowns, Protection Coverall, Equipment Cover, Surgical Packs, indiferent de cine sunt fabricate din Xuchang City, Henan Province, China, pentru care detin Certificatul de conformitate CE falsificat nr. G2S 073966 0008 Rev. 01, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2019-10-15, valabil pana la data de 2024-05-26.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
20.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Gauze Products, Synthetic Non-woven Products, 100% Cotton Non-woven Products, Cotton Products, Special Dressing Products, indiferent de cine sunt fabricate, pentru care detin Certificatul de conformitate CE falsificat nr. G2S 046241 0064 Rev. 04, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2019-12-09, valabil pana la data de 2024-05-26.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
20.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Surgical Gowns, Surgical Drapes, Sterile Instrumental Cover, Sterile Protective Cover, indiferent de cine sunt fabricate, pentru care detin Certificatul de conformitate CE falsificat nr. G2 078453 0014 Rev. 01, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2018-01-10, valabil pana la data de 2023-01-09.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
20.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Medical Silicone Gel Dressing, Medical Silicone Sheet Dressing (Light&Clear), Foam Dressing, Skin Stretching and Secure Would-Closure System, Hydrocolloid Dressing, Vacuum Sealing Drainage Dressing Kit, indiferent de cine sunt fabricate din afara UE, avand reprezentant autorizat in UE firma Prolinx GmbH Germania, pentru care detin Certificatul de conformitate CE falsificat nr. G2 094598 0005 Rev.00, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2018-11-09, valabil pana la data de 2021-07-28.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
20.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Medical face mask, Surgical mask – clasa I steril, fabricate de producatorul Anqing Jiaxin Medical Material Co, Ltd., China, pentru care detin Certificatul de conformitate CE falsificat nr. G2S 057761 0012, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2020-02-25, valabil pana la data de 2025-02-24.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
15.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Surgical Drape, Surgical Gown, Sterile Surgical Kit, Face Mask – clasa I steril, indiferent de cine sunt fabricate, pentru care detin Certificatul de conformitate CE falsificat nr. G2S 068194 0008 Rev. 00, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123), valabil de la data de 2019-01-23 pana la data de 2024-01-22.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
14.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Digital Thermometers, 3 ply disposable masks, 3M N95 surgical masks, Non-Contact Infrared Thermometer – clasa IIa, fabricate de producatorul EVERGREEN Cooperation Ltd., Camerun, pentru care detin Certificatul de conformitate CE falsificat nr. G2 17 12 02927 002, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2018-05-08, valabil pana la data de 2023-05-07.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
14.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Mobile ECG Detector– clasa IIa, fabricate de producatorul Shenzhen Maner Wei Plastic Hardware Products Co., Ltd., China, pentru care detin Certificatul de conformitate CE falsificat nr. G1 099677 0002 Rev. 00, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data de 2019-07-09, valabil pana la data de 2024-05-26.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
14.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Disposable Latex Surgical Gloves; Medical Examination Gloves – clasa IIa, fabricate de producatorul PIDEGREE INDUSTRIAL CO LIMITED, China, pentru care detin Certificatul de conformitate CE falsificat nr. G2 16 03 74980 008, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123), valabil de la data de 2016-05-19 pana la data de 2021-04-11.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
08.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul KN95 masks, medical masks – clasa IIa, fabricate de producatorul Wugang xiezhong Medical Equipment Co.Ltd., China, pentru care detin Certificatul de conformitate CE falsificat nr. DD 244236340a 001, care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH (0197), la data de 2020-05-09, valabil pana la data de 2023-05-09.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
08.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Dental Units – clasa IIa, fabricate de producatorul Wenzhou Longde Medical Technology Co., Ltd., China, pentru care detin Certificatul de conformitate CE falsificat nr. DD 60111840 0001, care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH (0197) la data de 2016-08-11, valabil pana la data de 2021-08-10.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
03.07.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Face Masks, Surgical Gowns, Coveralls, Caps – clasa I steril, fabricate de producatorul Page Global Pty Ltd, Africa de Sud, pentru care detin Certificatul de conformitate CE falsificat nr. DD 60135422 0001, care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH (0197), valabil de la data de 2019-07-16 pana la data de 2024-01-16.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
23.06.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Sterile Surgical Gloves And Examination Gloves fabricate de BESAFE GLOVES Co., Ltd., Thailanda pentru care detin Certificatul de conformitate CE falsificat nr. DD 60076250 0701, care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH (0197) la data 2019-06-13, valabil pana la data de 2023-06-13.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
22.06.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Kn 95 masks, medical masks, fabricate de Wugang xiezhong Medical Equipment Co., Ltd, China pentru care detin Certificatul de conformitate CE falsificat nr. DD 60132601 0002, care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH (0197) la data 2020-05-09, valabil pana la data de 2023-05-09.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
22.06.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Leukocyte Reduction Filters (sets) – clasa IIb, indiferent de cine sunt fabricate, pentru care detin Certificatul de conformitate CE falsificat nr. HD 60130160 0001, care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH (0197) la data 2018-06-21, valabil pana la data de 2023-06-20.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
22.06.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de clasa IIb fabricate de Aafama bv, Olanda, pentru care detin Certificatul de conformitate CE falsificat nr. HD 60133038 0001, care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH (0197) la data 2019-11-07, valabil pana la data de 2023-07-11.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
22.06.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
Ca urmare a unei informari primite de ANMDMR privind identificarea pe piata globala a multor fraude savarsite de agenti falsi, care pretindeau ca reprezinta companiile respective pentru furnizare de manusi, atentionam toti importatorii si distribuitorii care intentioneaza sa introduca pe piata din Romania manusi fabricate in Malaiezia, sa verifice autenticitatea producatorilor acestor dispozitve medicale la MARGMA – Malaysian Rubber Glove Manufacturers Association, astfel:
– prin accesarea link-ului http://www.margma.com.my
sau
– prin transmiterea unui email la adresa contact@margma.com.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
19.06.2020
În atenția persoanelor interesate – dispozitive medicale pentru diagnostic in vitro COVID-19
ANMDMR aduce la cunostinta tuturor partilor interesate de procesul de achizitie de teste in vederea utilizarii de catre specialistii in domeniul sanatatii in contextul testarii COVID-19 faptul ca a fost facuta publica de catre Comisia Europeana o baza de date cu dispozitivele medicale pentru diagnostic in vitro COVID-19, atat cu marcaj CE cat si dezvoltate in-house (Research Use Only).
Aceasta baza de date, care cuprinde dispozitivele medicale pentru diagnostic in vitro cu marcaj CE inregistrate de Autoritatile Competente din Statele Membre, potrivit prevederilor art. 29 si 31 din HG nr. 798/2003, echivalentul art. 10 alin. (1) si (3) din Directiva 98/79/EC, va fi actualizata de catre Comisia Europeana si se poate consulta accesand linkul:
https://covid-19-diagnostics.jrc.ec.europa.eu/ - Anunț important
19.06.2020
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România atenționează toți importatorii și distribuitorii de dispozitive medicale să nu introducă pe piața din România dispozitive medicale de tipul Sterile Surgical Caps, Sterile Surgical Face Masks, Sterile Surgical Gowns, Sterile Bed Protections, Sterile Surgical Drapes, Sterile Surgical Packs dacă sunt fabricate de orice alt producător în afară de Sunsmed Protective Products Ltd., China, pentru care au intrat în posesia unei copii falsificate a Certificatului de conformitate CE nr. DD 60111758 0001, emis de Organismul Notificat TÜV Rheinland LGA Products GmbH (0197) la data 2016-08-12, valabil până la data de 2021-08-11.
Pentru verificări proprii privind validitatea Certificatului de conformitate CE deținut se vor consulta informațiile din următorul anunț, postat pe site-ul ANMDMR la Secțiunea ANUNȚURI IMPORTANTE – DISPOZITIVE MEDICALE:
04.09.2020
În atenția tuturor părților interesate (unități sanitare contractante, importatori și distribuitori de dispozitive medicale s.a.)
Pentru a preveni introducerea în lanțul legal de distribuție, mai ales în contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respectă cerințele de reglementare aplicabile, vă rugăm să manifestați prudență maximă, să consultați permanent site-ul Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din Româniapentru astfel de informări și să vă asigurați că produsele pe care le achiziționați provin de la distribuitori avizați de instituția noastră, în conformitate cu dispozițiile art. 926 din Legea 95/2006 privind reforma în domeniul sănătății, republicată, cu modificările și completările ulterioare. - Anunț important
19.06.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Face Masks, Surgical Gowns, Surgical Caps, Surgical Drapes, Surgical Drape Packs – clasa I steril, indiferent de cine sunt fabricate, pentru care detin Certificatul de conformitate CE falsificat nr. DD 60139107 0001, care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH (0197) la data 2020-01-23, valabil pana la data de 2024-05-26.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
15.06.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Face Mask, Disposable surgical gloves, Protective overalls, Infrared digital Thermometer, hand sanitizers and surgical kits, fabricate de BALTIMER Sp. Z.o.o, Polonia pentru care detin Certificatul de conformitate CE falsificat nr. DD 60091096 0001, care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH (0197) la data 2019-01-28, valabil pana la data de 2024-01-27.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
15.06.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Gauze Pads, Disposable Shoe Covers, Gauze Rolls, Disposable Sterile Surgical Masks, Disposable Sterile Surgical Caps, Disposable Sterile Surgical Gown, Disposable Sterile Surgical Drapes, Disposable Sterile Bed Sheet, Disposable Sterile Pad, Disposable Sterile Towel – clasa I steril, indiferent de cine sunt fabricate, pentru care detin Certificatul de conformitate CE falsificat nr. G2S 095916 0006 Rev. 00, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data 2019-04-26, valabil pana la data de 2022-03-12.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
15.06.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Sterile Surgicat Gowns, Medical Surgical Gloves, Disposable Face Masks, Sterile Surgical Drapes, Sterile Equipment Covers and Sterile Scope Warmers, fabricate de ATOS SAGLIK URUNLERI TEKSTIL SANAYI VE TIC , LTD, Turcia pentru care detin Certificatul de conformitate CE falsificat nr. G2S 17 02 98215 001, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data 2017-03-14, valabil pana la data de 2022-03-13.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
11.06.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Non-contact Infrared Thermometer, Digital Thermometer, Ear Thermometer, Nasal Aspirator – clasa IIa, indiferent de cine sunt fabricate din afara UE, avand reprezentant autorizat in UE firma Wellkang Ltd., Irlanda, pentru care detin Certificatul de conformitate CE falsificat nr. G1 082883 0014 Rev. 00, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte, Germania (0123), valabil de 2019-05-15 pana la data de 2023-07-28.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
11.06.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul FFP3 Face Masks; KN95 Face Masks; 3PLY Face Masks; Non-Woven Surgical Gowns; Nitrile Surgical Hand Gloves; Latex Medical Examination Hand Gloves – clasa I steril, fabricate de producatorul SCHIFFA PLASTER, Siria, pentru care detin Certificatul de conformitate CE falsificat nr. G2S 16 12 57099 017, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte, Germania (0123), valabil de la data de 2020-03-29 pana la data de 2023-03-30.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
11.06.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Sterile Surgical Gowns, Sterile Surgical Packs, Face Mask, Isolation Gown – clasa I steril, fabricate de producatorul Lyncmed Medical Technology (Beijing) Co., Ltd., China, pentru care detin Certificatul de conformitate CE falsificat nr. G2S 17 08 99730 003, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte, Germania (0123), valabil de la data de 2017-12-20 pana la data de 2022-12-19.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
15.05.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Disposable Vinyl Gloves – clasa I steril, fabricate de producatorul HaoRui Industry Co., Ltd, China, pentru care detin Certificatul de conformitate CE falsificat nr. G2S 09 09 70125 002, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte, Germania (0123) la data 2016-11-12, valabil pana la data de 2021-11-11.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
15.05.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul „Latex and Nitrie Surgical Gloves Sterile 6, 6.5, 7, 7.5, 8, 8.5, 9” – clasa I steril, fabricate de producatorul Unigloves Sdn Bhd (Berhad), Malaezia, pentru care detin Certificatul de conformitate CE falsificat nr. G2S 12 03 43898 012, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte, Germania (0123), valabil de la data de 2012-06-18 pana la data de 2023-06-17.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
15.05.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Sterile disposable syringes, infusion sets, perfusion sets and transfusion sets, sterile needles, sterile surgical gloves, intravenous catheters, surgical gowns, surgical kits and surgical drapes fabricate de producatorul Nasza Chata Medical Products, Polonia, pentru care detin Certificatul de conformitate CE falsificat nr. D1263400017, care ar fi emis de Organismul Notificat mdc medical device certification GmbH, Germania (0483) la data 2020-03-26, valabil pana la data de 2024-05-26.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
15.05.2020
În atenția persoanelor interesate
Ca urmare a solicitărilor primite de ANMDMR de la diferite firme care doresc punerea pe piața din Romania a unor ventilatoare fabricate în regim de urgență, vă informam că potrivit dispozițiilor art. 932 alin. (1) din Legea nr. 95/2006 privind reforma în domeniul sănătății și ale art. 2 lit. d)-h) și art. 4 alin. (4) din Legea nr. 134/2019 privind reorganizarea Agenției Naționale a Medicamentului și a dispozitivelor Medicale, precum și pentru modificarea unor acte normative, ANMDMR este autoritatea competentă si decizională și autoritate de supraveghere a pieței în domeniul dispozitivelor medicale și nu are atribuții de organism de evaluare a conformității dispozitivelor medicale.
descarca documentul…
- Anunț important
15.05.2020
În atenția persoanelor interesate
Ca urmare a multiplelor solicitari primite de ANMDMR de la diferite unitati sanitare/firme de distributie privind conformitatea anumitor teste pe care intentioneaza sa le achizitioneze in vederea utilizarii de catre specialistii in domeniul sanatatii in contextul testarii COVID-19, punem la dispozitia tuturor celor interesati un tabel cu dispozitivele medicale pentru diagnostic in vitro identificate de ANMDMR la data de 12.05.2020 ca fiind inregistrate in Uniunea Europeana.
Mentionam faptul ca, potrivit reglementarii in vigoare, respectiv Directiva 98/79/EC privind dispozitivele medicale pentru diagnostic in vitro, cu modificarile si completarile ulterioare (transpusa in legislatia nationala prin HG nr. 798/2003 privind stabilirea condiţiilor de introducere pe piaţă şi de utilizare a dispozitivelor medicale pentru diagnostic in vitro, cu modificarile si completarile ulterioare), pentru a putea fi introduse pe piata UE si implicit in Romania, dispozitivele medicale pentru diagnostic in vitro de tipul testelor trebuie sa:
– Poarte marcajul CE, marcaj care semnifica indeplinirea cerintelor aplicabile tipului de produs potrivit dispozitiilor art. 10 alin. (1) din HG nr. 798/2003, respectiv art. 4 alin. (1) din Directiva 98/79/EC;
– Producatorul din afara UE trebuie sa desemneze un reprezentant autorizat cu sediul in UE si acesta sa fie nominalizat (in declaratie, pe eticheta sau ambalaj exterior ori instructiuni de utilizare) conform prevederilor art. 31 alin. (1) si lit. B) pct. 8.4 lit. a) din Anexa nr. 1 – Cerinte esentiale din HG nr. 798/2003, care transpun dispozitiile art. 10 alin. (3) si ale lit. B) pct. 8.4. lit. a) din Anexa I din Directiva 98/79/EC;
– Sa fie inregistrate la autoritatea competenta din statul membru UE unde isi are sediul producatorul (in cazul producatorilor din UE) potrivit prevederilor art. 29 si 32 din HG nr. 798/2003, echivalentul art. 10 alin. (1) si (4) din Directiva 98/79/EC sau la autoritatea competenta din statul membru UE unde isi are sediul reprezentantul autorizat (in cazul producatorilor din afara UE) conform art. 31 si 32 din HG nr. 798/2003 echivalentul art. 10 alin. (3) si (4) din Directiva 98/79/EC.
In contextul in care aceasta lista se modifica permanent de catre Autoritatile Competente responsabile de inregistrarea acestor dispozitive medicale pentru diagnostic in vitro, va rugam sa consultati in permanenta site-ul ANMDMR pentru informatii actualizate privind dispozitivele medicale pentru diagnostic in vitro inregistrate la nivelul UE pentru COVID-19.
descarca documentul…
- Anunț important
13.05.2020
În atenția tuturor celor interesați
ANMDMR aduce la cunostinta tuturor celor interesati anuntul facut de Comisia Europeana in 23.04.2020 privind adoptarea la nivelul Consiliului Europei si a Parlamentului European a propunerii de amanare cu 1 an, pana la 26 Mai 2021, a termenului de punere totala in aplicare a Regulamentului (UE) 2017/745 al Parlamentului European și al Consiliului din 5 aprilie 2017 privind dispozitivele medicale, de modificare a Directivei 2001/83/CE, a Regulamentului (CE) nr. 178/2002 și a Regulamentului (CE) nr. 1223/2009 și de abrogare a Directivelor 90/385/CEE și 93/42/CEE ale Consiliului – MDR, in scopul prioritizarii luptei impotriva Coronavirus. Regulamentul (UE) 2020/561 al al Parlamentului European și al Consiliului din 23 aprilie 2020 de amendare a MDR amana de asemenea cu 1 an data de abrogare a Directivelor 90/385/CEE și 93/42/CEE ale Consiliului, dar nu are niciun impact asupra datei de punere totala in aplicare a Regulamentului (UE) 2017/746 al Parlamentului European și al Consiliului din 5 aprilie 2017 privind dispozitivele medicale pentru diagnostic in vitro și de abrogare a Directivei 98/79/CE și a Deciziei 2010/227/UE a Comisiei – IVDR, care ramane 26 Mai 2022.
descarca documentul…
- Anunț important
13.05.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Respiratory humidification devices and accessories class II (Disposable Patient Circuits, Transfer Unit), fabricate de producatorul ANDERS LARSSON LIVS AB, Suedia, pentru care detin Certificatul de conformitate CE falsificat nr. 170724386, care ar fi emis de Organismul Notificat DQS Medizinprodukte GmbH, Germania (0297) la data 2019-02-02, valabil pana la data de 2024-02-02.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
13.05.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Surgical Gowns, Surgical Drapes, Sterile Instrumental Cover, Sterile Protective Cover – clasa I steril, indiferent de cine sunt fabricate din afara UE, avand reprezentant autorizat in UE firma Shanghai International Holding Corp. GmbH (Europe), Germania, pentru care detin Certificatul de conformitate CE falsificat nr. G2S 17 11 53056 020, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data 2018-01-10, valabil pana la data de 2023-01-09.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
30.04.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Surgical Mask, Wound Plaster – clasa I steril, indiferent de cine sunt fabricate din afara UE, avand reprezentant autorizat in UE firma Shanghai International Holding Corporation GmbH (Europe), Germania, pentru care detin Certificatul de conformitate CE falsificat nr. G2S 15 11 90069 004, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte (0123) la data 2016-02-04, valabil pana la data de 2021-02-03.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
30.04.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Disposable surgical mask 17,5cm x 9,5 cm – clasa I, fabricate de producatorul Guangzhou Renault Biotechnology Co. Ltd., China, pentru care detin Declaratia de conformitate CE nr. HDK-010-030220R emisa de producator la data 16.03.2020, cu identificarea in mod fals a firmei CMC Medical Devices & Drugs S.L, Spania ca reprezentant autorizat desemnat al producatorului.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
30.04.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul OP Drapes, Disposable Gowns (Clasa Is), Wound Dressings, (Clasele IIa, IIb, III), Cryotherapy Products (Clasa IIa), Disposable Face Masks 3M and 3Ply Face Masks, fabricate de producatorul BL Global Trading (Pty) Ltd, Africa de Sud, dispozitive care fac obiectul Certificatului de conformitate CE falsificat nr. 170715834, care ar fi emis de Organismul Notificat DQS Medizinprodukte GmbH, Germania (0297) la data 2018-05-16, valabil pana la data de 2022-03-09.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
30.04.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Medical Absorbent Gauze Pads, Medical Cotton Tipped Applicators, Disposable Sterile Medical Face Masks, Disposable Sterile Surgical Gowns, Disposable Medical Shoes Covers, Disposable Medical Surgical Drapes – clasa I steril, indiferent de cine sunt fabricate, dar pentru care detin Certificatul de conformitate CE falsificat nr. DD 60115803 0001, care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH, Germania (0197) la data 2017-04-20, valabil pana la data de 2022-01-27.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
30.04.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Medical Non-woven Masks, Medical Non-woven Gowns, Medical Coveralls – clasa I steril, indiferent de cine sunt fabricate, dar pentru care detin Certificatul de conformitate CE falsificat nr. DD 60131859 0001, care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH, Germania (0197) la data 2018-12-04, valabil pana la data de 2023-10-22.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
24.04.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Anaesthesia Systems, Ventilators, CPAP Systems – clasa IIb, fabricate de producatorul Shanghai Ro-Chain Medical Co. Ltd., China, dispozitive care fac obiectul Certificatului de conformitate CE falsificat nr. G1 17 10 82515 005 care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte, Germania (0123) la data de 2018-03-05, valabil pana la data de 2023-02-28.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
24.04.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Face Masks, Surgical Gowns, Non-woven Coveralls, Surgical Drapes – clasa I steril, fabricate de producatorul Honki Meilink Healthcare Co., Ltd, Vietnam, dispozitive care fac obiectul Certificatului de conformitate CE falsificat nr. DD 60098446 0001, care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH, Germania (0197) la data 2015-03-03, valabil pana la data de 2020-10-24.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
24.04.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Respiratory humidification devices and accessories (Disposable Patient Circuits, Transfer Unit) – clasa IIa, fabricate de producatorul TRADING COMPANY BL LTD, UK, dispozitive care fac obiectul Certificatului de conformitate CE falsificat nr. 170724386, care ar fi emis de Organismul Notificat DQS Medizinprodukte GmbH, Germania (0297) la data 2019-02-02, valabil pana la data de 2024-02-02.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
24.04.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Face Masks, Surgical Gowns, Surgical Caps, Surgical Sheets, Surgical Drapes, Coveralls, Shoe Covers, Surgical Kits – clasa I steril, indiferent de cine sunt fabricate, dar pentru care detin Certificatul de conformitate CE falsificat nr. DD 60091096 0001, care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH, Germania (0197) la data 2015-01-28, valabil pana la data de 2020-08-27.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
24.04.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Face Masks, Surgical Gowns, Coveralls, Caps – clasa I steril, indiferent de cine sunt fabricate, dar pentru care detin Certificatul de conformitate CE falsificat nr. DD 60102531 0001, care ar fi emis de Organismul Notificat TÜV Rheinland LGA Products GmbH, Germania (0197) la data 2015-07-10, valabil pana la data de 2020-07-09.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra, in conformitate cu dispozitiile art. 926 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare. - Anunț important
23.04.2020
În atenția persoanelor interesate
Ca urmare a multiplelor solicitari primite de ANMDMR de la diferite unitati sanitare/firme de distributie privind conformitatea anumitor teste pe care intentioneaza sa le achizitioneze in vederea utilizarii de catre specialistii in domeniul sanatatii in contextul testarii COVID-19, punem la dispozitia tuturor celor interesati un tabel cu testele identificate de ANMDMR ca fiind inregistrate in Uniunea Europeana la data de 20.04.2020.
Mentionam faptul ca, potrivit reglementarii in vigoare, respectiv Directiva 98/79/EC privind dispozitivele medicale pentru diagnostic in vitro, cu modificarile si completarile ulterioare (transpusa in legislatia nationala prin HG nr. 798/2003 privind stabilirea condiţiilor de introducere pe piaţă şi de utilizare a dispozitivelor medicale pentru diagnostic in vitro, cu modificarile si completarile ulterioare), pentru a putea fi introduse pe piata UE si implicit in Romania, dispozitivele medicale pentru diagnostic in vitro de tipul testelor trebuie sa:
– Poarte marcajul CE, marcaj care semnifica indeplinirea cerintelor aplicabile tipului de produs potrivit dispozitiilor art. 10 alin. (1) din HG nr. 798/2003, respectiv art. 4 alin. (1) din Directiva 98/79/EC;
– Producatorul din afara UE trebuie sa desemneze un reprezentant autorizat cu sediul in UE si acesta sa fie nominalizat (in declaratie, pe eticheta sau ambalaj exterior ori instructiuni de utilizare) conform prevederilor art. 31 alin. (1) si lit. B) pct. 8.4 lit. a) din Anexa nr. 1 – Cerinte esentiale din HG nr. 798/2003, care transpun dispozitiile art. 10 alin. (3) si ale lit. B) pct. 8.4. lit. a) din Anexa I din Directiva 98/79/EC;
– Sa fie inregistrate la autoritatea competenta din statul membru UE unde isi are sediul producatorul (in cazul producatorilor din UE) potrivit prevederilor art. 29 si 32 din HG nr. 798/2003, echivalentul art. 10 alin. (1) si (4) din Directiva 98/79/EC sau la autoritatea competenta din statul membru UE unde isi are sediul reprezentantul autorizat (in cazul producatorilor din afara UE) conform art. 31 si 32 din HG nr. 798/2003 echivalentul art. 10 alin. (3) si (4) din Directiva 98/79/EC.
In contextul in care aceasta lista se modifica permanent de catre Autoritatile Competente responsabile de inregistrarea acestor dispozitive medicale pentru diagnostic in vitro, va rugam sa consultati in permanenta site-ul ANMDMR pentru informatii actualizate privind testele COVID-19 inregistrate la nivelul UE.
descarca documentul…
- Anunț important
14.04.2020
În atenția persoanelor interesate
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Surgical Set, Surgical Gown, Surgical Drape, Tube Cover, Liquid Collection Pouch, Protective Coverall, Warm Blanket and Surgical Hood – clasa I steril, fabricate de producatorul Henan JoinKona Medical Products Stock Co., Ltd., China, dispozitive care fac obiectul Certificatului de conformitate CE falsificat nr. G2S 18 01 83528 008 care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte, Germania (0123) la data de 2018-04-23, valabil pana la data de 2023-04-22.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra. - Anunț important
13.04.2020
În atenția tuturor celor interesați
ANMDMR aduce la cunostinta tuturor celor interesati anuntul facut de Comisia Europeana in 03.04.2020 privind adoptarea la nivelul Comisiei Europene a unei propuneri de amanare cu 1 an a termenului de punere totala in aplicare a Regulamentului (UE) 2017/745 al Parlamentului European și al Consiliului din 5 aprilie 2017 privind dispozitivele medicale, de modificare a Directivei 2001/83/CE, a Regulamentului (CE) nr. 178/2002 și a Regulamentului (CE) nr. 1223/2009 și de abrogare a Directivelor 90/385/CEE și 93/42/CEE ale Consiliului – MDR, in scopul prioritizarii luptei impotriva Coronavirus.
Propunerea a fost transmisa spre aprobare Parlamentului European si Consiliul Europei.
descarca documentul…
- Anunț important
10.04.2020
În atenția persoanelor interesate
Inregistrarea petitiilor si solicitarilor in conditiile Legii nr. 544/2001 privind liberul acces la informatiile de interes public.
Începând cu data de 13.04.2020, pentru înregistrarea unei petiții potrivit dispozițiilor Ordonanţei Guvernului nr. 27/2002 privind reglementarea activităţii de soluţionare a petiţiilor, aprobată, cu modificări şi completări, prin Legea nr.233/2002 sau a unei solicitari în condiţiile Legii nr. 544/2001 privind liberul acces la informaţiile de interes public, în format electronic, se va folosi exclusiv Portalul ”Petitii online”!
Petițiile si solicitarile transmise prin intermediul adreselor de e-mail nu vor fi luate în considerare.
Răspunsurile ANMDMR vor fi comunicate de asemenea, în format electronic, la adresele de e-mail menționate în solicitare.
Pentru solicitările transmise în condiţiile Legii nr. 544/2001 se va preciza la rubrica ”Solicitarea dumneavoastra”, faptul că solicitarea este formulată în condițiile Legii 544/2001.
Conform art. 56 din Decretul privind instituirea stării de urgență pe teritoriul României, “pe perioada stării de urgență, termenele legale stabilite pentru soluționarea solicitărilor formulate în exercitarea liberului acces la informații de interes public, precum și a petițiilor se dublează“. - Anunț important
10.04.2020
În atenția persoanelor interesate
Ca urmare a multiplelor solicitari primite de ANMDMR de la diferite unitati sanitare/firme de distributie privind conformitatea anumitor teste pe care intentioneaza sa le achizitioneze in vederea utilizarii de catre specialistii in domeniul sanatatii in contextul testarii COVID-19, punem la dispozitia tuturor celor interesati un tabel cu testele identificate de ANMDMR ca fiind inregistrate in Uniunea Europeana la data de 30.03.2020.
Mentionam faptul ca, potrivit reglementarii in vigoare, respectiv Directiva 98/79/EC privind dispozitivele medicale pentru diagnostic in vitro, cu modificarile si completarile ulterioare (transpusa in legislatia nationala prin HG nr. 798/2003 privind stabilirea condiţiilor de introducere pe piaţă şi de utilizare a dispozitivelor medicale pentru diagnostic in vitro, cu modificarile si completarile ulterioare), pentru a putea fi introduse pe piata UE si implicit in Romania, dispozitivele medicale pentru diagnostic in vitro de tipul testelor trebuie sa:
– Poarte marcajul CE, marcaj care semnifica indeplinirea cerintelor aplicabile tipului de produs potrivit dispozitiilor art. 10 alin. (1) din HG nr. 798/2003, respectiv art. 4 alin. (1) din Directiva 98/79/EC;
– Producatorul din afara UE trebuie sa desemneze un reprezentant autorizat cu sediul in UE si acesta sa fie nominalizat (in declaratie, pe eticheta sau ambalaj exterior ori instructiuni de utilizare) conform prevederilor art. 31 alin. (1) si lit. B) pct. 8.4 lit. a) din Anexa nr. 1 – Cerinte esentiale din HG nr. 798/2003, care transpun dispozitiile art. 10 alin. (3) si ale lit. B) pct. 8.4. lit. a) din Anexa I din Directiva 98/79/EC;
– Sa fie inregistrate la autoritatea competenta din statul membru UE unde isi are sediul producatorul (in cazul producatorilor din UE) potrivit prevederilor art. 29 si 32 din HG nr. 798/2003, echivalentul art. 10 alin. (1) si (4) din Directiva 98/79/EC sau la autoritatea competenta din statul membru UE unde isi are sediul reprezentantul autorizat (in cazul producatorilor din afara UE) conform art. 31 si 32 din HG nr. 798/2003 echivalentul art. 10 alin. (3) si (4) din Directiva 98/79/EC.
In contextul in care aceasta lista se modifica permanent de catre Autoritatile Competente responsabile de inregistrarea acestor dispozitive medicale pentru diagnostic in vitro, va rugam sa consultati in permanenta site-ul ANMDMR pentru informatii actualizate privind testele COVID-19 inregistrate la nivelul UE.
descarca documentul…
- Anunț important
07.04.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul Urine Bag, Gauze Sponges, Gauze Balls, Non-woven Sponges, Gauze Bandages, Medical Eye Pad, Sterile Wound Plaster, Liquid Transfusion Plaster, Adhesive Wound Dressings, ABD Pad, Surgical Drapes, Surgical Gowns, Sterile Plastic Cover, Non-woven Face Mask – clasa I steril, fabricate de producatorul Medical Products Co., Ltd., China, dispozitive care fac obiectul Certificatului de conformitate CE falsificat nr. G2S 051736 0015 Rev.00, care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte, Germania (0123) la data de 2019-05-06, valabil pana la data de 2023-11-27.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra. - Anunț important
07.04.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu introduca pe piata din Romania dispozitive medicale de tipul In Vitro diagnostic for self testing, fabricate de producatorul Biological Pharmaceutical Co., Ltd., China, dispozitive care fac obiectul Certificatului de conformitate CE falsificat nr. V1 17 10 01684 002 care ar fi emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte, Germania (0123) la data de 2017-12-28, valabil pana la data de 2022-12-27.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra. - Anunț important
06.04.2020
În atenția tuturor importatorilor și distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale care intentioneaza sa introduca pe piata din Romania, in contextul pandemiei COVID-19, echipamente personale de protectie si kituri de testare COVID-19, ce pretind ca ar fi fost testate si certificate de Organismul Notificat SGS (0120), sa acceseze linkul https://www.sgs.com/en/news/2020/02/ppe-testing-verification si sa transmita documentele detinute catre SGS in vederea confirmarii veridicitatii acestora. Procedand astfel contribuiti inclusiv la stoparea comercializarii unui produs neconform pe intreg teritoriul Uniunii Europene.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra. - Anunț important
05.04.2020
În atenția persoanelor interesate
Dispozitivele medicale clasa I (măști, halate, combinezoane etc.) nu se mai înregistreaza în baza națională de date, pe perioada stării de urgență.
descarca documentul…
- Anunț important
02.04.2020
În atenția tuturor importatorilor si distribuitorilor de dispozitive medicale
ANMDMR atentioneaza toti importatorii si distribuitorii de dispozitive medicale sa nu intoduca pe piata din Romania dispozitive medicale de tipul Respiratory humidification devices and accessories (Disposable Patient Circuits, Transfer Unit) – clasa IIa, fabricate de producatorul Maine Holding B.V., Olanda, dispozitive care fac obiectul Certificatului de conformitate CE falsificat nr. 170724386, care ar fi emis de Organismul Notificat DQS Medizinprodukte GmbH, Germania (0297) la data 2019-02-02, valabil pana la data de 2024-02-02.
Pentru a preveni introducerea in lantul legal de distributie, mai ales in contextul pandemiei COVID-19, a unor dispozitive medicale neconforme, care nu respecta cerintele de reglementare aplicabile, va rugam sa manifestati prudenta maxima, sa consultati permanent site-ul ANMDMR pentru astfel de informari si sa va asigurati ca produsele pe care le achizitionati provin de la distribuitori avizati de institutia noastra. - Anunț important
01.04.2020
În atenția persoanelor interesate
Agentia Nationala a Medicamentului si a Dispozitivelor Medicale din Romania (ANMDMR) informeaza cu privire la schimbarea termenului limită de depunere a formularelor de declarare a activității de sponsorizare, atât pentru medicamentele de uz uman, cât și pentru dispozitivele medicale și materialele sanitare, in conformitate cu prevederile Ordinului 538/2020 pentru completarea unor ordine ale ministrului sanatatii care cuprin reglementari privind activitatile de sponsorizare in domeniul medicamentului de uz uman, al dispozitivelor medicale si al materialelor sanitare, publicat in Monitorul Oficial al Romaniei Nr 267/31.03.2020.
Astfel, noile termene limita de depunere a declaratiilor privind activitatile de sponsorizare sunt:
– 30 iunie 2020, pentru cele care privesc medicamentele de uz uman si care se transmit catre ANMDMR;
– 31 iulie 2020, in cazul dispozitivelor medicale si al materialelor sanitare, care se transmit catre Ministerul Sanatatii (MS), prin structura de specialitate din ANMDMR.
S-a modificat, de asemenea, termenul limita pana la care informatiile declarate se pot publica pe site-ul ANMDMR, respectiv MS, al entitatilor care au desfasurat activitatile de sponsorizare si al beneficiarilor acestora , dupa caz. Astfel, noile termene limita de publicare sunt:
– 30 septembrie 2020, pentru medicamentele de uz uman;
– 31 octombrie 2020, in cazul dispozitivelor medicale si al materialelor sanitare. - Anunț important
01.04.2020
În atenția persoanelor interesate
În atenția producătorilor români de dispozitive medicale care solicită Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România, punerea la dispoziție a specificațiilor tehnice, a informațiilor cu privire la materia primă utilizată sau a listelor cu furnizorii de materii prime/subansamble în vederea demarării procesului de producție.
descarca documentul…
- Anunt important
31.03.2020
În atenția tuturor importatorilor / distribuitorilor de dispozitive medicale
ANDMR, atentioneaza toti importatorii/distribuitorii de dispozitive medicale sa nu intoduca pe piata din Romania dispozitive medicale de tipul (Face Masks, Surgical Gowns, Coveralls, Caps) care fac obiectul Certificatul ui contrafacut nr. 0197/DD 60102531 0001 emis de Organismul Notificat TUV Rheinland LGA Products Gmbh, la data 2015-07-10, valabil pana la data de 2020-07-09.
Din verificarile efectuate de ANMDMR, producatorul THANYATORN SAFETY Co., Ltd. Tailanda, nu figureaza ca fiind prezent pe piata din Romania.
Pentru a preveni introducerea acestor produse in lantul legal de distributie, va rugam sa manifestati prudenta maxima si va asigurati ca produsele pe care le primiti provin de la distribui tori avizati. - Anunt important
31.03.2020
În atenția tuturor importatorilor / distribuitorilor de dispozitive medicale
ANDMR, atentioneaza toti importatorii/distribuitorii de dispozitive medicale sa nu intoduca pe piata din Romania dispozitive medicale de tipul (Face masks, Surgical Gowns, Non-woven convertible, Surgical Drapes, Melt-blown Fabric, BFE 95, BFE 98, BFE 99) care fac obiectul Certificatului falsificat nr. 0197/DD 60098386 0001 , emis de Organismul Notificat TUV Rheinland LGA Products Gmbh, la data 2020-01-21, valabil pana la data de 2025-01-20.
Din verificarile efectuate de ANMDMR, prod ucatorul NEFTEPROM – AJ PHIWES, Federatia Rusa nu figureaza ca fiind prezent pe piata din Romania.
Pentru a preveni introd ucerea acestor produse in lantul legal de distributie, va rugam sa manifestati prudenta maxi ma si va asigurati ca produsele pe care le primiti provin de la distribuitori avizati. - Anunt important
31.03.2020
În atenția tuturor importatorilor / distribuitorilor de dispozitive medicale
ANDMR, atentioneaza toti importatorii/distribuitorii de dispozitive medicale sa nu intoduca pe piata din Romania dispozitive medicale de tipul (Vital Signs Monitor, Handheld Pulse Oximeter, Fingertip Pulse Oximeter) care fac obiectul Certificatului falsificat nr. O123/G1.15.11.92582.002, emis de Organismul Notificat TUV SUD Product Service GmbH Zertifizierung Medizinprodukte Gmbh, la data 2016-06-30, valabil pana la data de 2021-06-29.
Din verificarile efectuate de ANMDMR, producatorul Ningbo Safebond Medical Co., Ltd, nu figureaza ca fiind prezent pe piata din Romania.
Pentru a preveni introducerea acestor produse in lantul legal de distributie, va rugam sa manifestati prudenta maxima si va asigurati ca produsele pe care le primiti provin de la distribuitori avizati. - Anunt important
26.03.2020
În atenția tuturor importatorilor / distribuitorilor de dispozitive medicale
ANDMR, atentioneaza toti importatorii / distribuitorii de dispozitive medicale sa nu intoduca pe piata din Romania dispozitive medicale de tipul (Face Masks, Surgical Gowns, Non-woven Caps, Non-woven Shoe Covers, Plastic Shoe Covers, Coveralls) fabricate de producatorul Medicom MTD Ltd, Federatia Rusa care fac obiectul Certificatului falsificat nr. 0197/DD 60104282 0001, emis de Organismul Notificat TÜV Rheinland LGA Products GmbH, la data 2015-10-16, valabil pana la data de 2020-10-15.
Pentru a preveni introducerea acestor produse in lantul legal de distributie, va rugam sa manifestati prudenta maxima si va asigurati ca produsele pe care le primiti provin de la distribuitori avizati. - Anunt important
26.03.2020
În atenția tuturor importatorilor / distribuitorilor de dispozitive medicale
ANDMR, atentioneaza toti importatorii / distribuitorii de dispozitive medicale sa nu intoduca pe piata din Romania dispozitive medicale de tipul (Anaesthesia Machines, Ventilators, Anaesthesia Vaporizer) care fac obiectul Certificatului falsificat nr.
0123/G1.17.12.64187.005, emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte Gmbh, la data 2018-01-17, valabil pana la data de 2023-01-08.
Din verificarile efectuate de ANMDMR, producatorul Healicom Medical Equipment Co., Ltd. China, nu figureaza ca fiind prezent pe piata din Romania.
Pentru a preveni introducerea acestor produse in lantul legal de distributie, va rugam sa manifestati prudenta maxima si va asigurati ca produsele pe care le primiti provin de la distribuitori avizati. - Anunt important
26.03.2020
În atenția tuturor importatorilor / distribuitorilor de dispozitive medicale
ANDMR, atentioneaza toti importatorii / distribuitorii de dispozitive medicale sa nu intoduca pe piata din Romania dispozitive medicale de tipul (In Vitro diagnostic test kit) care fac obiectul Certificatului falsificat nr. 0123/V1.16.08.96618.002, emis de Organismul Notificat TÜV SÜD Product Service GmbH Zertifizierung Medizinprodukte Gmbh, la data 2016-12-12, valabil pana la data de 2021-12-11.
Din verificarile efectuate de ANMDMR, producatorul Shanghai Eugene Biotech Co., LTD, China, nu figureaza ca fiind prezent pe piata din Romania.
Pentru a preveni introducerea acestor produse in lantul legal de distributie, va rugam sa manifestati prudenta maxima si va asigurati ca produsele pe care le primiti provin de la distribuitori avizati. - Anunt important
25.03.2020
În atenția tuturor importatorilor / distribuitorilor de dispozitive medicale
ANDMR, atentioneaza toti importatorii/distribuitorii de dispozitive medicale sa nu intoduca pe piata din Romania dispozitive medicale de tipul (Sterile Surgical Caps, Sterile Surgical Face Masks, Sterile Surgical Gowns, Sterile Bed Protections, Sterile Surgical Drapes, Sterile Surgical Packs) care fac obiectul Certificatului contrafacut nr. 0197/DD 60111758 0001 emis de Organismul Notificat TUV Rheinland LGA Products Gmbh, la data 2016-08-12, valabil pana la data de 2021-08-11.
Din verificarile efectuate de ANMDMR, producatorul DAARA PHARMA SUPPLIES SUA nu figureaza ca fiind prezent pe piata din Romania.
Pentru a preveni introducerea acestor produse in lantul legal de distributie, va rugam sa manifestati prudenta maxima si va asigurati ca produsele pe care le primiti provin de la distri buitori avizati. - Anunt important
25.03.2020
În atenția persoanelor interesate
Având în vedere evoluția situației epidemiologice caracterizată prin creșterea importantă a numărului de persoane infectate cu coronavirusul COVID-19 (atât prin circulația virusului pe teritoriul național cât și prin importarea acestuia odată cu revenirea în țară a persoanelor posibil infectate) și analizând măsurile necesare în vederea întârzierii propagării pandemiei, conducerea Agenției Naționale a Medicamentului și a Dispozitivelor Medicale din România a emis Decizia nr. 332 din data de 16.03.2020.
Conform acestei decizii, activitatea de inspecție și control a Direcției Generale Dispozitive Medicale și Direcției Inspecție Farmaceutică se suspendă pe o perioadă de 30 de zile de la data emiterii, pentru a evita expunerea angajaților și a reduce riscul de infectare a personalului și a beneficiarilor cu noul coronavirus.
În consecință, în această perioadă specialiștii ANMDMR nu se vor mai deplasa la sediul unităților sanitare pentru controlul prin verificare tehnică a dispozitivelor medicale în București și în alte localități. De asemenea nu se vor mai face evaluări ale dispozitivelor medicale din dotarea unităților mobile de intervenție la sediul ANMDMR-DGDM din sos. Titulescu, nr. 58, Sector 1.
Pentru toate dispozitivele medicale care au fost deja evaluate tehnic de către specialiștii noștri, au fost emise sau sunt în curs de emitere documentele specifice (aviz de utilizare/ buletin de verificare periodică/ raport de încercări-negativ). Documentele vor fi transmise în copie scanată pe e-mail, iar originalele vor intra în posesia beneficiarilor prin intermediul Poștei Române.
Mai precizăm că ANMDMR va transmite:
– O informare privind suspendarea activității de verificare tehnică a dispozitivelor medicale, către Casa Naţională de Asigurări de Sănătate, astfel încât beneficiarilor care se află în relație contractuală cu casele de sănătate să nu li se mai condiționeze prelungirea contractului de prezentarea documentelor emise de ANMDMR.
– O informare către Registrul Auto Roman (RAR) cu privire la suspendarea activității de verificare tehnică a dispozitivelor medicale și a dotării minime obligatorii din unitățile mobile de intervenție și emitere a avizului de utilizare.
Recomandăm de asemenea beneficiarilor să nu mai depună cererile tip pentru obținerea buletinului de verificare sau a avizului de utilizare întrucât acestea trebuie tarifate, însă inspectorii ANMDMR nu vor putea să le dea curs pe perioada de suspendare a activității. - Anunt important
23.03.2020
In atentia persoanelor interesate
In atentia atelierelor/fabricilor care confectioneaza masti de protectie din in, bumbac, panza si le comercializeaza/doneaza ca alternative la mastile chirurgicale
Revenim la anunturile postate in 18.03.2020: Conditii de introducere pe piata a mastilor faciale de uz medical si In atentia potentialilor producatori de masti faciale de uz medical, si facem urmatoarele precizari succinte.
descarca documentul…
- Anunț important
19.03.2020
În atenția persoanelor interesate
Unde si cum sa purtam o masca chirurgicala pentru a ne proteja de COVID 19
- Anunț important
18.03.2020
În atenția persoanelor interesate
Ca urmare a atentionarilor primite de ANMDMR de la diferite autoritati ale Statelor Membre UE privind existenta pe piata europeana a unor teste pentru depistarea noului Coronavirus (Covid-19) falsificate sau puse ilegal pe piata, fara a indeplini cerintele legale si de reglementare, ANMDMR, in calitate de Autoritate Competenta in Romania in domeniul dispozitivelor medicale, solicita tuturor societatilor comerciale si unitatilor sanitare care comercializeaza sau achizitioneaza astfel de teste sa verifice provenienta testelor si conformitatea lor cu cerintele legale si de reglementare.
In acest sens, avem rugamintea sa efectuati o evaluare preliminara a documentelor insotitoare ale acestor teste, tinand cont de urmatoarele informatii generale pe care vi le aducem la cunostinta:
1. Potrivit Art. 10 (1) din HG 798/2003 echivalentul Art. 4 (1) din Directiva 98/79/EC, toate dispozitivele medicale pentru diagnostic in vitro (IVD-uri) pentru a putea fi introduse pe piata UE si implicit in Romania trebuie sa poarte marcajul CE, marcaj care semnifica faptul ca aceste IVD-uri au fost supuse evaluarii din punct de vedere al conformitatii cu cerintele aplicabile din HG 798/2003 / Directiva 98/79/EC. Potrivit Art. 50 (3) din HG 798/2003 echivalentul Art. 16 (2) din Directiva 98/79/EC, IVD-urile care poarta marcajul CE urmat de un numar format din 4 cifre sunt dispozitive medicale care au fost evaluate din punct de vedere al conformitatii de producator, cu implicarea unui Organism Notificat la Bruxelles pe Directiva 98/79/EC. Pentru IVD-urile marcate CE va rugam sa solicitati declaratia de conformitate a producatorului, iar pentru cele purtatoare de marcaj CE urmat de un numar format din 4 cifre, va rugam sa solicitati declaratia de conformitate si certificatul de conformitate CE emis de Organismul Notificat implicat in evaluarea acelui IVD.
Va atragem atentia ca, potrivit cerintelor de reglementare cuprinse la Cap. IV din HG 798/2003 echivalentul Art. 9 in Directiva 98/79/EC, sunt purtatoare de marcaj CE urmat de un numar format din 4 cifre NUMAI IVD-urile cuprinse in Anexa II a acestei directive si IVD-urile de autotestare.
Pentru Certificatul de conformitate CE, numele Organismului Notificat al carui numar de identificare este cel de dupa marcajul CE (cel format din 4 cifre) il puteti verifica de pe site-ul web al Comisiei Europene https://ec.europa.eu/growth/tools-databases/nando/ , la sectiunea Body – criteriu de cautare: numarul de identificare din marcajul CE.
2. Potrivit Art. 31 (1) din HG 798/2003 echivalentul Art. 10 (3) din Directiva 98/79/EC, pentru introducerea pe piata a oricarui IVD, daca producatorul nu are sediul in UE, trebuie sa desemneze un reprezentant autorizat cu sediul in UE. Va rugam sa verificati identificarea acestui reprezentant autorizat in documentele provenite de la producator.
3. In conditiile de la pct. 2, potrivit Art. 31, 32 din HG 798/2003 echivalentul Art. 10 (3), (4) din Directiva 98/79/EC pentru a putea fi introduse legal pe piata UE, aceste IVD-uri trebuie sa fie inregistrate la Autoritatea Competenta din Statul Membru in care reprezentantul autorizat isi are sediul. In conditiile in care producatorul are sediul in UE, potrivit Art. 29, 32 din HG 798/2003, echivalentul Art. 10 (1), (4) din Directiva 98/79/EC aceste IVD-uri trebuie sa fie inregistrate la Autoritatea Competenta din Statul Membru in care isi are sediul producatorul.
Va rugam sa solicitati dovada de inregistrare.
https://www.anm.ro/dispozitive-medicale/legislatie/legi-ordonante-si-hotarari-de-guvern/
Pentru a nu incarca suplimentar activitatea Autoritatilor Competente din Statele Membre cu intrebari privind legalitatea introducerii pe piata UE a unui IVD anume, in conditiile in care situatia la nivel european este una CRITICA, va rugam ca anterior solicitarii de informatii la ANMDMR cu privire la conformitatea unui IVD, sa va asigurati dvs. ca detineti pentru IVD-ul respectiv pe care intentionati sa il importati/achizitionati toate documentele care demonstreaza respectarea cerintelor de reglementare mentionate anterior (1-3).
In lipsa oricareia dintre informatiile/documentele obligatorii mentionate la pct. 1-3, respectivele IVD-uri nu pot fi introduse pe piata UE/Romania.
In conditiile in care dupa solicitarile facute de dvs. catre producatori, in vederea efectuarii evaluarii de mai sus constatati ca pentru anumite IVD-uri nu va sunt puse la dispozitie toate documentele care atesta indeplinirea cerintelor de reglementare de la pct. 1-3 mentionate anterior, va rugam sa sesizati ANMDMR in vederea efectuarii de verificari suplimentare, inainte de achizitionarea acestor teste. - Anunt important
18.03.2020
În atenția persoanelor interesate
Condiții de introducere pe piață a măștilor faciale de uz medical
Anterior introducerii pe piata a mastilor faciale de uz medical (dispozitiv medical clasa I), producatorul are obligaţia să se înregistreze la ANMDMR, conform art. 4 al OMS nr. 1009/2016 privind înregistrarea dispozitivelor medicale în baza nationala de date.
descarca documentul…
- Anunț important
18.03.2020
În atenția potentialilor producatori de masti faciale de uz medical
Conform articolului 1 alineatul (6) din Directiva 93/42 / CEE privind dispozitivele medicale, prezenta directivă nu se aplica echipamentelor de protecție personala reglementate de Regulamentul 2016/425.
Pentru a decide daca un produs intra sub incidenta Directivei 93/42 / CEE sau a Regulamentului 2016/425, se tine seama de scopul intentionat al produsului. Ca urmare a acestei clauze, un produs dat este reglementat fie de Regulamentul 2016/425, fie de Directiva 93/42 / CEE.
descarca documentul…
- Anunț important
12.03.2020
În atenția persoanelor interesate
Având in vedere contextul epidemiologic actual, pentru evitarea pe cat posibil a deplasărilor cu documente, ANMDMR a luat decizia de restrângere, începând cu 13 martie până la 15 aprilie a.c. (cu posibilitatea de prelungire, daca situația o va impune), a activității cu publicul a serviciului Registratura. Documentele se pot transmite:
Medicamente de uz uman
– prin posta la adresa Str. Av. Sănătescu nr. 48, sector 1, 011478 București,
– prin fax la nr.: +4021-316.34.97
– electronic:
– către registratura@anm.ro
– prin CESP
– prin punctul unic de contact electronic (PCU-e).
Dispozitive medicale
– prin posta la adresa: Bd. Nicolae Titulescu 58, Sector 1, 011144, Bucuresti, Romania
– prin fax la nr.: +4021-222.86.83
– electronic:
– către dgdm@anm.ro
– prin punctul unic de contact electronic (PCU-e).
Pentru a intra în posesia documentelor emise de ANMDMR, se recomandă, în această perioadă, apelarea la serviciile de curierat.
De asemenea, anunțăm pe toți cei interesați că pentru aceeași perioadă, se suspendă audiențele.
Vă mulțumim pentru înțelegere și colaborare. - Anunt important
24.02.2020
În atenția persoanelor interesate
Clarificari referitoare la prevederile art. 16 din Regulamentul UE 2017/745 (in continuare MDR) referitoare la cerintele de traducere a etichetei/instructiunilor de utilizare si la reambalarea dispozitivelor medicale
Gasiti in continuare raspunsurile punctuale ale ANMDMR la solicitarile / intrebarile dvs. referitoare la prevederile art. 16. Astfel:
Afirmatie (text preluat dintr-o adresa de solicitare de clarificari):
„In conformitate cu articolul 16 alineatul (1) din MDR, distribuitorii […] isi asuma obligatiile producatorului daca modifica un dispozitiv deja introdus pe piata […] si alineatele 3 si 4 ale MDR, distribuitorii trebuie sa:
– informeaze producatorul si autoritatea competentă a statului membru, cu cel putin 28 de zile înainte de introducerea dispozitivului în statul membru;
– la cerere, furnizează producatorului si autoritatii competente un exemplar sau macheta a dispozitivului reetichetat sau reambalat, inclusiv orice eticheta si instructiuni de utilizare a dispozitivului, traduse
– transmite autoritatii competente un certificat, eliberat de un organism notificat si desemnat pentru tipul de dispozitive, care atesta faptul ca sistemul de management al calitatii al distribuitorului sau al importatorului este în conformitate cu cerintele prevazute la alineatul (3).
– indice pe dispozitiv adresa locului unde s-a desfașurat activitatea de reetichetare;
– se asigura ca dispun de un sistem de management al calitatii care include proceduri care asigura faptul că traducerea informatiilor este corecta si actualizata si ca activitatile de reetichetare sunt efectuate prin mijloace si in conditii care conserva starea originala a dispozitivului si ca ambalajul dispozitivului reambalat nu este defect, de slaba calitate sau cu aspect neingrijit. Sistemul de management al calitatii consta, printre altele, din proceduri prin care se asigura ca distribuitorul sau importatorul este informat cu privire la orice actiune corectiva întreprinsa de catre producator în legatura cu dispozitivul în cauza, pentru a solutiona probleme legate de siguranta sau pentru ca acesta sa devina conform cu prezentul regulament.”
Corectie la afirmatia de mai sus: Alin. (3) si (4) ale art. 16 nu sunt conexate alin. (1). Potrivit alin. (1), in conditiile in care un distribuitor, un importator sau o alta persoana fizica sau juridica pune la dispozitie pe piata un dispozitiv sub numele sau, denumirea sa comerciala înregistrata sau marca sa comerciala înregistrata, modifica scopul propus al unui dispozitiv deja introdus pe piata sau pus în functiune sau modifica un dispozitiv deja introdus pe piata sau pus in functiune astfel incat conformitatea cu cerintele aplicabile poate fi afectata, devine producator. In acest caz trebuie indeplinite toate cerintele din MDR aplicabile producatorului.
Exceptie de la prevederea anterioara fac cazurile în care distribuitorul sau importatorul incheie un acord cu un producator prin care producatorul este identificat ca atare pe eticheta și este responsabil pentru indeplinirea cerintelor impuse producatorilor în MDR, insa este specificata pe eticheta marca comerciala a distribuitorului/ importatorului.
Alin. (3) si (4) ale art. 16 sunt conexate alin. (2) literele a) si b) si se refera doar la activitatea de traducere a informatiilor puse la dispozitie de catre producator, sau la modificarea ambalajului exterior al unui dispozitiv introdus deja pe piata.
Întrebare 1: Traducerile : Ce fel de sistem de management al calitatii este necesar pentru traducere? Ar fi ISO 9001 suficient?
Raspuns 1: Deoarece MDR impune obligativitatea pentru distribuitorii si importatorii care desfasoara activitatile mentionate la art. 16, alin. (2) literele a) si b), sa detina si sa transmita Autoritatii Competente un certificat eliberat de un organism notificat si desemnat pentru tipul de dispozitive comercializate, nu este suficient ISO 9001. Sistemul de management al calitatii va fi certificat in conformitate cu ISO 13485, deoarece se refera la cerinte specifice dispozitivelor medicale.
Aceasta cerinta se regaseste intr-un proiect de act normativ care a fost transmis la Ministerul Sanatatii spre promovare.
Întrebare 2: Ar fi suficienta traducerea pe propria raspundere? Sau distribuitorul ar putea avea doar procedura interna a procesului de traducere?
Raspuns 2: Avand in vedere obligativitatea certificarii sistemului de management al calitatii, procedura care descrie activitatea de traducere face parte din acest sistem. Traducerile prevazute la art. 16 (2) se vor efectua de catre traducatori atestati/ autorizati in domeniul medical/tehnic, dupa caz.
Întrebare 3: Locul de reetichetare: Ce fel de sistem de management al calitatii este necesar pentru activitatile de reetichetare? Ar fi suficient certificatul GMP pentru ambalarea medicamentelor secundare? Ar fi ISO 9001 suficient? Sau distribuitorul ar putea avea doar procedura interna a activitatilor de reetichetare?
Raspuns 3: Aceleasi raspunsuri 1 si 2.
Întrebare 4: Din mai 2020, toate dispozitivele medicale ar trebui sa fie re-etichetate de distribuitori pe baza MDR?
Raspuns 4: Reetichetarea la care face trimitere art. 16 al MDR se refera la situatia in care este necesara traducerea etichetei sau/si a instructiunilor de utilizare, atunci cand versiunea in limba romana a instructiunilor nu este pusa la dispozitie direct de catre producator.
Întrebare 5: În cazul introducerii pe piata de catre distribuitori a dispozitivelor medicale eliberate pe baza MDD, procesul de etichetare ar putea fi bazat pe Directiva 93/42/EEC (MDD) si reglementarile locale?
Raspuns 5: Incepand cu 26 mai 2020 este aplicabil art. 16 al MDR, indiferent daca dispozitivele medicale au fost introduse pe piata in baza MDD sau MDR.
Întrebare 6: În cazul introducerii pe piata de catre distribuitor a dispozitivelor medicale eliberate pe baza MDR, procesul de etichetare ar trebui sa se bazeze pe MDR?
Raspuns 6: Acelasi raspuns 5. - Anunt important
10.02.2020
In atentia producatorilor romani de dispozitive medicale clasa I – tranzitia la noul Regulament privind dispozitivele medicale – MDR 2017/745
Rectificare la anuntul postat in data de 14.10.2019 referitor la: Clarificari cu privire la prevederile art. 120 alin. (4) al MDR 2017/745 – Dispoziții tranzitorii
Ca urmare a publicarii in Jurnalul Oficial al Uniunii Europene L334/165 din 27.12.2019 a documentului:
Rectificare la Regulamentul (UE) 2017/745 al Parlamentului European și al Consiliului din 5 aprilie 2017 privind dispozitivele medicale, de modificare a Directivei 2001/83/CE, a Regulamentului (CE) nr. 178/2002 și a Regulamentului (CE) nr. 1223/2009 și de abrogare a Directivelor 90/385/CEE și 93/42/CEE ale Consiliului,
Pentru dispozitivele medicale incadrate in clasa I in conformitate cu Directiva 93/42/CEE, dispozitive care potrivit prevederilor MDR 2017/745 trebuie reclasificate intr-o clasa de risc superioara, trebuie avute in vedere urmatoarele prevederi:
Un dispozitiv medical incadrat in clasa I potrivit Directivei 93/42/CEE, pentru care declaratia de conformitate a fost intocmita inainte de 26 mai 2020 si care, in procedura de evaluare a conformitatii potrivit MDR 2017/745, necesita implicarea unui organism notificat, poate fi introdus pe piata sau pus in functiune pana la 26 mai 2024, cu urmatoarele conditii:
– de la 26 mai 2020 acesta sa fie in continuare in conformitate cu prevederile Directivei 93/42/CEE
si
– sa nu existe modificari semnificative ale proiectului dispozitivului sau ale scopului sau propus.
Cu toate acestea, de la 26 mai 2020, pentru aceste dispozitive, cerintele privind supravegherea ulterioara introducerii pe piata, supravegherea pietei, vigilenta, inregistrarea operatorilor economici si a dispozitivelor se aplica din MDR 2017/745 in locul cerintelor corespondente din Directiva 93/42/CEE.
Dispozitivele medicale de clasa I introduse pe piata inainte de 26 mai 2020 in conformitate cu Directiva 93/42/CEE și dispozitivele medicale de clasa I introduse pe piata incepand cu 26 mai 2020, in conformitate cu alineatul (3) al art. 120 din MDR 2017/745, pot fi in continuare puse la dispozitie pe piata sau puse in functiune pana la 26 mai 2025.
Potrivit MDR 2017/745, „introducere pe piata” reprezinta prima punere la dispozitie pe piata Uniunii a unui dispozitiv, altul decat un dispozitiv care face obiectul unei investigații. Astfel, un dispozitiv medical se considera introdus pe piata in momentul in care paraseste depozitul producatorului si este pus la dispozitia distribuitorilor sau utilizatorilor.
Ramane in continuare valabil anuntul din 14.10.2019 cu privire la dispozitivele medicale clasa I, incadrate conform regulilor de clasificare MDR 2017/745 si anume: pentru a fi introduse pe piata dupa data de 26 mai 2020, producatorul trebuie sa elaboreze dosarul de produs conform cerintelor MDR 2017/745, sa emita declaratia de conformitate si sa inregistreze produsele in baza nationala de date. - Anunt important
04.02.2020
În atenția persoanelor interesate
Clarificări cu privire la dispozitivele medicale second-hand alimentate de la rețeaua de energie electrică, altele decât cele generatoare de radiații ionizante și RMN:
În conformitate cu art. 931 alin. (1) și (2) din legea 95 /2006 republicată – privind reforma în domeniul sănătății, “dispozitivele medicale second-hand, furnizate gratuit sau contra cost, se comercializează, se pun în funcţiune şi sunt utilizate numai în urma evaluării performanţelor acestora de către ANMDMR şi în baza avizului eliberat de către aceasta.” “Dispozitivele medicale second-hand prevăzute la alin. (1), comercializate şi/sau puse în funcţiune, trebuie să poarte marcajul de conformitate CE şi să fi fost supuse evaluării conformităţii înainte de introducerea pe piaţă, potrivit normelor europene privind dispozitivele medicale.”
În legislația specifică dispozitivelor medicale nu există o definiție a dispozitivelor medicale second-hand. În accepțiunea ANMDMR, dispozitivele medicale second-hand sunt dispozitivele medicale care au fost deja puse pe piață, deținute și utilizate în prealabil și care sunt ulterior distribuite, cu sau fără plată, pentru utilizare subsecventă, în acelaşi scop pentru care au fost fabricate. Aceste produse sunt considerate deja cu marcaj CE și introduse pentru prima dată pe piață și nu necesită marcajul CE de către noul lor proprietar.
Ca urmare, necesită obținerea avizului de utilizare dispozitivele medicale second-hand care sunt puse la dispoziție pe piața din România / puse în funcțiune, pentru prima dată.
Pentru a preveni eventuale întârzieri în desfășurarea activității operatorilor economici/unităților sanitare și pentru a nu genera activități repetitive (de ex. același control/verificări de fiecare dată când se schimbă proprietarul/locația, uneori și la interval de 1 luna), venim cu precizarea situațiilor în care nu este necesar și nu se va solicita de la ANMDMR aviz de utilizare:
1. Dacă s-a schimbat proprietarul/beneficiarul însă dispozitivele medicale au fost noi cu garanție acordată de producător/reprezentant producător și au fost introduse pe piața din România și puse în funcțiune conform prevederilor legale. Proprietarul/beneficiarul are obligația asigurării trasabilității provenienței dispozitivului medical.
2. Dispozitivele medicale au fost second-hand deținute și utilizate în prealabil, ieșite din perioada de garanție acordată de producător/reprezentatul producătorului, au obținut avizul de utilizare la punerea la dispoziție/punerea în funcțiune pentru prima dată, iar ulterior s-au schimbat proprietarii/beneficiarii. (ANMDMR evaluează o singură dată pentru un dispozitiv medical second-hand starea generală, etichetarea/identificarea, marcajul CE, integritatea fizică, funcționalitatea și accesoriile, parametrii definitorii de securitate electrică / performanță, etc.)
Pentru dispozitivele medicale second-hand care au obținut aviz de utilizare dar se încadrează în categoriile de dispozitive medicale supuse controlului prin verificare periodică în conformitate cu ordinul nr. 308 / 2015, proprietarul/beneficiarul are obligația să depună cerere în vederea obținerii buletinului de verificare periodică emis de ANMDMR.
Pentru toate dispozitivele medicale trebuie respectate prevederile art. 933 din Legea 95/2006 privind reforma în domeniul sănătății.
Art. 933 – (1) În vederea asigurării nivelului de securitate şi performanţă adecvat scopului pentru care sunt realizate dispozitivele medicale şi a evitării generării de incidente, utilizatorii au obligaţia:
a) de a utiliza dispozitivele medicale numai în scopul pentru care au fost realizate;
b) de a se asigura că dispozitivele medicale sunt utilizate numai în perioada de valabilitate a acestora, când este cazul, şi că nu prezintă abateri de la performanţele funcţionale şi de la cerinţele de securitate aplicabile;
c) de a aplica un program de supraveghere a dispozitivelor medicale care să ţină seama de riscul acestora pentru pacient, de domeniul de utilizare şi de complexitatea acestora, potrivit normelor metodologice în vigoare;
d) de a asigura verificarea periodică, întreţinerea şi repararea dispozitivelor medicale cu unităţi avizate pentru efectuarea acestor servicii;
e) de a comunica producătorilor şi structurii de specialitate orice incident survenit în timpul utilizării;
f) de a raporta toate dispozitivele medicale existente în unitate, înregistrate în evidenţele contabile ca mijloace fixe, indiferent de modul de procurare a acestora, conform normelor metodologice aprobate prin ordin al ministrului sănătăţii;
g) de a asigura un sistem documentat de evidenţă privind dispozitivele medicale utilizate, reparate şi verificate, potrivit normelor metodologice în vigoare.
(2) Excepţie de la prevederile alin. (1) fac dispozitivele medicale care se găsesc la utilizator pentru investigare clinică sau evaluare a performanţei în vederea certificării şi care se supun cerinţelor reglementărilor sau, după caz, procedurii de evaluare a conformităţii prevăzute în reglementarea tehnică aplicabilă.
(3) Utilizatorii de dispozitive medicale trebuie să se asigure că pentru dispozitivele medicale puse în funcţiune şi utilizate se asigură piese de schimb şi că există unităţi avizate pentru efectuarea service-ului. - Anunt important
14.10.2019
In atentia producatorilor romani de dispozitive medicale clasa I – tranzitia la noul Regulament privind dispozitivele medicale – MDR 2017/745
Clarificari cu privire la prevederile art. 120 alin. (4) al MDR 2017/745 – Dispoziții tranzitorii
”Dispozitivele introduse pe piață în mod legal în temeiul Directivelor 90/385/CEE și 93/42/CEE înainte de 26 mai 2020 și dispozitivele introduse pe piață începând cu 26 mai 2020 în baza unui certificat, astfel cum este menționat la alineatul (2) din prezentul articol, pot fi în continuare puse la dispoziție pe piață sau puse în funcțiune până la 27 mai 2025.”
Aceasta derogare nu se aplica dispozitivelor medicale clasa I introduse pe piata inainte de 26 mai 2020 in baza declaratiei de conformitate emisa de producator. Se aplica dispozitivelor medicale clasa I cu functie de masurare (Im) sau clasa I steril (Is), introduse pe piata in baza unui certificat emis de un organism notificat. Declaratia de conformitate emisa de producator nu poate fi asimilata unui certificat de marcaj CE emis de un organism notificat.
Pentru a fi introduse pe piata dupa data de 26 mai 2020, producatorul dispozitivelor medicale clasa I, incadrate conform regulilor de clasificare MDR, trebuie sa elaboreze dosarul de produs conform cerintelor MDR, sa emita declaratia de conformitate si sa inregistreze produsele in baza nationala de date.
Aceasta derogare nu se aplica dispozitivelor medicale introduse pe piata inainte de 26 mai 2020 ca si dispozitive medicale clasa I si care, conform MDR urmeaza sa fie incadrate intr-o clasa superioara de risc.
Mai pot fi utilizate si mentinute pe piata ulterior datei de 26 mai 2020 doar acele dispozitive medicale clasa I care la data de 26 mai 2020 se afla in stoc in institutiile sanitare sau la distribuitori.
Aceasta derogare nu se aplica produselor care contin sau constau din materiale biologice viabile, inclusiv microorganisme, bacterii, ciuperci sau virusuri vii, in scopul indeplinirii sau sprijinirii scopului propus al produsului, introduse pe piata inainte de 26 mai 2020 ca si dispozitive medicale. Conform art. 1 alin. (6), lit. (h) din MDR, aceste produse nu intra sub incidenta MDR. Mai pot fi utilizate si mentinute pe piata ulterior datei de 26 mai 2020 doar acele produse din această categorie care la data de 26 mai 2020 se afla in stoc in institutiile sanitare sau la distribuitori. - Anunt important
06.09.2019
In atentia tuturor distribuitorilor de dispozitive medicale si utilizatorilor
In data de 06 august 2019, ANMDMR a fost informata despre un caz de furt de dispozitive medicale, anchetat de autoritatile din Spania, dupa cum urmeaza:
PRODUS SERIE
1 FUJIFILM EG-530 FP 3G374A844
2 FUJIFILM EG-530 FP 1G374K036
3 FUJIFILM EG-530 FP 1G374K552
4 FUJIFILM EG-530 FP 1G374K903
5 FUJIFILM EC-530 FL 1C654K113
6 FUJIFILM EC-530 FL 4C654A221
7 FUJIFILM EC-530 FL 3C654A381
8 FUJIFILM EC-530 FL 1C654K195
9 FUJIFILM EC-530 FL 1C654K198
10 FUJIFILM EC-530 FL 1C654K444
Pentru a preveni reintroducerea acestor produse in lantul legal de distributie, va rugam sa manifestati prudenta maxima si va asigurati ca produsele pe care le primiti provin de la distribuitori avizati. In cazul in care primiti oferte suspecte, va rugam sa ne informati de urgenta. - Anunt important
30.08.2019
In atentia persoanelor interesate
Incepand cu 28.08.2019, solicitarile pentru emiterea unui certificat de libera vanzare dispozitive medicale vor fi insotite de documentele ce sustin solicitarea si de Formularul “Cerere pentru eliberarea unui certificate de libera vanzare dispozitive medicale”, completat. Formularul poate fi descarcat de la adresa https://www.anm.ro/dispozitive-medicale/formulare-si-tarife/. Nu vor fi inregistrate solicitarile ce nu vor fi insotite de acest formular. - Anunt important
04.07.2019
In atentia persoanelor interesate
ANMDM informeaza cu privire la dispozitivele medicale DERMAPEN 4 (MicroNeedles), producator EQUIPMED USA, SUA
Potrivit unei anchete desfasurate de ANMDM ca urmare a identificarii pe piata din Romania a dispozitivelor medicale DERMAPEN 4 (MicroNeedles), producator EQUIPMED USA, SUA si a informatiilor obtinute cu aceasta ocazie de la Organismul Notificat TÜV Süd Product Service GmbH, Germania (0123), marcajul CE0123 este aplicat incorect pe aceste produse, acestea nefiind evaluate din punct de vedere al conformitatii de acest Organism Notificat.
In aceste conditii,dispozitivele medicale DERMAPEN 4 (MicroNeedles),producator EQUIPMED USA, SUA nu au urmat procedura de evaluare a conformitatii aplicabila clasei de risc, potrivit cerintelor de reglementare din Directiva 93/42/EEC privind dispozitivele medicale, cerinte obligatorii in vederea introducerii pe piata Uniunii Europene a dispozitivelor medicale.
Avand in vedere posibilul impact negativ asupra sanatatii persoanelor, ANMDM atentioneaza persoanele fizice, unitatile sanitare, cabinetele medicale si societatile comerciale cu activitati de comercializare dispozitive medicale sa nu achizitioneze sau sa opreasca imediat de la utilizare si sa returneze la furnizori dispozitivele medicale DERMAPEN 4 (MicroNeedles), producator EQUIPMED USA, SUA purtatoare de marcaj CE0123, precum si sa transmita de urgenta la ANMDM orice informatie detinuta referitoare la aceste produse (ex. lantul de distributie / data achizitiei / loturile etc). - Anunt important
04.07.2019
In atentia persoanelor interesate
Tabel cu unitatile (unitati sanitare, producatori, importatori, distribuitori, prestatori de servicii – dispozitive medicale) sanctionate cu amenda contraventionala de Departamentul Reglementare, Autorizare, Supraveghere Piata DM din cadrul ANMDM, in perioada 01.01.2019 – 30.06.2019.
descarca documentul…
- Anunt important
02.07.2019
In atentia profesionistilor din domeniul sanatatii si institutiilor sanitare
Comisia Europeana a publicat Fisa informativa pentru profesionistii din domeniul sanatatii si institutiile sanitare cu privire la modificarea legislatiei privind dispozitivele medicale.
Gasiti in acest document informatii cu privire la principalele modificari aduse de noile regulamente, la etapele de tranzitie si la aplicabilitate.
descarca documentul…
- Anunt important
09.05.2019
In atentia persoanelor interesate
lnregistrarea o singura data in baza nationala de date a dispozitivelor medicale
Referitor la anuntul din data de 17.04.2019 privind notificarea ANMDM o singura data cu privire la punerea in functiune pe teritoriul Romaniei, recomandam ca anterior depunerii dosarelor de notificare sa consultati Baza nationala de date a dispozitivelor medicale, accesand link-ul: https://dispozitive.anm.ro/. Daca dispozitivul medical pe care l-ati pus in functiune se regaseste inregistrat in baza de date, nu mai este necesar sa depuneti formularul F3 in vederea notificarii. - Anunt important
03.05.2019
In atentia persoanelor interesate
Clarificari privind documentele depuse de furnizorii de dispozitive medicale la licitatii
Ca urmare a multiplelor informatii ajunse in atentia Agentiei Nationale a Medicamentului si a Dispozitivelor Medicale (ANMDM), conform carora in cadrul procedurilor de achizitie (directa / licitatie publica) desfasurate de unitatile sanitare din Romania se solicita, ca document eliminatoriu, dovada obtinuta de furnizor de la ANMDM ca urmare a notificarii privind punerea in functiune a respectivului dispozitiv medical, efectuate potrivit Ordinului ministrului sanatatii nr. 1009/2016 (OMS 1009/2016) privind inregistrarea dispozitivelor medicale in baza nationala de date, atragem atentia urmatoarelor prevederi legale in vigoare:
descarca documentul…
- Anunt important
17.04.2019
In atentia persoanelor interesate
Avand in vedere obligativitatea respectarii prevederilor art. 9 ale OMS nr. 1009/2016 privind inregistrarea dispozitivelor medicale in baza nationala de date, in conformitate cu dispozitiile art. 2 pct. 8 din HG nr. 54/2009 privind conditiile introducerii pe piata a dispozitivelor medicale si ale art. 2 pct. 27 din Regulamentul (UE) 2017/745 al Parlamentului European si al Consiliului din 5 aprilie 2017 privind dispozitivele medicale, de modificare a Directivei 2001/83/CE, a Regulamentului (CE) nr. 178/2002 si a Regulamentului (CE) nr. 1223/2009 si de abrogare a Directivelor 90/385/CEE si 93/42/CEE ale Consiliului, va comunicam urmatoarele:
ANMDM va fi notificata o singura data, cu privire la punerea in functiune pe teritoriul Romaniei a dispozitivelor medicale de catre producator, reprezentantul autorizat al producatorului, importator sau distribuitor, atunci cand dispozitivul medical este pus la dispozitia utilizatorului final. - Anunt important
11.04.2019
In atentia persoanelor interesate
Ca urmare a informatiilor primite de la National Institute of Pharmacy and Nutrition Directorate of Device Testing and Clinical Engineering, Ungaria (EMKI), Organismul Notificat 1011 implicat in evaluarea conformitatii dispozitivelor medicale Suturi chirurgicale neresorbabile cu / fara ac (Non-absorbable surgical sutures with and without needles), producator ASPIDE SUTURES, Franta cu cerintele aplicabile din Directiva 93/42/EEC privind dispozitivele medicale, conform carora Certificatul de conformitate EC nr. 5-755-200-1403 emis de acest organism in data de 28.03.2014 (valabil pana la 27.03.2019) a fost retras incepand cu data de 30.09.2016, pentru asigurarea protectiei pacientilor, ANMDM, in calitate de Autoritate Competenta in Romania in domeniul dispozitivelor medicale, solicita tuturor unitatilor sanitare si societatilor comerciale care au achizitionat suturi chirurgicale nesterile sau sterile fabricate de acest producator dupa data de 30.09.2016 sa le opreasca imediat de la utilizare si sa le returneze societatilor distribuitoare. - Anunt important
29.03.2019
In atentia persoanelor interesate
ANMDM informeaza cu privire la utilizarea produsului MEAPLASMA TM Blood collection systems
In urma controalelor de supraveghere de piata desfasurate de inspectorii ANMDM, au fost identificate produsele MEAPLASMA TM Blood collection systems (denumire de pe eticheta ambalajului colectiv)/ PRP kit MEAPLASMA TM (denumire care se regaseste in instructiunile de utilizare), producator Zhejiang Gongdong Medical Technology Co., Ltd, China, neconforme.
Dispozitivele medicale au fost comercializate si utilizate in scopul obtinerii de plasma imbogatita din sangele pacientului, plasma care se reinjecteaza in organism, in conditiile in care atat Organismul Notificat TUV SUD Product Service GmbH, Germania (0123) cat si Reprezentantul autorizat in Uniunea Europeana al producatorului Zhejiang Gongdong Medical Technology Co., Ltd, China, respectiv Shanghai International Holding corp.GmbH (Europe)- Germania au declarat ca acest dispozitiv medical nu este destinat reinjectarii plasmei în pacient.
In temeiul art.14 si urmatoarele din HG 306/2011 privind unele masuri de supraveghere a pietei produselor reglementate de legislatia Uniunii Europene care armonizeaza conditiile de comercializare a acestora, ANMDM a decis interzicerea introducerii pe piaţă/punerii in functiune, distributiei/comercializarii si utilizarii dispozitivelor medicale MEAPLASMA TM Blood collection systems.
Avand in vedere clasa mare de risc a produselor implicate si faptul ca nu au fost derulate proceduri de evaluare a conformitatii in scopul demonstrarii ca daca sunt utilizate în conditiile si in conformitate cu scopul propus nu compromit starea clinica sau siguranta pacientilor ori siguranta si sanatatea utilizatorilor, ANMDM solicita persoanelor fizice, unitatilor sanitare si societatilor comerciale care au achizitionat aceste tipuri de produse sa le opreasca imediat de la utilizare si sa le returneze societatilor distribuitoare, pana la finalizarea procedurii de retragere de la comercializare si eliminare a stocurilor si, de asemenea, sa transmita de urgenta la ANMDM orice informatie detinuta referitoare la aceste produse (ex. lantul de distributie/ data aprovizionarii/ loturile, etc). - Anunț important
06.03.2019
În atenția persoanelor interesate
Pentru diminuarea impactului BREXIT asupra disponibilității dispozitivelor medicale pe piața din România, cu implicații directe asupra sanatății publice, atragem atenția operatorilor economici asupra următoarelor aspecte, care vor aparea, începand cu data de 30.03.2019, în cazul retragerii UK din UE fără semnarea unui acord cu UE27.
descarcă documentul…
- Anunt important
11.02.2019
In atentia persoanelor interesate
ANMDM informeaza cu privire la SUTURILE RESORBABILE BRAND PRIMA
In urma controalelor de supraveghere de piata desfasurate de inspectorii ANMDM, au fost identificate produsele SUTURI RESORBABILE BRAND PRIMA, comercializate ca fiind dispozitive medicale de uz uman, in conditiile in care producatorii Jiangsu Huida Medical Instruments Co. Ltd., China si Yancheng Huida Medical Instruments Co. Ltd., China, au declarat ca aceste suturi au fost fabricate pentru uz veterinar.
In temeiul art.14 si urmatoarele din HG 306/2011 privind unele masuri de supraveghere a pietei produselor reglementate de legislatia Uniunii Europene care armonizeaza conditiile de comercializare a acestora, ANMDM a oprit de la comercializare produsele in cauza.
Avand in vedere clasa mare de risc a produselor implicate si faptul ca nu au fost derulate proceduri de evaluare a conformitatii in scopul demonstrarii ca daca sunt utilizate în conditiile si in conformitate cu scopul propus nu compromit starea clinica sau siguranta pacientilor ori siguranta si sanatatea utilizatorilor, ANMDM solicita unitatilor sanitare si societatilor comerciale care au achizitionat aceste tipuri de produse sa le opreasca imediat de la utilizare si sa le returneze societatilor distribuitoare, pana la finalizarea procedurii de retragere de la comercializare si eliminare a stocurilor si, de asemenea, sa transmita de urgenta la ANMDM orice informatie detinuta referitoare la aceste produse (ex. lantul de distributie/ data aprovizionarii/ loturile, etc). - Anunt important
23.07.2018
In atentia persoanelor interesate
Depunerea dosarelor de obtinere a avizului de functionare
Incepand cu 16.07.2018, dosarele depuse in vederea obtinerii/mentinerii/modificarii AVIZULUI DE FUNCTIONARE se primesc DOAR DACA SUNT INDOSARIATE (dosar cu sina, perforate si prinse direct in dosar).
CEREREA va fi insotita de OPISUL corespunzator activitatii prestate, iar documentele solicitate prin Opis vor fi indosariate in ordinea prevazuta in acesta.
Daca doriti avizarea mai multor activitati sau aveti mai multe puncte de lucru, se va depune un singur dosar.
Documentele specifice fiecarui punct de lucru (ex: lista de personal, dotarea cu echipamente), fiecarei activitati (opisul specific insotit de documentele solicitate prin acesta) vor fi evidentiate prin separatori.
Documentele comune vor fi depuse o singura data.
Producatorii dispozitivelor medicale pe care doriti sa le comercializati vor fi mentionati (in cerere sau in anexa) in ordine alfabetica. Pentru fiecare producator se va depune cate o declaratie de conformitate si, dupa caz, un certificat de marcaj CE, in termen de valabilitate.
Inainte de a depune dosarul, asigurati-va ca ati inclus toate documentele cerute si ati semnat / stampilat toate declaratiile si documentele.
SE PRIMESC DOAR DOSARE COMPLETE. - Anunt important
13.07.2018
In atentia persoanelor interesate
Decizie de interzicere introducere pe piata, distributie si utilizare dispozitive medicale
Va informam ca in urma controalelor de supraveghere de piata, desfasurate de inspectorii ANMDM in perioada noiembrie – decembrie 2017, au fost identificate aparate auditive ,,Hearing Aid’’ de tipul: KF-809, KF-909, KF-910, KF-913, KF-916, KF-916R (KF-912) producator Kanfot (HK) Electronics Co. Ltd., China, incadrate ca dispozitive medicale de clasa I, in conditiile in care potrivit Directivei europene 93/42/EEC aplicabile, aceste dispozitive medicale sunt clasa IIa de risc. Loturile de aparate auditive mentionate mai sus au fost puse pe piata din Romania fara detinerea de catre producator a unui certificat de conformitate CE emis de un Organism Notificat potrivit Anexei II fara Sectiunea 4 sau potrivit uneia dintre Anexele IV, V sau VI din Directiva europeana 93/42/EEC si fara existenta unui reprezentant autorizat unic in Uniunea Europeana desemnat explicit de catre producator.
Potrivit reglementarilor in vigoare, pentru aplicarea marcajului CE in vederea introducerii pe piata Uniunii Europene a unui dispozitiv medical clasa IIa (risc mediu), un producator trebuie sa faca dovada evaluarii conformitatii respectivului dispozitiv cu cerintele aplicabile din Directiva europeana 93/42/EEC, cu implicarea unui Organism Notificat la Bruxelles pentru aceasta directiva, iar producatorii cu sediul in afara Uniunii Europene trebuie sa faca dovada desemnarii unui reprezentant autorizat unic, cu sediul in UE.
Avand in vedere considerentele de mai sus, ANMDM a decis interzicerea de la introducerea pe piata, distributia si utilizarea ca dispozitiv medical a produsului ,,Hearing Aid’’- producator Kanfot (HK) Electronics Co. Ltd., China.
Va rugam sa tineti cont de masurile dispuse de ANMDM referitoare la aparatele auditive neconforme, producator Kanfot (HK) Electronics Co. Ltd., China si sa aduceti la cunostinta ANMDM orice alta informatie detinuta referitoare la aceste dispozitive medicale (ex. distribuitori / firme de protezare care folosesc aceste tipuri de aparate auditive etc.). - Anunt important
28.06.2018
In atentia persoanelor interesate
Decizie de interzicere introducere pe piata, distributie si utilizare dispozitive medicale
Va informam ca in urma controalelor de supraveghere de piata desfasurate de inspectorii ANMDM in luna aprilie 2018 au fost identificate anumite loturi de fire de sutura resorbabile (dispozitive medicale clasa III de risc potrivit Directivei europene 93/42/EEC privind dispozitivele medicale) fabricate de producatorul Demophorius Limited, Cipru in afara perioadei de valabilitate a certificatului de examinare a proiectului detinut, emis de un Organism Notificat conform Anexei II Sectiunea 4 din Directiva europeana 93/42/EEC.
In conditiile in care, potrivit reglementarilor in vigoare, pentru aplicarea marcajului CE in vederea introducerii pe piata a dispozitivelor medicale clasa III (risc cel mai mare) un producator trebuie sa faca dovada detinerii unui sistem complet de asigurare a calitatii certificat conform Anexei II (inclusiv Sectiunea 4) din Directiva europeana 93/42/EEC, ANMDM a decis interzicerea de la introducerea pe piaţă, distributia si utilizarea in Romania a loturilor de fire de sutura resorbabile fabricate de producatorul Demophorius Limited, Cipru dupa data de 17.01.2017 (data de expirare a certificatului de examinare a proiectului detinut de acest producator pentru fire de sutura resorbabile tip PDE,PGA,PGLA). Masura va fi mentinuta pana cand producatorul va face dovada obtinerii unui nou Certificat de examinare a proiectului, emis de un Organism Notificat conform Anexei II Sectiunea 4 din Directiva europeana 93/42/EEC.
Va rugam sa tineti cont de masurile dispuse de ANMDM referitoare la firele de sutura resorbabile, producator Demophorius Limited, Cipru fabricate dupa data de 17.01.2017 si sa transmiteti de urgenta la ANMDM orice informatie detinuta referitoare la aceste dispozitive medicale (ex. lantul de distributie/ data aprovizionarii/ loturile, etc.). - Anunt important
08.05.2018
In atentia persoanelor interesate
Tabel cu unitatile sanctionate contraventional de ANMDM (unitati sanitare, producatori, importatori, distribuitori, prestatori de servicii – dispozitive medicale) in perioada 01.01.2018-30.04.2018.
descarca tabel …
- Anunt important
21.03.2018
In atentia tuturor distribuitorilor de dispozitive medicale si utilizatorilor
Dispozitive medicale falsificate
In data de 07 martie 2018 ANMDM a primit o alerta de la Autoritatea pentru medicamente si dispozitive medicale din Serbia referitoare la identificarea pe piata din Serbia a unor dispozitive medicale falsificate si anume Prezervative Durex, producator Reckitt Benckiser Healthcare (UK) Limited, dupa cum urmeaza:Nume Loc Productie Numar lot Data expirare 1 Extra safe 3 pack Tailanda 0010815033 2020/09 2 Extra safe 3 pack Tailanda 0010815033 2022/04 3 Extra safe 3 pack Tailanda 0010815033 2020/07 4 Extra safe 3 pack Tailanda 0010815033 2020/08 5 Classic 3 pack Tailanda 1000124732 2021/11 6 Feel thin 3 pack Tailanda 0010821302 2020/07 7 Tickle me 3 pack Tailanda 0010895928 2020/07 8 Tickle me 3 pack Tailanda 0010853745 2020/09 9 Tickle me 3 pack Tailanda 0010853745 2020/06 ANMDM a derulat o ancheta in acest sens insa nu a identificat pe teritoriul Romaniei aceste loturi de dispozitive medicale.
In cazul in care va sunt oferite spre distributie sau utilizare produse care apartin unuia din loturile de mai sus, trebuie sa informati imediat ANMDM. - Anunt important
12.03.2018
In atentia persoanelor interesate
In atenția producatorilor, reprezentantilor autorizati ai producatorilor, importatorilor si distribuitorilor care pun in functiune pe teritoriul Romaniei produse pe baza de VACCINIUM MACROCARPON (MERISOR), incadrate in categoria dispozitivelor medicale
ANMDM va aduce la cunostinta Decizia de punere in aplicare (UE) 2017/1445 a Comisiei din 8 august 2017 privind grupul de produse a caror principala actiune prevazuta, bazata pe proantocianidinele (PAC) prezente in merisoare (Vaccinium macrocarpon), este de a preveni sau de a trata cistita:
«Grupul de produse a caror principala actiune prevazuta, bazata pe proantocianidinele prezente in extractul de merisoare (Vaccinium macrocarpon), este de a preveni sau de a trata cistita, nu se incadreaza in definitia dispozitivelor medicale prevazuta la articolul 1 alineatul (2) litera (a) din Directiva 93/42/CEE.»
Prin Decizia mai sus mentionata, produsele pe baza de Vaccinium macrocarpon (merisor) nu mai sunt purtatoare de marcaj CE ceea ce face ca distributia / utilizarea acestora in aceste conditii sa fie contrara prevederilor Art.11, alin 1 din Hotararea nr. 54 din 29 ianuarie 2009 privind conditiile introducerii pe piata a dispozitivelor medicale (transpunerea in legislatia nationala a Directivei 93/42/CEE privind Dispozitivele Medicale, care prevede:
« Se admite introducerea pe piata sau punerea in functiune a dispozitivelor care poarta marcajul european de conformitate CE, prevazut la art. 49, denumit in continuare marcaj CE, marcaj care semnifica faptul ca aceste dispozitive au fost supuse evaluarii conformitatii potrivit prevederilor cap. V – Evaluarea conformitatii.»
Drept urmare, această stare de fapt intra sub incidenta Art. 56, alin 1, lit. a) din acelasi act normativ, care prevede:
«Urmatoarele fapte constituie contraventii si se sanctioneaza dupa cum urmeaza:
a) nerespectarea cerintelor esentiale prevazute la art. 10, cu amenda de la 5.000 lei la 10.000 lei, retragerea de pe piata si/sau interzicerea utilizării si a introducerii pe piata a dispozitivelor neconforme;»
http://eur-lex.europa.eu/legal-content/RO/TXT/PDF/?uri=CELEX:32017D1445&from=EN
descarca Decizia de punere in aplicare (UE) 2017/1445 a Comisiei din 8 august 2017 …
- Anunt important
20.02.2018
In atentia persoanelor interesate
Oprire temporara de la comercializare
In urma controalelor efectuate de ANMDM in activitatea de supraveghere a pietei dispozitivelor medicale, s-au constatat inadvertente intre continutul declaratiilor de conformitate, certificatele de conformitate CE si al etichetei unor dispozitive comercializate de catre societatile TOP-TRADE MEDICAL SRL si EURODOTH TOTAL SRL, motiv suficient pentru a pune la indoiala conformitatea produselor cu cerintele de reglementare aplicabile. Drept urmare, s-a decis oprirea temporara de la comercializare si punere in functiune a urmatoarelor dispozitive medicale:
– Fire sutura cu ac, resorbabile – Polyglycolic acid (PGA), producator HUAIAN PINGAN MEDICAL INSTRUMENT CO. LTD, China, lot 170401B-21470 bucati;
– Fire sutura neresorbabile din poliester si polipropilena producator HUAIAN PINGAN MEDICAL INSTRUMENT CO. LYD, China, lot 170401B si 171114B – 18477 bucati.
In termen de 30 zile de la data de 13.02.2018 vor fi puse la dispozitia ANMDM documentele necesare pentru aducerea produselor la conformitate.
Daca aveti suspiciuni asupra provenientei, calitatii si conformitatii unor dispozitive medicale va rugam sa ne sesizati acest lucru. Va asigurati astfel ca nu sunt puse la dispozitia utilizatorului final dispozitive medicale care sa le poata pune viata in pericol. - Anunt important
16.02.2018
In atentia persoanelor interesate
Incepand cu data de 16.02.2018, ANMDM a pus la dispozitia publicului prin postarea pe site-ul institutiei, doua baze nationale de date, dupa cum urmeaza:
1. Baza nationala de date a producatorilor cu sediul in Romania, care introduc dispozitive medicale pe piata sub propriul nume / al reprezentantilor autorizati in UE care introduc pe piata din Romania dispozitive medicale fabricate de producatori cu sediul social care nu se afla pe teritoriul UE
in conformitate cu art. 31 alin. (1) şi (4) din Hotararea Guvernului nr. 54/2009 privind conditiile introducerii pe piata a dispozitivelor medicale, cu art. 29 şi 32 din Hotararea Guvernului nr. 55/2009 privind dispozitivele medicale implantabile active si cu art. 29 din Hotararea Guvernului nr. 798/2003 privind stabilirea conditiilor de introducere pe piata si de utilizare a dispozitivelor medicale pentru diagnostic in vitro
2. Baza nationala de date cu dispozitivele medicale puse in functiune pe teritoriul Romaniei, in baza notificarilor distribuitorilor acestora
in conformitate cu art. 31 alin. (2) din Hotararea Guvernului nr. 54/2009 privind conditiile introducerii pe piata a dispozitivelor medicale, cu modificarile ulterioare, cu art. 30 din Hotararea Guvernului nr. 798/2003 privind stabilirea conditiilor de introducere pe piata si de utilizare a dispozitivelor medicale pentru diagnostic in vitro, cu modificarile şi completarile ulterioare si cu art. 30 din Hotararea Guvernului nr. 55/2009 privind dispozitivele medicale implantabile active, cu modificarile ulterioare.
Aceste baze de date contin totalitatea inregistrarilor la 15.02.2018 si vor fi actualizate periodic.
https://dispozitive.anm.ro/
Publicarea acestor baze de date ii ajuta pe cei interesati (distribuitori, unitati sanitare) sa obtina mai rapid informatii referitoare la producatorii romani de dispozitive medicale clasa scazuta de risc, care introduc pe piata dispozitive medicale productie proprie si, de asemenea, informatii referitoare la dispozitivele medicale care au fost puse in functiune la un moment dat pe piata si la distribuitorii acestor dispozitive medicale. - Anunt important
13.02.2018
In atentia persoanelor interesate
Urmatoarele documente emise de departamentele de dispozitive medicale ale ANMDM sunt transmise prin Posta Romana, sau inmanate personal la sediul din Bucuresti, sector 1, sos. Nicolae Titulescu nr. 58:
-RAPOARTE DE EVALUARE + AVIZE DE FUNCTIONARE;
-RAPOARTE DE EVALUARE SUPRAVEGHERE;
-CERTIFICATE DE INREGISTRARE A DISPOZITIVELOR MEDICALE;
-CONFIRMARI INREGISTRARI IN BAZA NATIONALA DE DATE A DISPOZITIVELOR MEDICALE PUSE IN FUNCTIUNE;
-AVIZE DE DONATIE;
-AVIZE DE VAMA;
-NEGATII;
-ADRESE;
-BULETINE DE VERIFICARI PERIODICE;
-AVIZE DE UTILIZARE;
-RAPOARTE DE INCERCARI
La solicitarea beneficiarului aceste documente se pot transmite si prin curier rapid.
In acest caz beneficiarul va suporta integral cheltuielile de expeditie. - Anunt important
31.01.2018
In atentia persoanelor interesate
Pentru a intra in deplina conformitate cu legislatia europeana in domeniul dispozitivelor medicale, incepand cu data de 01.02.2018, ANMDM nu mai emite avize de utilizare pentru unitatile mobile de interventie decat in urmatoarele situatii: autovehicul second-hand dotat cu dispozitive medicale second-hand sau parte din ele noi, autovehicul nou dotat cu dispozitive medicale second-hand sau parte din ele noi, autovehicul second-hand dotat cu dispozitive medicale noi.
Pentru unitatile mobile de interventie noi produse in UE (autovehicule noi , echipate in UE cu dispozitive medicale noi) nu se mai emite aviz de utilizare decat in cazul cererilor de acest tip aflate in lucru la data de 01.02.2018.
Pentru unitatile mobile de interventie (ambulantele) pe care producatorul sau reprezentantul autorizat al producătorului stabilit în Romania le introduce pe piata trebuie sa se respecte cerintele aplicabile din HG 54/2009 (art.29) si exista obligatia notificarii ANMDM cu formularul F1 din Ordinul MS nr.1009/2016, dar si cea de obtinere a avizului de functionare ca distribuitor al dispozitivelor medicale din dotarea ambulantei. Avizul de functionare trebuie detinut si de catre distribuitorii ambulantelor produse in restul statelor membre UE. - Anunt important
15.01.2018
In atentia persoanelor interesate
In urma controalelor efectuate de ANMDM privind supravegherea pietei dispozitivelor medicale puse in functiune pe teritoriul Romaniei, s-a constatat ca societatile Complet Electro Serv SRL si Altex Romania SRL au comercializat dispozitivul medical ,,Aparat de masurare a presiunii arteriale de brat- tip Myria MY4811’’, producator Hangzhou Sejoy Electronics & Instruments Co.,Ltd.- China, prezentand neconformitati minore prin nerespectarea cerintelor Anexei 1, pct.13 al H.G. 54/2009, respectiv pe eticheta aparatului nu este precizat numele producatorului si adresa acestuia, numele si adresa reprezentantului autorizat, nr.lot/serie.
Începand cu data de 15.12.2017, pentru neconformitatile minore mentionate mai sus, au fost oprite temporar de la comercializare şi punere în funcţiune pe teritoriul României un numar de 874 de ,,Aparate de masurare a presiunii arteriale de brat- tip Myria MY4811’’ producator Hangzhou Sejoy Electronics & Instruments Co. Ltd.- China.
In cazul in care aveti cunostinta de distribuitori care comercializeaza acest produs sau daca dvs. comercializati acest produs, in conditiile descrise mai sus, va solicitam sa ne comunicati acest lucru, sa opriti comercializarea si sa dispuneti retragerea lor de pe piata.
Daca aveti suspiciuni asupra provenientei, calitatii si conformitatii unor dispozitive medicale va rugam sa ne sesizati acest lucru. Va asigurati astfel ca nu sunt puse la dispozitia utilizatorului final dispozitive medicale care sa le poata pune viata in pericol. - Anunt important
15.01.2018
In atentia persoanelor interesate
Tabel cu unitatile sanctionate contraventional de ANMDM (unitati sanitare, producatori, importatori, distribuitori, prestatori de servicii – dispozitive medicale) in perioada 01.11.2017-31.12.2017.
descarca tabel …
- Anunt important
12.01.2018
In atentia persoanelor interesate
Toate avizele de functionare pana la numarul 4907 inclusiv, valabile, trebuie preschimbate in mod esalonat, pana la data de 31 decembrie 2018, conform OMS 1008/2016.
ANMDM va realiza preschimbarea acestor avize in acelasi timp cu procesarea unei cereri/notificari pentru modificarea avizului depusa la registratura, incepand cu ianuarie 2018, pentru a realiza acest deziderat in mod esalonat si fara discontinuitati. - Anunt important
22.12.2017
Mesajul de sfarsit de an al presedintelui ANMDM
Acum, cand ne apropiem de sfarsitul anului 2017, doresc sa va multumesc dumneavoastra, colaboratorilor si partenerilor ANMDM, pentru suportul acordat si in acest an.
Dupa cum bine stiti, nu a fost intotdeauna usor sa ramanem aplecati asupra misiunii noastre, in conditiile diverselor provocari de peste an.
Privim, insa, cu speranta spre 2018 si suntem increzatori ca intregul personal al Agentiei va depune in continuare toate eforturile pentru a-si indeplini misiunea si ca, alaturi de dumneavoastra, vom reusi sa atingem obiective ambitioase.
Eu si intreg personalul ANMDM va dorim Craciun fericit si un An Nou cu sanatate si impliniri profesionale! - Anunt important
14.11.2017
In atentia utilizatorilor de oxigenoterapie hiperbara
Conform Titului XX din LEGEA Nr. 95 din 14 aprilie 2006 *** Republicata – Partea I privind reforma in domeniul sanatatii
CAPITOLUL III
Supravegherea dispozitivelor medicale in utilizare
ART. 933
(1) In vederea asigurării nivelului de securitate si performanta adecvat scopului pentru care sunt realizate dispozitivele medicale si a evitarii generarii de incidente, utilizatorii au obligatia:
a) de a utiliza dispozitivele medicale numai in scopul pentru care au fost realizate;
In urma controlului efectuat de ANMDM, Serviciul supraveghere piata dispozitive medicale, in data de 29.09.2017 la CENTRUL MEDICAL UNIREA –SUN PLAZA s-a interzis utilizarea echipamentului OXILIFE I pentru tratarea pacientilor cu diverse afectiuni. Desi in manualul de utilizare producatorul SC OXIHELP INDUSTRY SRL declara ca echipamentul nu este un dispozitiv medical si ca oxigenarea hiperbara se poate aplica cu succes in urmatorele cazuri (stare de bine, anti-imbatranire, sport, relaxare) acesta era utilizat ca dispozitiv medical in scopul de a trata diverse afectiuni. - Anunt important
08.11.2017
In atentia persoanelor interesate
Tabel cu unitatile sanctionate contraventional de ANMDM (unitati sanitare, producatori, importatori, distribuitori, prestatori de servicii – dispozitive medicale ) in perioada 01.07.2017 – 31.10.2017.
descarca tabel …
- Anunt important
25.10.2017
In atentia persoanelor interesate
Agentia Nationala a Medicamentului si a Dispozitivelor Medicale va comunica decizia de interzicere a introducerii pe piata, a distributiei si utilizarii ca dispozitiv medical a produsului „Plasture cu ardei iute”- PRIMA, produs de Zhejiang Bangli Medical Products Co., Ltd China.
Decizia de interzicere a fost luata ca urmare a depistarii pe piata a acestui produs in cadrul actiunii de supraveghere de piata si a constatarii incadrarii gresite a acestuia in categoria dispozitivelor medicale. Avand in vedere ca plasturele se aplica numai pe tegument sanatos si ca scopul principal atribuit este de suport al substantei active (extract capsicum) in vederea eliberarii acesteia in organism, ANMDM considera ca acest produs se incadreaza in definitia medicamentului prevazuta la art. 699 din Legea 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile ulterioare. - Anunt important
19.10.2017
In atentia Farmaciilor, Hypermarketurilor, Supermarketurilor, firmelor de distributie online si tuturor distribuitorilor de dispozitive medicale
Conform HG 54/2009 privind conditiile introducerii pe piata a dispozitivelor medicale, HG 55/2009 privind dispozitivele medicale implantabile active, HG 798/2003 privind stabilirea conditiilor de introducere pe piata si de utilizare a dispozitivelor medicale pentru diagnostic in vitro si Ordinului Ministrului Sanatatii nr.1009 privind inregistrarea dispozitivelor medicale in baza nationala de date,
OMS nr.1009/2016
„Art. 9.
(1) Producatorul, reprezentantul autorizat al producatorului, importatorul sau distribuitorul stabilit în Romania sau in orice alt stat membru are obligatia sa notifice ANMDM punerea in functiune pe teritoriul Romaniei a următoarelor tipuri de dispozitive medicale:
a) dispozitive medicale din clasele IIa, IIb şi III;
b) dispozitive medicale pentru diagnostic in vitro care fac obiectul anexei nr. 2 la Hotararea Guvernului nr. 798/2003, cu modificarile si completarile ulterioare;
c) dispozitive medicale pentru diagnostic in vitro de autotestare;
d) dispozitive medicale implantabile active.
(2) Notificarea trebuie facuta in maximum 3 luni de la punerea in functiune a dispozitivului medical.”
Nerespectarea acestei cerinte constituie contraventie si se sanctioneaza cu amenda de la 2.500 lei la 5.000 lei. - Anunt important
09.10.2017
In atentia persoanelor interesate
In situatia in care doriti sa achizitionati online dispozitive medicale va recomandam sa va asigurati ca sunt respectate urmatoarele conditii :
– Operatorul economic furnizeaza in mod clar si inteligibil, informatiile obligatorii privind: denumirea si sediul firmei, CUI-ul acesteia, numarul de tefefon, adresa de e-mail;
– Pe site-ul operatorului economic sunt afisate informatiile privind: principalele caracteristici ale produselor comercializate, denumirea si sediul producatorului, marcajul de conformitate CE, indicatii, contraindicatii si instructiuni de utilizare. - Anunt important
18.09.2017
In atentia persoanelor interesate
Incepand cu 18.09.2017, solicitarile pentru emiterea unei negatii sau a unui aviz de vama in domeniul dispozitivelor medicale vor fi insotite de documentele ce sustin solicitarea si de Formularul pentru plata tarifului – negatie / aviz de vama, completat in dublu exemplar. Formularul poate fi descarcat de la adresa https://www.anm.ro/dispozitive-medicale/formulare-si-tarife/. Nu vor fi inregistrate solicitarile ce nu vor fi insotite de acest formular. - Anunt important
13.09.2017
In atentia persoanelor interesate
Ca urmare a numeroaselor sesizari privind produsele achizitionate de la societatea LA SANTRADE SRL – CENTRUL DE SANATATE BIOSISTEM cu sediul in Bucuresti, strada Constantin Balacescu nr. 1, intersectie cu strada Witting, va informam ca la aceasta data societatea nu detine Aviz de Functionare emis de ANMDM si nu este autorizata sa comercializeze dispozitive medicale.
Produsele comercializate (Saltea Infra Celliant marca AEDEN, Aparat cu laser semiconductor pentru incheietura si nas, Saltea cu impulsuri electromagnetice) nu sunt declarate de catre producatori dispozitive medicale ci aparate de tip weellness. Ca urmare nu pot fi prezentate si comercializate de societatea LA SANTRADE SRL ca dispozitive medicale destinate de producator a fi folosite pentru om în scop de: diagnosticare, prevenire, monitorizare, tratament sau ameliorare a unei afectiuni, producatorii nedeclarand conformitatea produselor cu cerintele Directivei 93/42/EEC. - Anunt important
18.07.2017
In atentia persoanelor interesate
Tabel cu unitatile sanctionate contraventional de ANMDM (producatori, reprezentanți autorizati, importatori, distribuitori, prestatori de servicii – dispozitive medicale) in perioada 01.03.2017-30.06.2017. Acest tabel va fi actualizat periodic.
descarca tabel …
- Anunt important
06.05.2017
In atentia persoanelor interesate
In data de 05.05.2017 au fost publicate în Jurnalul Oficial al Uniunii Europene nr. L117 cele doua regulamente: MDR (Regulamentul (UE) 2017/745 al Parlamentului European si al Consiliului din 5 aprilie 2017 privind dispozitivele medicale, de modificare a Directivei 2001/83/CE, a Regulamentului (CE) nr. 178/2002 si a Regulamentului (CE) nr. 1223/2009 si de abrogare a Directivelor 90/385/CEE si 93/42/CEE ale Consiliului) si IVDR (Regulamentul (UE) 2017/746 al Parlamentului European si al Consiliului din 5 aprilie 2017 privind dispozitivele medicale pentru diagnostic in vitro si de abrogare a Directivei 98/79/CE si a Deciziei 2010/227/UE a Comisiei).
http://eur-lex.europa.eu/legal-content/EN/TXT/PDF/?uri=CELEX:32017R0746&from=EN
http://eur-lex.europa.eu/legal-content/RO/TXT/PDF/?uri=CELEX:32017R0746&from=EN
http://eur-lex.europa.eu/legal-content/EN/TXT/PDF/?uri=CELEX:32017R0745&from=EN
http://eur-lex.europa.eu/legal-content/RO/TXT/PDF/?uri=CELEX:32017R0745&from=EN - Anunt important
28.03.2017
In atentia persoanelor interesate
Pentru a evita mari discontinuitati privind valabilitatea buletinelor de verificare periodica a dispozitivelor medicale, recomandam ca solicitarile de emitere a acestora sa fie depuse la ANMDM cu 6 luni inainte de expirarea celor vechi. - Anunt important
03.03.2017
In atentia persoanelor interesate
Tabel cu unitatile sanctionate contraventional de ANMDM (producatori, reprezentanți autorizati, importatori, distribuitori, prestatori de servicii – dispozitive medicale ) in perioada 01.12.2016-28.02.2017. Acest tabel va fi actualizat periodic.
descarca tabel …
- Anunt important
09.02.2017
In atentia persoanelor interesate
Incepand cu data de 13.02.2017 registratura Dispozitivelor Medicale din cadrul Agentiei Nationale a Medicamentului si a Dispozitivelor Medicale va functiona in sediul din Bd. Nicolae Titulescu Nr.58, Sector 1, Bucuresti.
Program cu publicul
LUNI- JOI : 9,45- 13,45
VINERI – FARA PROGRAM CU PUBLICUL - Anunt important
26.01.2017
In atentia persoanelor interesate
Avand in vedere obligatia, conform legislatiei in vigoare, a declararii activitatilor de sponsorizare de catre producătorii sau reprezentanţii acestora în România, distribuitorii angro şi en detail de dispozitive medicale si materiale sanitare, precum si de catre beneficiarii activitatilor de sponsorizare, până la data de 31 martie a anului în curs, ANMDM RECOMANDA utilizarea formularelor electronice de declarare si utilizarea Ghidurilor de completare a formularelor de declarare (online, pentru beneficiar si prin e-mail, pentru sponsor) disponibile pe site–ul institutiei, la adresa: /dispozitive-medicale/sponsorizari-dispozitive-medicale/ - Anunt important
23.12.2016

- Anunt important
07.12.2016
In atentia persoanelor interesate
Tabel cu unitatile sanctionate contraventional de ANMDM (producatori, reprezentanti autorizati, importatori, distribuitori, prestatori de servicii – dispozitive medicale) in perioada 01.10-30.11.2016. Acest tabel va fi actualizat periodic.
descarca documentul …
- Anunt important
23.11.2016
In atentia persoanelor interesate
Ordinul ministrului sanatatii nr.1009 privind inregistrarea dispozitivelor medicale in baza nationala de date (OMS nr.1009/2016) a fost emis in vederea desfasurarii in conditii optime a activitatilor privind inregistrarea dispozitivelor medicale in baza nationala de date privind dispozitivele medicale, care sa cuprinda dispozitivele medicale introduse pe piata de persoane fizice sau juridice stabilite in Romania şi a persoanelor responsabile de introducerea pe piata a dispozitivelor medicale, dispozitivele medicale din clasele IIa, IIb şi III, a dispozitivelor medicale pentru diagnostic in vitro de autotestare, a dispozitivelor medicale pentru diagnostic in vitro cuprinse in anexa 2 la Hotararea Guvernului nr.798/2003 privind stabilirea conditiilor de introducere pe piata a dispozitivelor medicale pentru diagnostic in vitro, cu modificarile ulterioare, si a dispozitivelor medicale implantabile active puse in functiune pe teritoriul Romaniei.
Inregistrarea in baza nationala de date a dispozitivelor medicale puse in functiune pe teritoriul Romaniei, nu reprezinta o aprobare sau autorizare din partea Agentiei Nationale a Medicamentului si a Dispozitivelor Medicale si nu poate constitui un motiv pentru restrictionarea liberei circulatii a unui dispozitiv medical.
Punerea la dispozitie pe piata nu poate fi interzisa sau restrictionata daca nu s-a realizat aceasta notificare a dispozitivelor in baza nationala de date de catre producatorul/reprezentantul autorizat al producătorului/ importatorul sau distribuitorul stabilit in Romania. Conform art.9, alin 2 al Ordinului OMS 1009/2016 “Notificarea trebuie facută in maximum 3 luni de la punerea in functiune a dispozitivului medical”.
Persoana de contact: Ing. Ioana TENE – Sef DRASP, Email: ioana.tene@anm.ro - Anunt important
21.11.2016
In atentia persoanelor interesate
In urma controalelor efectuate in actiunea de supraveghere a pietei dispozitivelor medicale s-a constatat ca societatea HIGHER PRODUCTS CORPORATION SRL din Bucuresti efectueaza la punctele de lucru din Bucuresti (Centrul de Sanatate Platinum , Centrul de sanatate din Calea Grivitei nr.136) si alte localitati din tara, ANALIZE sau TESTE DE SANATATE folosind analizoare de rezonanta magnetica „Quantum magnetic analyzer”. Aceste aparate nu sunt declarate de catre producator ca fiind dispozitive medicale, deci nu sunt destinate a fi folosite în scop de: diagnosticare, prevenire, monitorizare, tratament sau ameliorare a unei afecţiuni si nu sunt aprobate sau inregistrate de catre Ministerul Sanatatii-ANMDM.
Persoana de contact: Ing. Ioana TENE – Sef DRASP, Email: ioana.tene@anm.ro - Anunt important
17.11.2016
In atentia persoanelor interesate
Situatia DM oprite definitiv /temporar de la comercializare, la data 17.11.2016
Retragerea de dispozitive medicale de pe piata sau interzicerea ori restrangerea introducerii lor pe piata sau a punerii lor in functiune, se face in temeiul prevederilor stabilite de:
– Legea 95/2006, republicata , privind reforma în domeniul sanatatii, Art. 932, alin 1;
– Hotararea Guvernului nr. 54/2009, privind conditiile introducerii pe piata a dispozitivelor medicale ART. 9, alin. 1, Art. 11, alin. 1,alin. 2 si Art.14;
– Hotararea Guvernului nr. 798/2003 privind stabilirea conditiilor de introducere pe piata si de utilizare a dispozitivelor medicale pentru diagnostic in vitro Art.8 alin 2, Art. 10 alin 1, Art.14 , Art. 57 , alin 1;
– H.G. 306/2011, privind unele masuri de supraveghere a pietei produselor reglementate de legislatia Uniunii Europene care armonizeaza conditiile de comercializare a acestora Art. 14 si Art.19.
La data 17.11.2016, dispozitivele medicale cuprinse in tabelul de mai jos sunt definitiv / temporar oprite de la comercializare pana la eliminarea neconformitatilor.
descarca documentul …
- Anunt important
14.10.2016
In atentia persoanelor interesate
Va informam ca in Monitorul Oficial al Romaniei partea I, nr.736 din 22 septembrie 2016, a fost publicat Ordinul ministrului sanatatii nr.1008 pentru aprobarea Normelor metodologice de aplicare a titlului XX din Legea nr. 95/2006 privind reforma in domeniul sanatatii, referitoare la avizarea activitatilor in domeniul dispozitivelor medicale (OMS nr.1008/2016).
Acest ordin cuprinde criteriile generale de evaluare a competentei si capabilitatii persoanelor fizice sau juridice de a realiza activitatile in domeniul dispozitivelor medicale pentru care solicita avizul prevazut la art. 926 alin. (2) din Legea nr. 95/2006 privind reforma in domeniul sanatatii, republicata, cu modificarile si completarile ulterioare.
Ordinul ministrului sanatatii nr.1008 pentru aprobarea Normelor metodologice de aplicare a titlului XX din Legea nr. 95/2006 privind reforma in domeniul sanatatii, referitoare la avizarea activitatilor in domeniul dispozitivelor medicale include urmatoarele modificari importante:
1. Pentru avizarea activitatilor de import dispozitive medicale, de depozitare si distributie dispozitive medicale, de reparare, mentenanta si punere in functiune/ instalare dispozitive medicale, optica medicala si protezare, ANMDM, in baza propriei proceduri, evalueaza la sediul solicitantului competenta si capabilitatea acestuia. Evaluarea se finalizeaza cu un raport de evaluare in baza caruia ANMDM emite avizul de functionare. Cu scopul de a facilita procesul de completare a cererii de eliberare a avizului de functionare pentru activitati in domeniul dispozitivelor medicale va aducem la cunostiinta urmatoarle definitii: Importator inseamna orice persoana fizica sau juridica stabilita in interiorul Comunitatii care introduce pe piata comunitara un dispozitiv medical dintr-o tara terta
Distribuitor inseamna orice persoana fizica sau juridica din lantul de distributie, alta decat producatorul sau importatorul, care pune la dispozitie pe piata un dispozitiv medical, pana la punctul de punere in functiune
Punere in functiune – etapa in care dispozitivul este pus la dispozitia utilizatorului final, fiind gata de utilizare pe piata Uniunii Europene, pentru prima data pentru scopul propus;
Punere la dispozitie pe piata inseamna orice furnizare a unui dispozitiv medical, altul decat dispozitivul medical supus investigatiei clinice, pentru distributie, consum sau utilizare pe piata comunitara in cursul unei activitati comerciale, in schimbul unei plati sau gratuit.
Utilizator inseamna orice utilizator profesionist in ingrijiri de sanatate sau orice utilizator laic.
Utilizator laic inseamna orice persoana care nu are educatie formativa intr-un domeniu relevant de ingrijiri de sanatate sau intr-o disciplina medicala.
2. Avizele de functionare emise sau preschimbate pana la data intrarii in vigoare a prezentelor norme metodologice se preschimba in mod esalonat, pana la data de 31 decembrie 2018, la solicitarea unitatii respective. Pentru preschimbarea avizului de functionare, detinatorul acestuia inainteaza ANMDM cererea pentru eliberarea avizului de functionare, pe care face mentiunea PRESCHIMBARE, insotita de documentele prevazute la art. 5 alin. (3) si/sau (5) din OMS 1008/2016.
Ordinul ministrului sanatatii nr. 309/2015 pentru aprobarea Normelor metodologice de aplicare a titlului XIX din Legea nr. 95/2006 privind reforma in domeniul sanatatii, referitoare la avizarea activitatilor in domeniul dispozitivelor medicale, publicat in Monitorul Oficial al Romaniei, Partea I, nr. 198 din 25 martie 2015, a fost abrogat prin articolul 3 din OMS nr. 1008/2016.
Ordinul ministrului sanatatii nr.1008 pentru aprobarea Normelor metodologice de aplicare a titlului XX din Legea nr. 95/2006 privind reforma in domeniul sanatatii, referitoare la avizarea activitatilor in domeniul dispozitivelor medicale il puteti gasi integral pe acest site la adresa dispozitive medicale- evaluare unitati tehnico medicale- legislatie specifica.
Formularul de cerere pentru eliberarea avizului de functionare, formularul de cerere pentru modificarea avizului de functionare precum si formularul de cerere pentru inregistrarea in baza de date a furnizorilor de servicii in domeniul dispozitivelor medicale rezidenti in UE sau SEE se pot descarca de la adresa dispozitive medicale- evaluare unitati tehnico medicale- documente utile. - Anunt important
05.10.2016
In atentia persoanelor interesate
Situatia DM oprite definitiv /temporar de la comercializare, la data 05.10.2016
Retragerea de dispozitive medicale de pe piata sau interzicerea ori restrangerea introducerii lor pe piata sau a punerii lor in functiune, se face in temeiul prevederilor stabilite de: – Legea 95/2006, republicata , privind reforma în domeniul sanatatii, Art. 932, alin 1;
– Hotararea Guvernului nr. 54/2009, privind conditiile introducerii pe piata a dispozitivelor medicale ART. 9, alin. 1, Art. 11, alin. 1,alin. 2 si Art.14;
– Hotararea Guvernului nr. 798/2003 privind stabilirea conditiilor de introducere pe piata si de utilizare a dispozitivelor medicale pentru diagnostic in vitro Art.8 alin 2, Art. 10 alin 1, Art.14 , Art. 57 , alin 1;
– H.G. 306/2011, privind unele masuri de supraveghere a pietei produselor reglementate de legislatia Uniunii Europene care armonizeaza conditiile de comercializare a acestora Art. 14 si Art.19.
La data 05.10.2016, dispozitivele medicale cuprinse in tabelul de mai jos sunt definitiv / temporar oprite de la comercializare pana la eliminarea neconformitatilor
descarca documentul …
- Anunt important
04.10.2016
In atentia persoanelor interesate
Tabel cu unitatile sanctionate contraventional de ANMDM (producatori, reprezentanti autorizati, importatori, distribuitori, prestatori de servicii – dispozitive medicale ) in perioada 01.06 – 30.09.2016. Acest tabel va fi actualizat periodic.
descarca documentul …
- Anunt important
23.09.2016
In atentia persoanelor interesate
Situatia DM oprite definitiv/temporar de la comercializare, la data 16.09.2016
Retragerea de dispozitive medicale de pe piata sau interzicerea ori restrangerea introducerii lor pe piata sau a punerii lor in functiune, se face in temeiul prevederilor stabilite de:
– Legea 95/2006, republicata , privind reforma în domeniul sanatatii, Art. 932, alin 1;
– Hotararea Guvernului nr. 54/2009, privind conditiile introducerii pe piata a dispozitivelor medicale ART. 9, alin. 1, Art. 11, alin. 1,alin. 2 si Art.14;
– Hotararea Guvernului nr. 798/2003 privind stabilirea conditiilor de introducere pe piata si de utilizare a dispozitivelor medicale pentru diagnostic in vitro Art.8 alin 2, Art. 10 alin 1, Art.14 , Art. 57 , alin 1;
– H.G. 306/2011, privind unele masuri de supraveghere a pietei produselor reglementate de legislatia Uniunii Europene care armonizeaza conditiile de comercializare a acestora Art. 14 si Art.19
La data 16.09.2016, dispozitivele medicale cuprinse in tabelul de mai jos sunt definitiv / temporar oprite de la comercializare pana la eliminarea neconformitatilor .
descarca documentul …
- Anunt important
23.09.2016
In atentia persoanelor interesate
A.N.M.D.M. a fost informata despre retragerea voluntara de catre producatorul Sage Products Inc., a unor loturi din dispozitivele medicale clasa I, “Comfort Shield Personal Cleansing Perineal Care Washcloths”, în urma contaminarii acestora cu bacteria Burkholderia cepacia. Sage Products Inc. si-a notificat distribuitorii si au fost furnizate instructiuni pentru intreruperea utilizarii si returnarii produselor catre producator.
Loturile afectate au nr. 53957, cu data expirarii 06.03.2018 si respectiv nr. 55781, cu data expirarii 19.06.2018 si au fost distribuite către clienti in perioada 31 martie – 24 iunie 2016.
Administrarea topica a unui produs contaminat cu Burkholderia cepacia poate provoca infectii grave la pacientii ale căror organe nu pot lupta impotriva bolii sau la pacientii spitalizati, precum si anumite alte grupuri de pacienti. Aceste infectii ar putea pune viața in pericol. Pana in prezent, nu au fost raportate evenimente adverse asociate cu produsele afectate, care au fost livrate catre distribuitori și facilitătile de asistenta medicala în Statele Unite. Produsul “Comfort Shield Barrier Cream Cloths” este o panza nesterila pentru utilizare topica, cu rol de protectie in prevenirea si tratarea iritatiilor pielii asociate umezelii cauzate de expunerea la urina si / sau scaun.
Avand in vedere ca produsele mai sus mentionate sunt dispozitive medicale clasa I si nu exista obligativitatea inregistrarii acestora in baza de date a A.N.M.D.M. cu dispozitivele medicale puse in functiune pe teritoriul Romaniei, in cazul in care aveti cunostinta de distribuitori care comercializeaza aceste produse sau daca dumneavoastra comercializati aceste produse, va solicitam sa ne comunicati acest lucru, sa opriti comercializarea acestora si sa dispuneti retragerea lor de pe piata, astfel incat sa nu fie pusa in pericol sanatatea si securitatea pacientilor. - Anunt important
23.09.2016
In atentia persoanelor interesate
Dacă aveti suspiciuni asupra provenientei, calitatii şi conformitatii unor dispozitive medicale va rugam sa ne anuntati pentru a putea lua toate masurile legale.
Persoana de contact: Ing. Ioana TENE – Şef DRASP, Email: ioana.tene@anm.ro - Anunt important
22.09.2016
In atentia persoanelor interesate
Va informam ca ANMDM a publicat lista societatilor care au fost sanctionate contraventional incepand cu data de 01.06.2016. Aceasta lista va fi actualizata periodic.
descarca lista …
- Anunt important
21.09.2016
In atentia persoanelor interesate
Va informam ca in Monitorul Oficial al Romaniei partea I, nr.705 din 12 septembrie 2016, a fost publicat Ordinul ministrului sanatatii nr.1009 privind inregistrarea dispozitivelor medicale in baza nationala de date (OMS nr.1009/2016).
Acest ordin a fost emis in vederea desfasurarii in conditii optime a activitatilor privind inregistrarea dispozitivelor medicale in baza nationala de date privind dispozitivele medicale, care sa cuprinda:
– dispozitivele medicale introduse pe piata de persoane fizice sau juridice stabilite in Romania şi a persoanelor responsabile de introducerea pe piata a dispozitivelor medicale
– dispozitivele medicale din clasele IIa, IIb şi III, a dispozitivelor medicale pentru diagnostic in vitro de autotestare, a dispozitivelor medicale pentru diagnostic in vitro cuprinse in anexa 2 la Hotararea Guvernului nr.798/2003 privind stabilirea conditiilor de introducere pe piata a dispozitivelor medicale pentru diagnostic in vitro, cu modificarile ulterioare, si a dispozitivelor medicale implantabile active puse in functiune pe teritoriul Romaniei.
Formularele din OMS1009/2016 sunt disponibile pe site-ul www.anm.ro:
– Formularele F1 si F2 – la Sectiunea Dispozitive medicale/ Reglementare, Autorizare si Supraveghere piata/Inregistrare dispozitive medicale la introducerea pe piata
– Formularul F3 – la Sectiunea Dispozitive medicale/ Reglementare, Autorizare si Supraveghere piata/Notificare dispozitive medicale la punerea in functiune
Ordinul ministrului sanatatii nr.1009/2016 privind inregistrarea dispozitivelor medicale in baza nationala de date include urmatoarele modificari importante:
Notificarea dispozitivelor medicale de tipul celor prevazute la art. 9, din OMS nr.1009/2016 trebuie facuta in maximum 3 luni de la punerea in functiune a dispozitivului medical.
Dispozitivele medicale de tipul celor prevazute la art. 4, din OMS nr.1009/2016, pentru care Ministerul Sanatatii/ANMDM a emis certificat de inregistrare a dispozitivelor medicale din anul 2007 si pana la data intrarii in vigoare a OMS nr.1009/2016 (12 septembrie 2016), sunt considerate inregistrate in baza nationala de date ca dispozitive medicale introduse pe piata pe teritoriul Romaniei. Certificatele de inregistrare a dispozitivelor medicale emise raman valabile.
Dispozitivele medicale de tipul celor prevazute la art. 9, din OMS nr.1009/2016, pentru care a fost notificat Ministerul Sanatatii/ANMDM din anul 2007 si pana la data intrarii in vigoare a OMS nr. 1009/2016 (12 septembrie 2016), sunt considerate inregistrate in baza nationala de date ca dispozitive medicale puse in functiune pe teritoriul Romaniei.
in cazul dispozitivelor medicale de tipul celor prevazute la art. 9, pentru care a fost notificat Ministerul Sanatatii inainte de anul 2007, notificarea se realizeaza pana la data de 31 decembrie 2017.
Inregistrarea in baza nationala de date a dispozitivelor medicale puse in functiune pe teritoriul Romaniei, in baza notificarii cu Formularul F3, nu reprezinta aprobare sau autorizare din partea Agentiei Nationale a Medicamentului si a Dispozitivelor Medicale.
OMS nr. 372/2015 privind inregistrarea dispozitivelor medicale a fost abrogat de art. 16 din OMS nr. 1009/2016. - Anunt important
02.09.2016
In atentia persoanelor interesate
Cu ocazia controalelor efectuate in cadrul actiunii de supraveghere a pietei dispozitivelor medicale, s-a constatat ca S.C. ILIAS MED SRL, inmatriculata la Registrul comertului cu nr. J13/2564/2008, avand CUI 24245686, cu sediul in Constanta, Soseaua Mangaliei, Complex Doraly, Stand 17 C, judetul Constanta, desfasoara activitate de optica medicala fara a detine Aviz de functionare emis in conformitate cu prevederile Legii 95/2006, republicate in august 2015.
ANMDM a sanctionat contraventional societatea si a dispus oprirea activitatii pana la intrarea in legalitate. - Anunt important
02.09.2016
In atentia persoanelor interesate
Cu ocazia controalelor efectuate in cadrul actiunii de supraveghere a pietei dispozitivelor medicale, s-a constatat ca S.C. NONINO TRADING SRL, inmatriculata la Registrul comertului cu nr. J13/2240/1997, avand CUI 9806654, cu sediul in Constanta, Bd. 1 Mai, nr.1, Bloc H9, Parter, distribuie si comercializeaza dispozitive medicale fara a detine Aviz de functionare emis in conformitate cu prevederile Legii 95/2006, republicate in august 2015.
ANMDM a sanctionat contraventional societatea si a dispus oprirea de la comercializare a dispozitivelor medicale, pana la intrarea in legalitate. - Anunt important
02.09.2016
In atentia persoanelor interesate
ANMDM s-a autosesizat si a dispus efectuarea unui control la Spitalul Universitar de Urgenta Bucuresti, in vederea stabilirii cauzelor care ar fi putut determina, in data de 11.08.2016, incidentul reclamat, referitor la electrocutarea asistentului ATI, in momentul manevrarii butonului de administrare debit crescut de oxigen al echipamentului de anestezie tip Fabius Tiro, serie ARZC 0107/2008 (producator Draeger Medical AG, Germania).
In data de 16.08.2016, o echipa a ANMDM – Departamentul Tehnic Laboratoare s-a deplasat la locul de utilizare a echipamentului, pentru determinarea parametrilor de securitate electrica si de performanta ai acestuia.
Constatarile, consemnate in Raportul de expertiza, au fost urmatoarele:
– Atat valorile obtinute la determinarea parametrilor de securitate electrica ai echipamentului, cat si a celor de performanta, s-au incadrat in limitele prevazute in specificatiile tehnice ale producatorului si in standardele aplicabile. Valorile obtinute la masurarea, in mod repetat, a parametrilor definitorii de securitate electrica, la intervale neregulate de timp, s-au incadrat de fiecare data in limitele prevazute de specificatiile tehnice ale producatorului si de standardele aplicabile;
– Valorile obtinute la masurarea curentilor de scurgere intalniti pe toate partile tangibile ale ramei metalice a butonului de administrare debit crescut de oxigen s-au incadrat in limitele prevazute de specificatiile tehnice ale producatorului si in standardele aplicabile;
– S-a facut dovada instruirii personalului medical care a utilizat echipamentul.
In concluzie, avand in vedere rezultatele masuratorilor efectuate in conditiile de teren regasite la momentul controlului, la folosirea echipamentului conform manualului de utilizare al producatorului, de un personal instruit in acest sens, nu este posibila aparitia incidentului reclamat (electrocutare). Concluzia echipei de control a ANMDM – Departamentul Tehnic Laboratoare a fost de altfel sustinuta si de faptul ca, la doar o zi de la incidental reclamat, anterior controlului ANMDM, acelasi echipament a fost utilizat la o interventie chirurgicala de urgenta, cand s-a recunoscut functionarea la parametrii normali, fara semnalarea vreunui incident. - Anunt important
02.09.2016
In atentia persoanelor interesate
ANMDM s-a autosesizat si a dispus efectuarea unui control la Spitalul Clinic Coltea, Bucuresti, in vederea stabilirii cauzelor care ar fi putut determina, in data de 28.07.2016 incidentul reclamat (referitor la aprinderea electrodului bipolar – accesoriu reutilizabil), petrecut in timpul utilizarii echipamentului de electrochirurgie cu curenti de inalta frecventa GN300, producator Aesculap Germania.
In data de 29.07.2016, o echipa a ANMDM – Departamentul Tehnic Laboratoare s-a deplasat la locul de utilizare a echipamentului, pentru determinarea parametrilor de securitate electrica si de performanta ai acestuia.
Constatarile, consemnate in Raportul de expertiza si in Raportul de control, au fost urmatoarele:
– Echipamentul de electrochirurgie cu curenti de inalta frecventa GN300 era functional si se incadra in limitele prevazute in specificatiile tehnice ale producatorului si in standardele aplicabile;
– Cordonul de legatura dintre portelectrod si echipamentul de electrochirurgie cu curenti de inalta frecventa era sectionat la imbinarea cu portelectrodul, fara insa a se constata topirea izolatiei cablului si nici a se simti miros de arsura electrica. De mentionat este faptul ca accesoriile implicate in incident au fost accesorii reutilizabile, apartinand spitalului.
– Nu s-a facut dovada respectarii cerintei privind nominalizarea unei persoane cu responsabilitati in ceea ce priveste respectarea instructiunilor de utilizare si respectiv, de verificare vizuala a integritatii echipamentelor si de efectuare a testelor necesare inainte de utilizarea acestora.
– Nu s-a facut dovada instruirii medicului care a utilizat echipamentul Electrocauter GN300 si a reclamat incidentul. - Anunt important
26.08.2016
In atentia persoanelor interesate
Incepand cu data de 01.09.2016 registratura din Bd. Nicolae Titulescu 58, Sector 1, Bucureşti, va functiona in sediul din Str. Aviator Sanatescu 48, Sector 1, Bucuresti. - Anunt important
25.07.2016
Situatia DM oprite temporar/ definitiv de la comercializare, la data 21.07.2016.
Retragerea de dispozitive medicale de pe piata sau interzicerea ori restrangerea introducerii lor pe piata sau a punerii lor in functiune, se face in temeiul prevederilor stabilite de:
– Legea 95/2006, republicata, privind reforma in domeniul sanatatii, Art. 932, alin 1;
– Hotararea Guvernului nr. 54/2009, privind conditiile introducerii pe piata a dispozitivelor medicale ART. 9, alin. 1, Art. 11, alin. 1,alin. 2 si Art.14; – Hotararea Guvernului nr. 798/2003 privind stabilirea conditiilor de introducere pe piata si de utilizare a dispozitivelor medicale pentru diagnostic in vitro Art.8 alin 2, Art. 10 alin 1, Art.14 , Art. 57 , alin 1;
– H.G. 306/2011, privind unele masuri de supraveghere a pietei produselor reglementate de legislatia Uniunii Europene care armonizeaza conditiile de comercializare a acestora Art. 14 si Art.19.
La data 21.07.2016, dispozitivele medicale cuprinse in tabelul de mai jos sunt temporar/definitiv oprite de la comercializare pana la eliminarea neconformitatilor.
descarca documentul …
- Anunt important
25.07.2016
In atentia persoanelor interesate
In urma unei anchete desfasurate de catre Organizatia Mondiala a Sanatatii la sediul producatorului, Hangzhou Biotest Biotech Co. Ltd, China, au fost constatate neconformitati critice si majore in procesul de productie a dispozitivelor medicale pentru diagnostic in vitro, pe care producatorul nu a reusit sa le rezolve. Producatorul a dispus retragerea de pe piata a urmatoarelor produse cu loturile aferente:
– RightSign HIV 1.2.O Rapid Test Cassette,
Loturi: HIV14060001; HIV14060002; HIV14100001;
HIV14100002; HIV15080003; HIV15110001;
HIV16020005; HIV16050008
– RightSign HCV Rapid Test Cassette,
Loturi: HCV14060001; HCV14100001; HCV15050007;
HCV15050008; HCV15090007; HCV15110001;
HCV15110002; HCV16030007
– RightSign HBsAg Rapid Test Cassette
Loturi: HBSG14060001; HBSG14100001; HBSG15040001;
HBSG15040002; HBSG15050005; HBSG15060003;
HBSG15080001; HBSG15120003; HBSG16030001;
HBSG16050014
Producatorii BIOSYNEX S.A. – Franta si DIALAB – Austria, sunt deasemenea implicati, dispozitvele medicale pentru diagnostic in vitro ale acestora fiind de tipul OBL.
OBL – Un etichetator marca proprie ce achizitioneaza un produs finit sau parti componente ale acestuia, de la Producatorul original al echipamentului (OEM – Original Equipment Manufacturer), pe care apoi il introduce pe piata sub numele sau marca comerciala proprie.
Produsele fabricate de catre BIOSYNEX S.A. – Franta si DIALAB – Austria, cu loturile aferente, afectate, se regasesc mai jos
– Biosynex S.A., Franta:
– Exacto Pro test HIV Ref 857318
– Biosynex HIVTOP Ref 1150004
– HIVTOP Ref 5059
– Immunoquick HIV Ref 0556_K25
– Biosynex HCV Ref 1150002
– HCVTOP Ref 5058
– Immunoquick HCV Ref 0557_K25
– Biosynex HBV Ref 1150003
– HBVTOP Ref 5060
– Immunoquick HBsAg Ref 0558_K25
– Dialab, Austria:
– DIAQUICK HIV Triline Cassette:
Loturi: HIV15100013 (Exp.: 2017-08-31)
HIV16010011 (Exp.: 2017-12-31)
HIV16020005 (Exp.: 2018-02-28)
– DIAQUICK HCV Cassette:
Loturi: HCV15100013 (Exp.: 2017-10-31)
HCV16010008 (Exp.: 2018-01-31)
HCV16030007 (Exp.: 2018-03-31)
– DIAQUICK HBsAg Cassette:
Loturi: HBSG15100016 (Exp.: 2017-10-31)
HBSG16010012 (Exp.: 2018-01-31)
Toti cei trei producatori au dispus retragerea de pe piata a tuturor produselor implicate, dupa cum urmeaza:
– In data de 08.06.2016, producatorul Biosynex S.A. Franta, a emis o „Notificare de suspendare, utilizare si retragere de pe piata a dispozitivelor medicale”, către distribuitori, pentru retragerea produselor si loturilor mai sus mentionate, cu returnarea acestora la producator;
– In data de 16.06.2016, producatorul Hangzhou Biotest Biotech Co. Ltd, a emis o Notă de Atentionare, catre distribuitori, pentru retragerea produselor mai sus mentionate, cu returnarea acestora la producator;
– In data de 20.06.2016, producatorul DIALAB, Austria a emis o Nota de Atentionare, catre distribuitori, pentru retragerea produselor si loturilor mai sus mentionate, cu returnarea acestora la producator.
Având in vedere informatiile detinute si riscurile cu implicatii majore asupra sanatatii, in scopul protectiei sanatatii publice, ANMDM a decis transmiterea catre posibilii distribuitori ai produselor mentionate, in data de 28.06.2016, o atentionare de retragere a acestor produse, si a demarat actiunea de control in vederea verificarii respectarii dispozitiilor, de retragere a produselor, date de către producatori.
Dacă aveti cunostinta de distribuitori care comercializeaza aceste produse sau dumneavoastra comercializati dispozitive medicale pentru diagnostic in vitro, fabricate de Hangzhou Biotest Biotech Co. Ltd. – China, va solicitam sa ne informati si sa stopati comercializarea acestor produse astfel incat sa nu fie pusa in pericol sanatatea si securitatea utilizatorilor acestor dispozitive medicale.
Mai multe detalii referitoare la această ancheta gasiti pe site-ul OMS. - Anunt important
25.07.2016
In atentia persoanelor interesate
Daca aveti suspiciuni asupra provenientei, calitatii si conformitatii unor dispozitive medicale va rugam sa ne anuntati pentru a putea lua toate masurile legale.
Persoana de contact: Ing. Ioana TENE – Sef DRASP, Email: ioana.tene@anm.ro - Anunt important
07.07.2016
Situatia DM oprite temporar/ definitiv de la comercializare, la data 04.07.2016
Retragerea de dispozitive medicale de pe piata sau interzicerea ori restrangerea introducerii lor pe piata sau a punerii lor in functiune, se face in temeiul prevederilor stabilite de:
– Legea 95/2006, republicata , privind reforma in domeniul sanatatii, Art. 932, alin 1;
– Hotarârea Guvernului nr. 54/2009, privind conditiile introducerii pe piata a dispozitivelor medicale ART. 9, alin. 1, Art. 11, alin. 1,alin. 2 si Art.14;
– Hotarârea Guvernului nr. 798/2003 privind stabilirea conditiilor de introducere pe piata si de utilizare a dispozitivelor medicale pentru diagnostic in vitro Art.8 alin 2, Art. 10 alin 1, Art.14 , Art. 57 , alin 1;
– H.G. 306/2011, privind unele masuri de supraveghere a pietei produselor reglementate de legislatia Uniunii Europene care armonizeaza conditiile de comercializare a acestora Art. 14 si Art.19.
La data 04.07.2016, dispozitivele medicale cuprinse in tabelul de mai jos sunt temporar/definitiv oprite de la comercializare pana la eliminarea neconformitatilor.
descarca documentul …
- Anunt important
05.07.2016
In atentia persoanelor interesate
In urma controalelor efectuate in actiunea de supraveghere a pietei dispozitivelor medicale s-a constatat ca o societate din Brasov a comercializat dispozitive medicale care desi au inscriptionat pe eticheta anumiti producatori, din documentele de provenienta rezulta ca alta societate este producatorul acestor dispozitive.
Produsele in cauza sunt:
– „Turbina cu led W&H model TE-95 RM” , producator trecut pe eticheta : W&H DENTALWERK Burmoos Gmbh Austria;
– „Ace Protaper, marca Dentsply “Dentsply protaper files” , producator inscris pe eticheta : MAILLEFER INSTRUMENTS HOLDING SARL Elvetia.
Din documentele de provenienta ( declaratie de conformitate, factura fiscala) rezulta ca OSAKADENT GROUP Ltd- HonngKong este producator . Am luat legatura cu producatorii MAILLEFER INSTRUMENTS HOLDING SARL Elvetia si W&H DENTALWERK Burmoos Gmbh Austria care ne-au confirmat ca produsele identificate sunt contrafacute , nefiind fabricate de ei.
Daca aveti cunostinta de distribuitori care comercializeaza aceste produse sau dumneavoastra comercializati dispozitive medicale fabricate de OSAKADENT GROUP Ltd- HonngKong va solicitam sa ne informati si sa stopati comercializarea acestor produse astfel incat sa nu fie pusa in pericol sanataea si securitatea utilizatorilor acestor dispozitive medicale.
Daca aveti suspiciuni asupra provenientei, calitatii si conformitatii unor dispozitive medicale va rugam sa ne anuntati pentru a putea lua toate masurile legale.
Persoana de contact: Ing. Ioana TENE – Sef DRASP, Email: ioana.tene@anm.ro - Anunt important
03.06.2016
Situatia DM oprite temporar/ definitiv de la comercializare, la data 27.05.2016
Retragerea de dispozitive medicale de pe piata sau interzicerea ori restrangerea introducerii lor pe piata sau a punerii lor in functiune, se face in temeiul prevederilor stabilite de:
– Legea 95/2006, republicata , privind reforma in domeniul sanatatii, Art. 932, alin 1;
– H.G. 54/2009, privind conditiile introducerii pe piata a dispozitivelor medicale ART. 9, alin. 1, Art. 11, alin. 1,alin. 2 si Art.14;
– Hotararea Guvernului nr. 798/2003 privind stabilirea conditiilor de introducere pe piata si de utilizare a dispozitivelor medicale pentru diagnostic in vitro Art.8 alin 2, Art. 10 alin 1, Art.14 , Art. 57 , alin 1;
– H.G. 306/2011, privind unele masuri de supraveghere a pietei produselor reglementate de legislatia Uniunii Europene care armonizeaza conditiile de comercializare a acestora Art. 14 si Art.19.
La data 17.05.2016, dispozitivele medicale cuprinse in tabelul de mai jos sunt temporar oprite de la comercializare pana la eliminarea neconformitatilor.
descarca documentul …
- Anunt important
18.05.2016
Situatia DM oprite temporar/ definitiv de la comercializare, la data 17.05.2016
Retragerea de dispozitive medicale de pe piata sau interzicerea ori restrangerea introducerii lor pe piata sau a punerii lor in functiune, se face in temeiul prevederilor stabilite de:
– Legea 95/2006, republicata , privind reforma in domeniul sanatatii, Art. 932, alin 1;
– H.G. 54/2009, privind conditiile introducerii pe piata a dispozitivelor medicale ART. 9, alin. 1, Art. 11, alin. 1,alin. 2 si Art.14;
– Hotararea Guvernului nr. 798/2003 privind stabilirea conditiilor de introducere pe piata si de utilizare a dispozitivelor medicale pentru diagnostic in vitro Art.8 alin 2, Art. 10 alin 1, Art.14 , Art. 57 , alin 1;
– H.G. 306/2011, privind unele masuri de supraveghere a pietei produselor reglementate de legislatia Uniunii Europene care armonizeaza conditiile de comercializare a acestora Art. 14 si Art.19.
La data 17.05.2016, dispozitivele medicale cuprinse in tabelul de mai jos sunt temporar oprite de la comercializare pana la eliminarea neconformitatilor.
descarca documentul …
- Anunt important
25.04.2016
Situatia DM oprite temporar/definitiv de la comercializare, la data 25.04.2016
Retragerea de dispozitive medicale de pe piata sau interzicerea ori restrangerea introducerii lor pe piata sau a punerii lor in functiune, se face in temeiul prevederilor stabilite de:
– Legea 95/2006, republicata , privind reforma in domeniul sanatatii, Art. 932, alin 1;
– H.G. 54/2009, privind conditiile introducerii pe piata a dispozitivelor medicale ART. 9, alin. 1, Art. 11, alin. 1,alin. 2 si Art.14;
– H.G. 306/2011, privind unele masuri de supraveghere a pietei produselor reglementate de legislatia Uniunii Europene care armonizeaza conditiile de comercializare a acestora Art. 14 si Art.19.
Dispozitivele medicale cuprinse in tabelul de mai jos sunt temporar oprite de la comercializare pana la eliminarea neconformitatilor:
descarca documentul …
- Anunt important
10.03.2016
Decizia Nr. 203/02.03.2016
In baza probelor si a verificarilor facute s-a intocmit REFERATUL de motivare, drept pentru care, in temeiul legii, ANMDM, prin Decizia Nr.203/02.03.2016, a dispus INTERZICEREA introducerii pe piata, comercializarea si utilizarea precum si publicitatea capsulelor HearMEC Hyperbaric Oxygen, fabricate de Hear MEC Corporation Japonia.
Decizia nr.203/02.03.2016 …
- Anunt important
01.02.2016
Declararea activitatilor de sponsorizare in domeniul dispozitivelor medicale
Va reamintim ca in conformitate cu art.1 alineatul ( 1 ) din OMS nr. 874/10 iulie 2015 pentru aprobarea formularelor de declarare a activitatilor de sponsorizare in domeniul dispozitivelor medicale si al materialelor sanitare, pana la data de 31 martie 2016 se raporteaza toate activitatile de sponsorizare, precum si orice alte cheltuieli suportate in 2015.
Formularele de declarare a activitatilor de sponsorizare, precum si a celorlalte cheltuieli, altele decat sponsorizarea, se vor depune in original la Registratura ANMDM, sediul din Sos. N. Titulescu, nr. 58, sector 1, Bucuresti, conform programului si se vor transmite in format electronic de tip EXCEL pe adresa de mail: sponsorizare_dm@anmdm.ro.
Nu vor fi luate in considerare formularele completate, altele decat cele in conformitate cu OMS nr. 874/2015.
In adresa de inaintare ce insoteste formularul completat este absolut necesar sa se mentioneze atat persoana de contact, cat si datele de contact (telefon, fax, e-mail etc.). - Anunt important
30.07.2015
Declararea activitatilor de sponsorizare in domeniul dispozitivelor medicale
Avand in vedere publicarea in Monitorul Oficial a OMS 874/2015 privind aprobarea formularelor de declarare a activitatilor de sponsorizare in domeniul dispozitivelor medicale si al materialelor sanitare, va comunicam ca formularele necesare raportarii activitatilor desfasurate in conf cu art.799 din Legea 95/2006 privind reforma in domeniul sanatatii cu modificarile si completarile ulterioare au fost postate pe website-ul ANMDM la sectiunea „Sponsorizare”.
Formularele de declarare a activitatilor de sponsorizare, precum si a celorlalte cheltuieli, altele decat sponsorizarea, se vor depune in original la Registratura ANMDM, sediul din Sos. N. Titulescu nr. 58, sector 1, Bucuresti, conform programului si se vor transmite in format electronic pe adresa de mail sponsorizare_dm@anmdm.ro. - Anunt important
20.05.2015
Continutul etichetei si instructiunilor de utilizare pentru dispozitive medicale
Se admite introducerea pe piata sau punerea in functiune doar a dispozitivelor care poarta marcajul european de conformitate CE, marcaj care semnifica faptul ca aceste dispozitive au fost supuse evaluarii conformitatii . Dispozitivele trebuie sa indeplineasca cerintele esentiale care le sunt aplicabile prevazute in anexa nr. 1din HG 54/2009 , anexa 1 din HG 55/2009 sau anexa 1 din HG 798/ 2003 , tinând seama de scopul propus al acestora.
In ceea ce priveste etichetarea si instructiunile de utilizare, cerintele esentiale prevad urmatoarele:
citeste anuntul integral …
- Anunt important
20.05.2015
Notificarea dispozitivelor medicale la punerea in functiune
Conform HG 54/2009, HG 55/2009, HG 798/2003 si Ordinului Nr. 372/2015,
Producatorul, reprezentantul autorizat al producatorului, importatorul sau distribuitorul stabilit in Romania sau in orice alt stat membru are obligatia sa notifice ANMDM punerea in functiune pe teritoriul Romaniei a urmatoarelor tipuri de dispozitive medicale:
a) dispozitive medicale din clasele IIa, IIb si III;
b) dispozitive medicale pentru diagnostic in vitro care fac obiectul anexei nr. 2 la Hotararea Guvernului nr. 798/2003, cu modificarile si completarile ulterioare;
c) dispozitive medicale pentru diagnostic in vitro de autotestare;
d) dispozitive medicale implantabile active.
Punere in functiune – etapa in care dispozitivul este pus la dispozitia utilizatorului final, fiind gata de utilizare pe piata Uniunii Europene, pentru prima data pentru scopul propus.
Conform Art. 9 al OMS 372 / 2015:
Nerespectarea acestei cerinte constituie contraventie si se sanctioneaza cu amenda de la 2.500 lei la 5.000 lei si interzicerea comercializarii pana la o data stabilita de ANMDM impreuna cu producatorul, reprezentantul autorizat sau distribuitorul, dupa caz, pentru eliminarea neconformitatilor; - Anunt important
20.05.2015
In atentia persoanelor interesate
In ultima perioada se comercializeaza tot mai mult aparate, dispozitive si instrumente de tipul: saltele magnetice, dispozitive cu lumina polarizata, dispozitive de biorezonanta, dispozitive de protectie cu magneti, bandaje magnetice (cotiere, genunchiere, glesniere), aparate pentru terapie wellness, etc, care desi nu sunt inregistrate ca dispozitive medicale promit prevenirea, monitorizarea, investigarea, ameliorarea si/sau tratarea anumitor afectiuni de sanatate.
In cazul multora dintre aceste echipamente nu exista studii clinice concludente care sa confirme eficacitatea in ameliorarea sau tratarea diverselor afectiuni.
Inainte de a achizitiona asemenea produse, informati-va daca sunt declarate ca fiind dispozitive medicale de catre producatorii lor si consultati medicul curant in ceea ce priveste utilizarea acestora pentru afectiunile dorite a fi tratate de dvs. Nu le utilizati fara consultarea unui medic si fara a citi cu atentie instructiunile de utilizare. - Anunt important
16.04.2015
In atentia persoanelor interesate
S-au publicat in Monitorul Oficial OMS nr.308 /17.03.2015 privind controlul prin verificare periodica a dispozitivelor medicale puse in functiune ºi aflate in utilizare (inlocuieste OMS nr.44/2013) OMS nr.309/17.03.2015 pentru aprobarea Normelor metodologice de aplicare a titlului XIX din Legea nr. 95/2006 privind reforma in domeniul sanatatii, referitoare la avizarea activitatilor in domeniul dispozitivelor medicale (inlocuieste OMS nr.748/2014).
Aceste ordine pot fi descarcate de la TEHNIC-LABORATOARE/Legislatie specifica, respectiv EVALUARE UNITATI TEHNICO-MEDICALE/Legislatie specifica.
Cererile tip pentru avizul de functionare, pentru anexa la avizul de functionare si pentru inregistrarea in baza de date a furnizorilor de servicii in domeniul dispozitivelor medicale rezidenti in UE sau SEE se pot descarca de la EVALUARE UNITATI TEHNICO-MEDICALE/Documente utile.
Cererile si corespondenta aferenta activitatilor ANMDM in domeniul dispozitivelor medicale se depun la registratura sediului din Sos.Nicolae Titulescu nr.58, sector 1, dupa urmatorul program: de luni pana joi – orele 9:00-16:00; vineri – orele 9:00-13:00.
Eliberarea documentelor se face in zilele de marti si miercuri, orele 9:00-15:00. - Anunt important
22.10.2014
In atentia persoanelor interesate
Incepand cu data de 13.10.2014, prin publicarea Legii nr.132/2014 privind aprobarea Ordonantei de urgenta a Guvernului nr. 2/2014 pentru modificarea si completarea Legii nr. 95/2006 privind reforma in domeniul sanatatii, precum si pentru modificarea si completarea unor acte normative, ANMDM este Autoritate Competenta pentru dispozitivele medicale, preluand atributiile acesteia de la Ministerul Sanatatii.
Pana la definitivarea noii metodologii, cererile tip din Ordinul MS nr.253/2010 click aici se pot depune la registratura Autoritatii Competente de la punctul de lucru din Sos.N.Titulescu nr.58.
Cererea pentru emiterea avizului de functionare pentru activitatile de optica medicala, protezare auditiva, protezare ortopedica sau reparare, mentenanta si punere in functiune/instalare dispozitive medicale va fi insotita de urmatoarele documente:
a) copie a certificatului de inregistrare ºi a certificatului constatator emise de oficiul registrului comertului sau alt inscris oficial/act normativ care sa ateste infiintarea unitatii solicitante;
b) copie a statutului societatii comerciale/actul constitutiv;
c) dupa caz:
– autorizatie sanitara de functionare sau proces verbal de constatare a conditiilor igienico – sanitare emis DSP;
– autorizatie de mediu
d) dovada detinerii spatiului la care se anexeaza planul incaperilor, cu precizarea dimensiunilor, compartimentarilor si destinatia acestora;
e) lista cuprinzand personalul de specialitate al unitatii , la care se anexeaza copii dupa documentele de studii si instruiri punctuale;
f) declaratie privind domeniul de activitate desfasurat (pentru service se vor mentiona categoriile si tipurile de dispozitive medicale pentru care se executa lucrari de reparare, mentenanta si punere in functiune/ instalare)
g) lista privind echipamentele si dispozitivele de masurare si monitorizare cuprinzand seria, anul de fabricatie, data ultimei etalonari/calibrari;
h) instructiuni de lucru referitoare la activitatile desfasurate sau procedura de service pentru unitatile care au implementat SR EN ISO 9001;2008 sau SR EN ISO 13485:2012, referitoare la activitatile desfasurate;
i) copie dupa certificatul de management al calitatii SR EN ISO 9001:2008 sau SR EN ISO 13485:2012 pentru unitati care presteaza activitati in domeniul service dispozitive medicale, protezare auditiva, protezare ortopedica, alte tipuri de protezare.*
*Certificatele SR EN ISO 9001:2008 si SR EN ISO 13485:2012 trebuie sa fie emise de un organism de certificare, acreditat de un organism national de acreditare (RENAR sau similar). - Anunt important
18.09.2014
Noutati privind dispozitivele medicale
O noua procedura de evaluare a capabilitatii si competentei firmelor care au solicitat emiterea avizului de functionare pentru prestarea de activitati in domeniul dispozitivelor medicale a intrat in vigoare la data de 15.09.2014. Aceasta procedura, noul formular de cerere si chestionarele de evaluare pe tip de activitate pot fi accesate in sectiunea Avize de functionare. - Anunt important
08.11.2011
Chestionar de evaluare a nivelului de satisfactie a clientului
Pentru a veni in sprijinul imbunatatirii permanente a activitatii Departamentului Tehnic-Laboratoare, rugam beneficiarii sa completeze si sa transmita la nr.fax.0212228683, urmatorul chestionar:
descarca chestionarul …
- Anunt important
08.11.2011
Noutati privind dispozitivele medicale
Ca urmare a monitorizarii activitatii desfasurate de catre societatile tehnico-medicale, avizate de catre Ministerul Sanatatiii sau in curs de avizare, care au certificat si implementat sistemul de management al calitatii SR EN ISO 9001:2008 sau SR EN ISO 13485:2004 cu organisme de certificare acreditate de un organism de acreditare national (RENAR sau similar), cat si datorita consultarilor si discutiilor purtate cu o parte din aceste organisme de certificare, ANMDM-Departamentul de evaluare unitati tehnico-medicale precizeaza urmatoarele:
– Domeniul dispozitivelor medicale este reglementat de directive europene (93/42, 98/79, 90/365) si in baza art.6 din Legea nr.176/2000 privind dispozitivele medicale, republicata, cu modificarile ulterioare, precum si a OMS nr.1636/2007, cu modificarile ulterioare, ANMDM efectueaza activitatea de evaluare a organizatiilor care presteaza servicii in domeniul dispozitivelor medicale (optica medicala, protezare ortopedica/ auditiva/ alte tipuri sau reparare, verificare si punere in functiune dispozitive medicale);
– ANMDM “elaboreaza proceduri tehnice specifice in domeniul dispozitivelor medicale”, “evalueaza si/sau auditeaza, la cererea Ministerului Sanatatii, persoanele fizice sau juridice care solicita avizul de functionare” (art.7 din legea mentionata mai sus) si intocmeste raportul de evaluare in baza caruia Ministerul Sanatatii emite acest aviz (art.8, alin.2 din OMS 1636/2007);
– Raportul de evaluare intocmit de ANMDM confirma ca persoana fizica sau juridica ce solicita avizul de functionare indeplineste toate conditiile de lucru, dotare tehnico-materiala, calificare, capabilitate, proceduri si instructiuni pentru a desfasura activitatea respectiva.
Urmarind in timp calitatea serviciilor prestate de furnizorii de servicii in domeniul dispozitivelor medicale, ANMDM a constatat ca nu toti pot demonstra capacitatea de a furniza servicii care in mod constant satisfac cerintele clientilor si cerintele de reglementare aplicabile domeniului de activitate. In acest sens a fost imperios necesara solicitarea certificarii sistemului de management al calitatii, ca o dovada a respectarii acestor cerinte.
Deoarece activitatile evaluate sunt in domeniul dispozitivelor medicale si au implicatii serioase in sanatatea publica, in baza legislatiei in domeniu si avand in vedere ca pentru certificarea sistemelor de management al calitatii in conformitate cu SR EN ISO 13485 (specific dispozitivelor medicale) exista putine organisme acreditate in tara, iar majoritatea organismelor de certificare acreditate in vederea certificarii SR EN ISO 9001:2008 nu folosesc experti tehnici si auditori calificati si cu experienta in domeniul dispozitivelor medicale, pentru a se asigura ca furnizorii de servicii in domeniul dispozitivelor medicale isi desfasoara activitatea in conformitate cu cerintele acestor standarde , ANMDM a intocmit o procedura tehnica proprie de evaluare.
Institutia noastra nu a dorit monopolizarea acestei activitati, a dorit doar sa se asigure ca aceste activitati sunt desfasurate de catre personal calificat
Codurile CAEN 3313, 3314 si 332 nu fac referire explicit la reparare , verificare si punere in functiune dispozitive medicale, iar din experienta ANMDM s-a constatat ca auditorii/ expertii din echipele de audit nu cunosc intotdeauna legislatia specifica domeniului. Acestea au fost motivele care ne-au determinat sa gandim procedura de agreere a organismelor de certificare. Nu s-a inteles reactia organismelor de certificare, atata timp cat ANMDM-ul nu a dorit altceva decat sa analizeze in profunzime satisfacerea cerintelor specifice domeniului.
Deoarece demersul nostru a fost eronat inteles , s-a renuntat la acesta procedura de agreere a organismelor de certificare in activitatea de evaluare a unitatilor de tehnica medicala, mentinandu-se doar cerinta certificarii sistemului de management al calitatii, cu un organism de certificare acreditat.
Evaluarea unitatilor tehnico-medicale care solicita emiterea avizului de functionare, cat si evaluare de supraveghere a acestor unitati, se desfasoara de catre ANMDM- Departamentul EUTM in baza unei proceduri proprii ca si pana acum.


